Роман-А. Леонард,
к.в.н., практикующий ветеринарный врач, президент Российской научно-практической ассоциации ветеринарных нефрологов и урологов (НАВНУ, www.vetnefro.ru)
В статье использованы фото ветеринарного офтальмолога Веры Олейник.
Введение
Диагностика такой широко распространённой во всём мире нефропатии кошек, как ХБП1, в подавляющем числе случаев осуществляется ветеринарными специалистами лишь на основании повышения уровня креатинина и мочевины в сыворотке крови. С азотемией (или т. н. уремической интоксикацией) традиционно, хотя и необоснованно, связывают и большую часть клинических проявлений заключительных этапов почечного континуума.
Даже если отбросить в сторону то обстоятельство, что креатинин и мочевина — это в большей степени лишь биомаркеры почечного поражения2, а не факторы патогенеза и «виновники» большинства осложнений клинического этапа ХБП у кошек, необходимо учитывать и тот факт, что далеко не всегда у животного, погибающего от этой асептической нефропатии (по причине ряда тяжелейших её осложнений: гидроторакса, гидроперикарда, метаболического ацидоза, гиперпаратиреоза, гипертонии и т. д.), азотемия превышает общепринятые3 референтные значения.
Впрочем, возможна и обратная ситуация, когда у клинически здорового животного с безупречными анализами мочи и крови уровень креатинина значительно повышен и выявляется случайно, например при скрининге или при подготовке к рутинной хирургической операции (овариоэктомия и проч.).
Говоря в целом, уровень азотемии далеко не всегда позволяет оценить степень тяжести почечного поражения. Поэтому практически всегда требуется проведение совокупной оценки всех имеющихся у пациента изменений как в общем состоянии, так и отклонений, выявляемых при неинвазивных и, если требуется, инвазивных методах диагностики.
К несчастью, нередки случаи, когда на приём к врачу попадают пациенты с катастрофическими изменениями в ренальной паренхиме и, как следствие этого, набором патологических изменений в структуре/работе различных органов и систем. Но в нефрологическом диагнозе и, соответственно, в жизненно необходимом лечении таким животным необоснованно отказывают лишь на основании того, что уровень азотемии у них находится в пределах формальной нормы. Мало того, на основании некорректных диагнозов таким пациентам могут быть назначены препараты, обладающие абсолютными и относительными4 нефротоксичными свойствами.
Как же диагностировать ХБП у кошек, если азотемия в этом деле не слишком надёжный помощник?
Может возникнуть вопрос: как же определить эти самые тяжёлые структурные изменения в почечной паренхиме, если у кошки с ХБП отсутствует азотемия? Ведь пункционная нефробиопсия с последующими гистоморфологическими исследованиями почечного биоптата — это сложно, опасно, дорого и долго.
Но тут далеко не всё так страшно, как кажется на первый взгляд. Прежде всего, ценность инвазивных методов диагностики нефропатий высока лишь на ранних доклинических этапах их течения. Только тогда результаты исследования могут значимо повлиять на долговременную стратегию нефропротективной терапии. На клиническом этапе ХБП у кошек (а он, как уже было сказано, далеко не всегда гиперазотемический) в почечной паренхиме обычно выявляются ярко выраженные, но весьма однотипные структурные изменения, представляющие различные этапы процессов ренальной деструкции, неминуемо ведущие к единому итогу — нефросклерозу. Результаты пункционной нефробиопсии на клиническом этапе ХБП (т. е. у кошек, у которых не менее 75% почечной паренхимы находятся в состоянии частичной или полной деструкции) никак не способны повлиять на симптоматическую/заместительную терапию, лишь только и возможную в этом случае.
А что же расскажет врачу о тяжёлой почечной деструкции, если не инвазивные методы диагностики? Тут всё весьма банально. И при правильно поставленной работе точно не страшно, не дорого, быстро и экономически целесообразно. В 99% случаев вся необходимая информация будет в анализах мочи. Да, именно, о процессах деструкции в почечной паренхиме и даже об их выраженности может рассказать простой общеклинический анализ мочи. Поскольку протеинурия, гипостенурия, агранулоцитарная лейкоцитурия и проч. безапелляционно об этом свидетельствуют, и давно доказана прямая корреляция этих изменений и степени тяжести необратимого почечного поражения.
Из этого, с одной стороны, следует, что постановка какого угодно нефрологического диагноза на любом этапе почечного континуума невозможна без исследования мочи (исключением, пожалуй, могут быть названы только анурические состояния), а необоснованное пренебрежение этим легкодоступным, высокоинформативным и высокоприбыльным методом диагностики является врачебной ошибкой5. А с другой стороны, особенно если пациент кошка, множество различных патологических изменений, с жалобами на которые владельцы обращаются в клинику, прямо или косвенно могут быть связаны с различными нефропатиями, и прежде всего с ХБП. А следовательно, рекомендация о необходимости исследования мочи у кошек должна быть дана одной из первых, вне зависимости от наличия/отсутствия клинических проявлений и изменений в анализах крови.
Установление степени почечного поражения у кошек с ХБП является важным ещё и потому, что заключительные этапы почечного континуума накладывают как минимум существенные ограничения на использование большинства лекарственных препаратов, поскольку их фармакодинамика и фармакокинетика неразрывно связаны с почками (в т. ч. и поэтому возможно накопление нефротоксичных эффектов даже у средств, проявляющих в иных условиях нефропротективные свойства). Эти обстоятельства обязательно должен учитывать курирующий пациента врач, а узкие специалисты, к которым в случае необходимости животное может быть направлено на консультацию, должны быть проинформированы о почечном статусе пациента и об ограничениях в терапии, который он накладывает.
К примеру, ухудшение качества кожи и шерсти, говоря в общем даже без привязки к какой-либо нозологической форме, весьма распространённая причина обращения в ветеринарную клинику. (А если владельцы не обращают на эту проблему особого внимания, списывая всё, например, на возраст, сухость и жару в квартирах, хроническую линьку и т. д., то врач при первой возможности должен проинформировать их о необходимости и возможных вариантах установления причины появления у животного трихо- и/или дермопатии.) И у таких кошек наверняка будут значимые и стойкие отклонения в анализах мочи. А следовательно, есть все основания для того, чтобы предположить, что вышеназванные изменения являются осложнением ХБП у кошки (или усугубляются ей), которые автор предлагает обозначать как нефрогенный дерматит, или уремическая дерматопатия, если так проще объяснить самому себе или владельцам пациента причину развития этого осложнения — патологическое воздействие на структуры кожи разнообразных биологически активных веществ (прежде всего паратиреоидного гормона), накопление которых является прямым или косвенным следствием декомпенсированной почечной недостаточности.
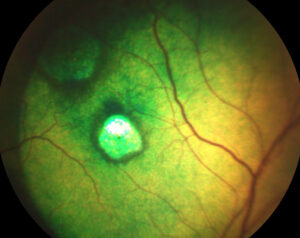
Ещё одним относительно ранним, распространённым и наглядным осложнением ХБП у кошек и собак является поражение глазного дна (снижение светочувствительности сетчатки обычно приводит к легко диагностируемому симптому — патологическому билатеральному мидриазу), а то и глазного яблока в целом (фото 1–6).
 |
 |
| Фото 1. Кошка, 15 лет. Дегенерация сетчатки | Фото 2. Кошка, 14 лет. Отслойка и геморрагии сетчатки |
 |
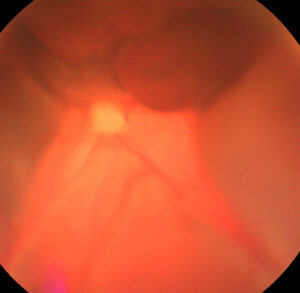 |
| Фото 3. Кошка, 15 лет. Гемофтальм | Фото 4. Кошка, 13 лет. Отслойка сетчатки |
 |
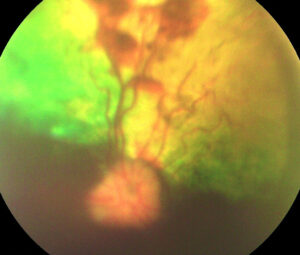 |
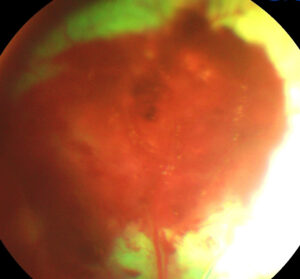
| Фото 5. Кошка, 13 лет. Отслойка сетчатки, гемофтальм | Фото 6. Собака, 12 лет. Отслойка сетчатки, гемофтальм |
Не секрет, что системная гипертензия (в т. ч. и ренальная, тяжесть которой напрямую коррелирует с уровнем протеинурии и гипостенурии) опасна у кошек прежде всего необратимым поражением органов-мишеней, одним из которых являются глаза. Поэтому не стоит с порога отправлять пациента к окулистам, поскольку без терапии основного заболевания и попыток поставить под контроль уровень системной гипертензии заниматься лечением в т. ч. и офтальмологических осложнений ХБП, очевидно, не имеет смысла. А определиться с нефрологическим диагнозом, разъяснить владельцам причины возникших вторичных изменений6 и назначить необходимое пациенту лечение должен, по крайней мере, терапевт, если по какому-то недоразумению в клинике, в которой ведётся приём кошачьих, всё ещё нет ветеринарного нефролога-уролога. А уж потом, при большом желании владельцев, можно и направить кошку с ХБП к узкоспециализированным ветеринарным специалистам. И здесь ни в коем разе нет пренебрежения к уважаемым коллегам, а только огромное желание, чтобы умирающих от ХБП животных, которым «не повезло» с уровнем азотемии, лечили и от основного заболевания, а не только от его разнообразных осложнений, так ловко, зараза их возьми, маскирующихся под разные иные патологии.
Симптомы ХБП, возникающие на её клиническом этапе у пациентов в т. ч. с уровнем азотемии, находящимся в пределах референтных значений, и основные/наиболее вероятные причины их развития приведены в таблице 1.
Оценка степени тяжести ХБП у конкретной кошки требует, возможно, более полной оценки как различных клинических проявлений, так и результатов лабораторных и визуализирующих (т. е. неинвазивных) методов диагностики (а в случае, когда к этому есть показания, также и инвазивных). Поэтому при осмотре необходимо указать владельцам на все, даже на первый взгляд незначительные, изменения в состоянии животного. Именно такой комплексный подход (по совокупности признаков, а не основанный лишь на уровне отдельных лабораторных показателей, например креатинина) поможет и в постановке корректного нефрологического диагноза (на максимально ранних этапах почечного континуума). И при работе с владельцами, которым необходимо детально разъяснить значимость/опасность патологии и возможности (или отсутствие таковых) профилактики и лечения её на различных этапах.
Благодарности
Автор выражает признательность за предоставленные фотографии и поддержку в профессиональной деятельности замечательному офтальмологу Вере Олейник (Московский ветеринарный центр глазных болезней доктора Олейник).
Примечания
1 Хроническая болезнь почек.
2 Наряду с активно внедряемым в последнее время в клиническую практику симметричным диметиларгинином.
3 Вернее, установленные Международным обществом изучения заболевания почек (у мелких домашних животных) — IRIS (www.iris-kidney.com).
4 Степень нефротоксичности у таких препаратов во многом зависит от степени тяжести почечного поражения.
5 А в нефрологическом центре, которым руководит автор статьи, факт подобного пренебрежения расценивается как вражеский демарш и махровый коллаборационизм, направленные на подрыв экономического суверенитета лечебного учреждения (ст. 12-8а УК УЦВНиУ: расстрел на рассвете).
6 В случае с офтальмологическими осложнениями ХБП владельцев кошек необходимо изначально проинформировать о том, что восстановления зрительной функции у пациента, скорее всего, не произойдёт. Это в последующем позволит избежать ряда претензий с их стороны.
Таблица 1
| Клинические признаки ХБП у кошек | Причина/наиболее вероятная причина возникновения |
| Ухудшение качества кожи и шерсти; хроническое выпадение шерсти (исключить стресс-обусловленное, например, на приёме в клинике), значимо превышающее физиологическую норму | 1. Компенсированная (патологически высоким уровнем фосфатурических гормонов) или декомпенсированная гиперфосфатемия и её прямое следствие — гиперпаратиреоз и неконтролируемое выделение и накопление в крови паратиреоидного гормона, воздействие которого на свои рецепторы II типа (длительное время считалось, что у паратиреоидного гормона есть только рецепторы одного, соответственно первого, типа, расположенные на клетках костной ткани), находящиеся в различных структурах кожи, и приводит к изменениям в ней, характерным для кошек с ХБП (нозологическая форма дермопатии, требует уточнения). Кроме того, высокие уровни паратиреоидного гормона обусловливают во всех тканях организма тот или иной уровень дисбаланса между внутри- и внеклеточным ионизированным кальцием, который, помимо прочего, является ключевой внутриклеточной сигнальной молекулой, необходимой для их нормальной функции.
2. Гипертиреоз. |
| Анорексия, рвота
Астения, кахексия |
1. Нефрогенный (уремический1) гастрит, гастроэнтерит и связанные с ними нарушения ферментации пищи, пристеночного пищеварения и т. д.
2. Поражение паратиреоидным гормоном рвотного центра (тошнота, рвота) и структур ЦНС, отвечающих за формирование чувства голода и физиологически обусловленных вкусовых предпочтений. 3. Ятрогения. Такая, например, рекомендация врача: не давайте ничего до тех пор, пока не начнёт есть то, что нужно. Заканчивается гибелью животного от дефицита пластических и энергетических веществ в организме, психическими расстройствами у владельцев и формированием у них стойкой отрицательной позиции к определённым видам диетической продукции. |
| Нарушение аккомодации зрачка — патологический билатеральный мидриаз (исключить стрессогенный, например, связанный с посещением клиники) и снижение светочувствительности сетчатки вследствие структурных изменений на глазном дне (синдром извилистых артерий сетчатки, отёки и кровоизлияния в сетчатку, отслоение сетчатки и т. д.; это всегда патология, не имеющая отношения к стрессу, и поэтому мидриаз, с ней связанный, также всегда является значимым патологическим отклонением) | 1. Гиперактивация симпато-адреналовой (САС), а также тканевого и плазматического компонентов ренин-ангиотензин-альдостероновой системы (РААС) и формирование первоначально интраренальной, а затем и стойкой системной гипертензии.
2. Формирование порочного круга рено-кардиального и кардио-ренального континуумов: усугубление тяжести системной гипертензии. 3. Глаукома. |
| Очень часто у кошек с ХБП изменения на глазном дне видны и без использования специальных средств2. «Благодаря» патологическому мидриазу в направленном луче света (от смартфона, например) у кошек с тяжёлыми нефропатиями (в т. ч. и с «нормальным» уровнем азотемии) глазное дно выглядит грязно-красно-зелёным, грязно-жёлто-красным или серо-жёлтым с красными вкраплениями (приблизительно так выглядят осенние листья в лужах различной степени загрязнённости). Фото 1–6. Благодаря уже стрессовому мидриазу у кошек, у которых глазное дно не поражено (хотя это не гарантирует того, что у пациента совершенно здоровые почки), при аналогичных методах осмотра можно увидеть лучистое изумрудно-зелёное свечение3. | |
| Нефрогенный (уремический) перикардит (в т. ч. с перикардиальным выпотом) | 1. Воздействие паратиреоидного гормона на свои рецепторы II типа, расположенные в структурах перикарда.
2. Гиперактивация САС и РААС. |
| Нистагм глазных яблок, скрежет зубами, нарушение координации движений, манежные движение головой, шейная вентрофлексия, кома | 1. Токсическое поражение центральной и периферической нервной системы.
2. Метаболический ацидоз. |
| Инспирационная одышка (в т. ч. с высунутым языком), брюшной тип дыхания | 1. Патологическое перераспределение жидкости в организме4 — гидроторакс (не путать с отёком легких) и гидроперикард. Часто на фоне общей гиповолемии.
2. Тромбоз лёгочных артерий на фоне системной гипертензии (положение усугубляется ещё и высокой порозностью этих артерий, свойственной кошкам). 3. Ацидоз. |
| Хронический дистресс (его развитие в некоторых случаях требует частичного или даже полного отказа от диагностических и лечебных мероприятий) | 1. Ухудшение общего самочувствия, дурнота, тошнота, сильная слабость (кошки в принципе крайне плохо переносят боль и близкие к ней по дискомфорту состояния). Автор располагает лишь единичными показаниями самих кошек об их ощущениях на клиническом этапе ХБП, явно недостаточными для глобального обобщения. Но, вероятнее всего, это что-то близкое к мироощущению при похмелье или пищевой токсикоинфекции средней или тяжёлой степени.
2. Необходимость проведения различных диагностических и лечебных процедур как в клинике, так и в домашних условиях. |
| Галитоз | 1. Нефрогенный (уремический) гингивит, гастроэнтерит.
2. Метаболический ацидоз. |
| Парез/паралич задних конечностей (или состояния, клинически напоминающие эти патологии) | 1. Тромбоз подвздошных артерий.
2. Токсическое поражение периферической нервной системы. |
| Иммунодефицитные состояния и обострение вирусных инфекций, ранее имеющих латентное течение | 1. Нефрогенный иммунодефицит, развивающийся в т. ч. и потому, что почки вырабатывают ряд аминокислот и иных БАВ, являющихся неотъемлемыми компонентами иммунной системы.
2. Хронический дистресс, развивающийся у некоторых кошек на фоне проведения лечебно-диагностических мероприятий (требует терапевтической коррекции рядом психотропных препаратов). |
1 Термин «уремический» совершенно не отражает всё многообразие нарушений в организме, возникающих на клиническом этапе ХБП у кошек, и фактически увязывает патогенез этой многофакторной нефропатии лишь с накоплением в организме конечных продуктов азотистого обмена. А также ставит знак равенства между степенью тяжести ХБП и уровнем азотемии. Что в корне неверно. Поэтому закостенелый термин «уремический» употребляется в данной статье лишь отдавая дань традиции и для некоторого облегчения понимания материала врачами, только недавно начавшими интересоваться ветеринарной нефрологией.
2 Капель, расширяющих зрачок, дорогих и очень дорогих офтальмоскопов, высококвалифицированных офтальмологов и т. д., хотя последнее, конечно, и не возбраняется, если у кошки уже определён нефрологический статус или офтальмологическое обследование проводится параллельно с этим.
3 Поэтому предложение, высказанное в одной известной песне «да загляни-ка в глазки ей…» может помочь не только в поиске определённого рода сокровищ, но также, например, и в установлении почечного статуса будущей избранницы.
4 Крайне неблагоприятный с прогностической точки зрения симптом ХБП у кошек, свидетельствующий о вовлечении в её патогенез сердечной и дыхательной систем. Прежде чем приступать к осмотру животного или любым иным действиям с ним (например, к термометрии, фиксации, постановке в/в катетера и т. д.), необходимо отойти от пациента в сторону и проинформировать владельцев о том, что животное может в любой момент погибнуть от острой полиорганной недостаточности.
Литература
- Barber P.J., Elliott J. Feline chronic renal failure: calcium homeostasis in 80 cases diagnosed between 1992 and 1995. J Small Anim Pract. 1998 Mar;39(3):108–16.
- Bartges Joe, Polzin David J. Nephrology and Urology of Small Animals. WILEY-BLACKWELL/ A John Wiley & Sons, Ltd., Publication, 2011.
- Brown, S., C. Atkins, et al. (2007). Guidelines for the identification, evaluation, and management of systemic hypertension in dogs and cats. J Vet Intern Med 21: 542–558.
- Elliott, J., P.J. Barber, et al. (2001). Feline hypertension: clinical findings and response to antihypertensive treatment in 30 cases.
J Small Anim Pract 42: 122–129. - KDIGO Clinical Practice Guideline for the Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD–MBD) // Kidney Int. 2009; 76 (suppl 113): S1–S130.
- Komaba H., Goto S., Fukagawa M. Critical issues of PTH assays in CKD // Bone. 2009; 44: 666–670.
- Noordzij M., Korevaar J.C., Boeschoten E.W., Dekker F.W., Bos W.J., Krediet R.T. The Kidney Disease Outcomes Quality Initiative (K/DOQI) Guideline for Bone Metabolism and Disease in CKD: association with mortality in dialysis patients. Am J Kidney Dis (2005) 46:925–932.
- Slatopolsky E. Role of phosphorus in the pathogenesis of secondary hyperparathyroidism //Am J Kidney Dis. 2001; 37: 54–57.
- Slatopolsky Е., Brown А., Dusso А. Pathogenesis of secondary hyperparathyroidism // Kidney Int. 2005; Vol. 56, Supplement 73: S14–S19.
- www.iris-kidney.com.
- www.vbps-online.org.
- Ветчинникова О. Н. Гиперпаратиреоз при хронической болезни почек. Эффективная фармакотерапия. Урология и Нефрология. Спецвыпуск (44), 2013.
- Волгина Г. В., Перепечёных Ю. В. Лечение вторичного гиперпаратиреоза у больных с хронической почечной недостаточностью (Практические рекомендации). Нефрология и диализ, Т. 2, № 4, 2000.
- Ермоленко В. М., Волгина Г. В., Добронравов В. А. и др. Национальные рекомендации по минеральным и костным нарушениям при хронической болезни почек. Российское диализное общество. «Нефрология и диализ» Т. 13, № 1 2011.
- Кирк Роберт. У., Бонагура Дж. Д. Современный курс ветеринарной медицины Кирка. Аквариум, 2014.
- Рожинская Л. Я. Вторичный гиперпаратиреоз и почечные остеопатии при хронической почечной недостаточности. Нефрология и диализ. Т. 2, № 4, 2000.
СВМ № 2/2018