Willem J. Botha1, Varaidzo Mukorera1, Robert M. Kirberger1
1 Department of Companion Animal Clinical Studies, University of Pretoria, South Africa.
На осмотр был представлен пятилетний некастрированный кобель породы йоркширский терьер, у которого отмечалась вялость и отсутствие аппетита в течение шести дней. В процессе клинического осмотра было выявлено скопление налёта на зубах, а также вовлечение брюшных мышц в дыхательный процесс и приглушённые тоны сердца. Рентгенография грудной клетки выявила увеличенный шарообразный сердечный силуэт с лёгкой степенью пневмоперикарда; в то время как трансторакальное ультразвуковое исследование выявило перикардиальный выпот, после чего с помощью перикардиоцентеза, цитологии и посева бактериальных культур был поставлен диагноз септического перикардита. Были выделены культуры трёх полирезистентных бактерий, две из которых ранее уже связывали с развитием газообразующих инфекций. Септический перикардит не удалось вылечить с помощью медикаментозной терапии, и, вследствие этого, была выбрана эвтаназия. На патологоанатомическом осмотре обнаружили хроническое костно-хрящевое инородное тело пищевода у собаки, расположенное краниально к основанию сердца. Септический перикардит и пневмоперикард редко встречаются у собак. Это первый описанный случай пневмоперикарда, вызванного полирезистентными бактериями, и второй описанный случай септического перикардита, связанного с инородным телом пищевода.
Введение
Неопластический и идиопатический экссудаты составляют наибольшую часть перикардиальных выпотов у собак [2; 11]. Септический перикардит, вызывающий перикардиальный выпот, встречается редко [11]. Способность вызывать септический перикардит приписывалась грибкам (аспергиллез, Candida albicans и кокцидиомикоз), бактериям (Acinetobacter spp., Actinomyces, Bacteroides, Nocardia, Pasteurella multocida, Pseudomonas, Staphylococcus, Streptococcus и возбудителю туберкулёза) и паразитам (дирофиляриоз и лейшманиоз) [5; 15; 18; 19]. Причинами септического перикардита обычно являются раны от укусов [6], внутриперикардиальное инородное тело у собак, миграция остей трав [1; 23], введение препаратов, подавляющих иммунитет [18], а также распространение инфекции с кровотоком [14; 19] и локальное распространение инфекции [17]. Лечение септического перикардита проводится с помощью перикардиоцентеза для удаления экссудата, а также с помощью введения необходимых антимикробных препаратов; в то время как для постоянного дренажа экссудата рекомендуется перикардэктомия [1].
Данный отчёт описывает клинический случай септического перикардита, вызванного группой полирезистентных бактерий и связанного с ним пневмоперикарда у йоркширского терьера с хроническим субклиническим инородным телом пищевода.
Этические соображения
Данный отчёт является ретроспективным описанием клинического случая у собаки, являющейся собственностью владельца, с использованием данных, полученных из клинических записей Ондерстепортской ветеринарной академической больницы. При жизни питомец подвергся госпитализации и лечению в соответствии со стандартными протоколами обращения с животными, находящимися в собственности клиента. Тестов и лечения в исследовательских целях не проводилось. Владелец предоставил подписанное стандартное информированное согласие, разрешающее использование данных и изображений для публикации.
Описание клинического случая
Пятилетний некастрированный кобель породы йоркширский терьер был направлен в больницу с вялостью и отсутствием аппетита в течение шести дней. Состояние собаки не улучшилось после лечения различными антибиотиками (цефалексин, метронидазол, энрофлоксацин и амоксициллин с клавулановой кислотой; дозы, длительность лечения и производители препаратов не были указаны). Собака была единственным домашним животным из пригородного района; в анамнезе жизни отсутствовали сведения о путешествиях и предыдущих заболеваниях. На осмотре конституция собаки была оценена как плохая (2/5), были также выявлены сильное скопление зубного налёта, периодонтит и абдоминальный компонент дыхания. Сердечные тоны были приглушены, слизистые оболочки имели бледно-розовый цвет, скорость наполнения капилляров была 1,5 сек., а периферический пульс был в норме.
Моча, собранная с помощью цистоцентеза, отличалась тёмно-жёлтым цветом и мутностью, но была адекватно концентрирована и содержала небольшое количество белка, выявленного с помощью тест-полосок. Стандартный биохимический и гематологический анализы крови выявили сильную нейтрофилию со сдвигом влево, умеренную гипоальбуминемию и небольшую гипокалиемию (таблица 1).
Таблица 1. Аномальные показатели гематологического и биохимического анализов крови
| Тест | Результат | Единица измерения | Референтный интервал | |
| Лейкоциты | 35,17 | × 109/L | 6–15 | |
| Сегментные нейтрофилы | 27,43 | × 109/L | 3–11,5 | |
| Палочкоядерные нейтрофилы | 6,33 | × 109/L | 0–0,5 | |
| Лимфоциты | 0,70 | × 109/L | 1–4,8 | |
| Моноциты | 0,00 | × 109/L | 0,15–1,35 | |
| Эозинофилы | 0,00 | × 109/L | 0,1–1,25 | |
| Альбумин | 14,20 | g/L | 28–41 | |
| Калий | 3,00 | mmol/L | 3,6–5,1 | |
УЗИ брюшной полости выявило клинически незначимые мелкие почечные камни, в то время как УЗИ грудной клетки через подгрудинное чреспечёночное окно показало отсутствие нормального артефакта «зеркального отражения» из-за наличия анэхогенной жидкости с множественными эхогенными вкраплениями, многие из которых имели дистальные артефакты реверберации. По результатам УЗИ был поставлен диагноз предполагаемого плеврального выпота с вкраплениями пузырьков свободного газа. Дальнейшее обследование было сосредоточено на грудной клетке. Ортогональные рентгеновские снимки грудной клетки выявили сильно увеличенный шарообразный силуэт сердца, занимающий шесть межрёберных пространств с большой областью контакта между сердцем и грудиной, простирающийся до седьмого грудинного сегмента (рис. 1). На снимке в боковой проекции в пределах силуэта сердца присутствовали как минимум три центральных газовых просветления, наибольшее из которых было 12 мм в диаметре. Отсутствовало какое-либо указание на патологию лёгких или плевры. В качестве дифференциального диагноза рассматривали перитонеально-перикардиальную диафрагмальную грыжу (ППДГ), однако отсутствие других рентгенографических изменений, характерных для ППДГ, таких как присутствие кишечника в пределах силуэта сердца, сделало этот диагноз маловероятным; в то же время подозревалось присутствие свободного газа, возможно, производимого бактериями в перикардиальной полости. Присутствие свободного газа в перикардиальном выпоте подтвердили с помощью трансторакального УЗИ. Полоса перикардиальной жидкости была до 12 мм шириной и вызвала небольшую тампонаду стенки правого предсердия. С помощью перикардиоцентеза удалили 25 мл мутной красно-жёлтой жидкости, при этом сразу после удаления жидкости ширина выпота уменьшилась до 2 мм. Анализ жидкости подтвердил присутствие септического экссудата. Цитологическое исследование выявило преобладание дегенеративных нейтрофилов, фагоцитировавших палочковидные бактерии, а также присутствие двух морфологически различных кокковых форм, что указывало на инфекционный процесс, вызванный группой бактерий (рис. 2). В ходе исследования культуры бактерий и антибиотикочувствительности септического экссудата выделили бактерии видов Enterococcus faecalis, Klebsiella pneumoniae и метициллинрезистентный Staphylococcus aureus (MRSA). Данные результаты соответствовали результатам цитологии, где обнаружили одну колонию бактерий бациллярной формы (Klebsiella pneumoniae) и две кокковые колонии (Enterococcus faecalis and Staphylococcus spp.). Все изоляты были в значительной степени полирезистентны к антибиотикам, которые обычно используются в тесте на антибиотико-чувствительность. Был поставлен диагноз септического перикардита и связанного с ним пневмоперикарда.
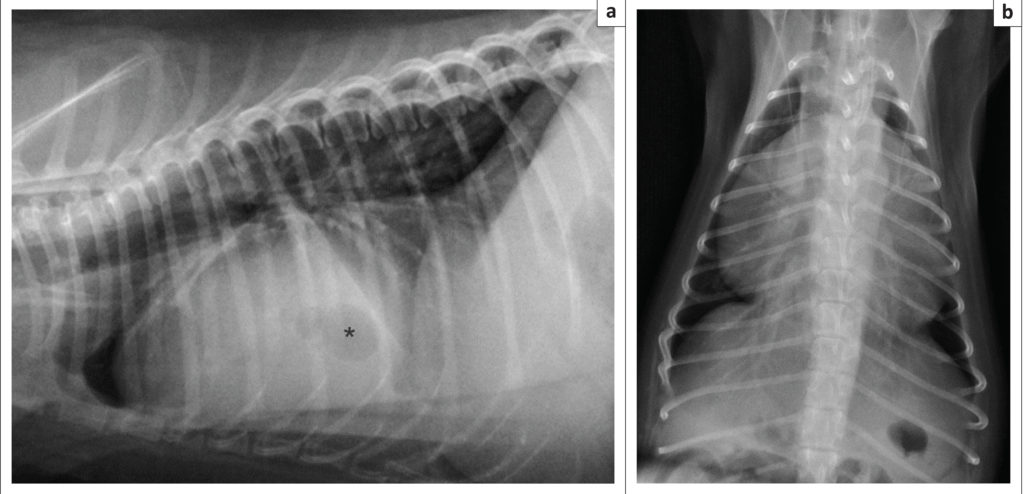 |
| Рис. 1. Рентгеновские снимки в правой боковой (а) и дорсо-вентральной (б) проекциях. (а) Обратите внимание на чрезвычайно сильно увеличенный шарообразный силуэт с фокальными круглыми просветами, являющимися пузырьками газа (*), наложенными на центральный силуэт сердца. (б) Обратите внимание на широкую зону контакта между силуэтом сердца и диафрагмой, что послужило причиной неправильного диагноза плеврального выпота во время УЗИ брюшной полости. Изображения сделаны Sr. Olivier, отделение визуальной диагностики, Ондерстепортская ветеринарная академическая больница |
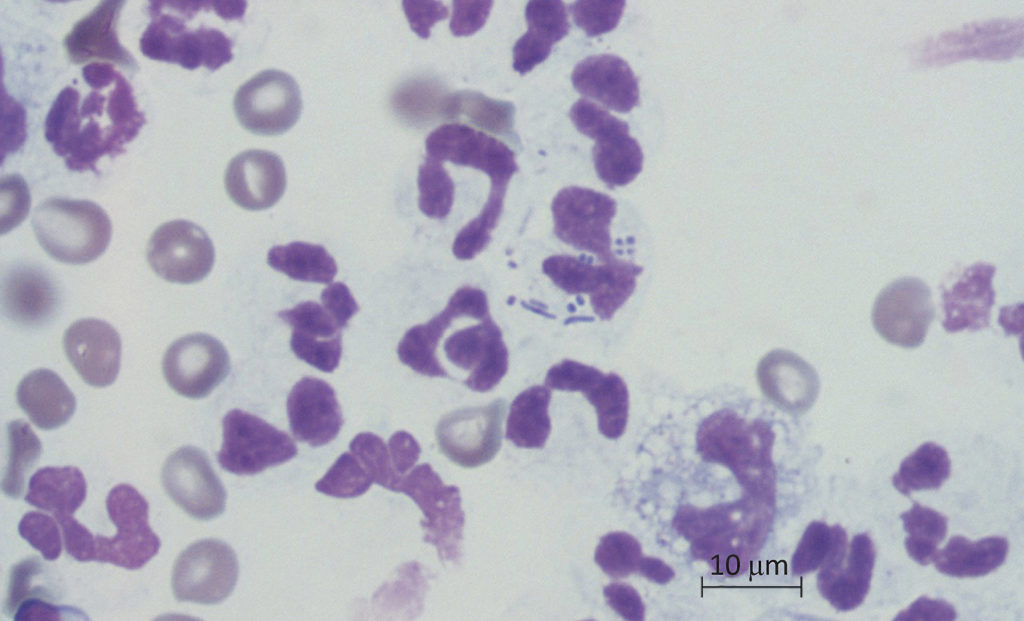 |
| Рис. 2. Световая микрофотография мазков перикардиального выпота. Отмечается преобладающее число дегенерированных нейтрофилов, фагоцитирующих палочки и кокки. Три вида бактерий были выделены из перикардиальной жидкости. Фотомикрография была выполнена Mrs Muller, отделение клинической патологии, отделение клинической диагностики мелких домашних животных, университет Претории |
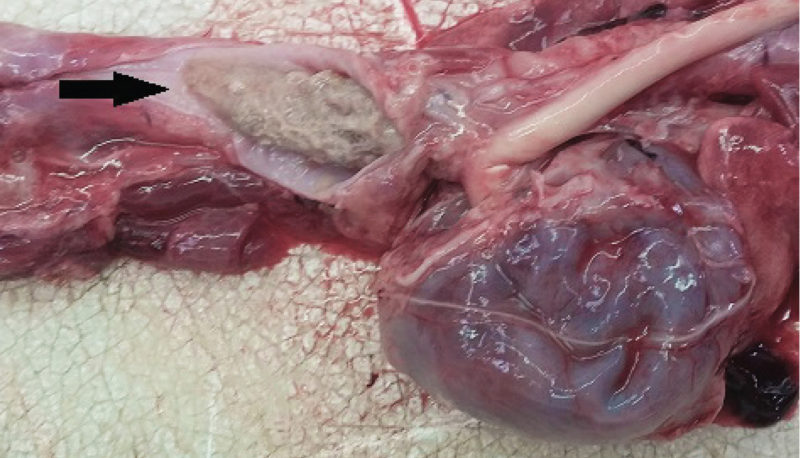
Владелец отказался от перикардэктомии из-за финансовых трудностей и выбрал медикаментозное лечение. До получения результатов теста на антибиотикочувствительность лечение собаки проводили с помощью амоксициллина с клавулановой кислотой (Sandoz Co-amoxyclav 0,6 g, Sandoz SA [Pty] Ltd) в дозе 20 мг/кг ежедневно три раза в день внутривенно и энрофлоксацина (Baytril 5%, Bayer [Pty] Ltd) в дозе 5 мг/кг один раз в день подкожно. После получения результатов антибиотикочувствительности энрофлоксацин был заменён на амикацин (Amikacin-Fresenius, Fresenius Kabi) в дозе 20 мг/кг один раз в день внутривенно. Также проводили внутривенные вливания раствора Рингера лактата (Ringer-lactate solution, Fresenius Kabi) со скоростью 7 мл/час с добавлением 40 ммоль раствора хлорида калия (Adco-Potassium Chloride 15%, Adcock Ingram Ltd). Через пять дней после первоначального диагноза повторное рентгеновское исследование грудной клетки выявило небольшое увеличение перикардиального выпота с образованием фибриновых спаек, однако отсутствовали признаки тампонады сердца. Спустя восемь дней после госпитализации у собаки развился умеренный асцит из модифицированного транссудата, и рентгеновское исследование грудной клетки выявило ухудшение перикардиального выпота (ширина 5 мм, правая парастернальная позиция по короткой оси, положение лёжа на животе) с обширными эхогенными фибриновыми спайками и трепетаниями стенок правого предсердия и желудочка, что указывало на сердечную тампонаду, возможно вследствие сдавливающего (констриктивного) перикардита. Владелец животного выбрал эвтаназию из-за финансовых трудностей и плохого прогноза для животного. Патолого-анатомическое вскрытие подтвердило наличие септического перикардита и связанную с ним застойную правостороннюю сердечную недостаточность. Также в пищеводе краниально к основанию сердца был обнаружен фрагмент хряща (5×2 см), что было связано с развитием местного хронического язвенного воспаления пищевода (рис. 3 и 4). Сообщения между пищеводом и околосердечной сумкой обнаружено не было.
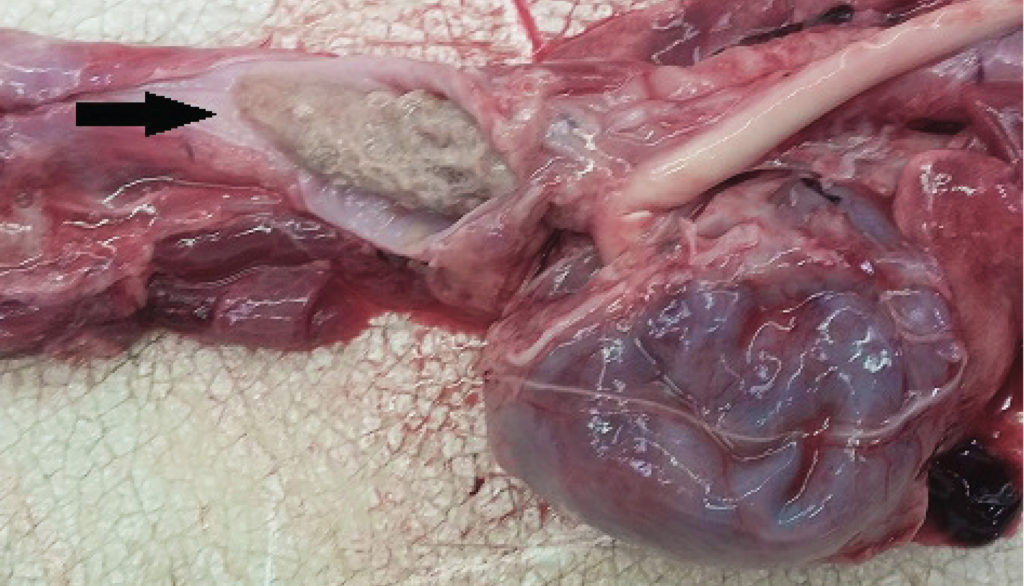 |
| Рис. 3. Фотография патолого-анатомического вскрытия. Обратите внимание на хрящевое инородное тело с застрявшими в нем фрагментами пищи (отмечено стрелкой), расположенное в пищеводе краниально к основанию сердца. Фотография сделана авторами |
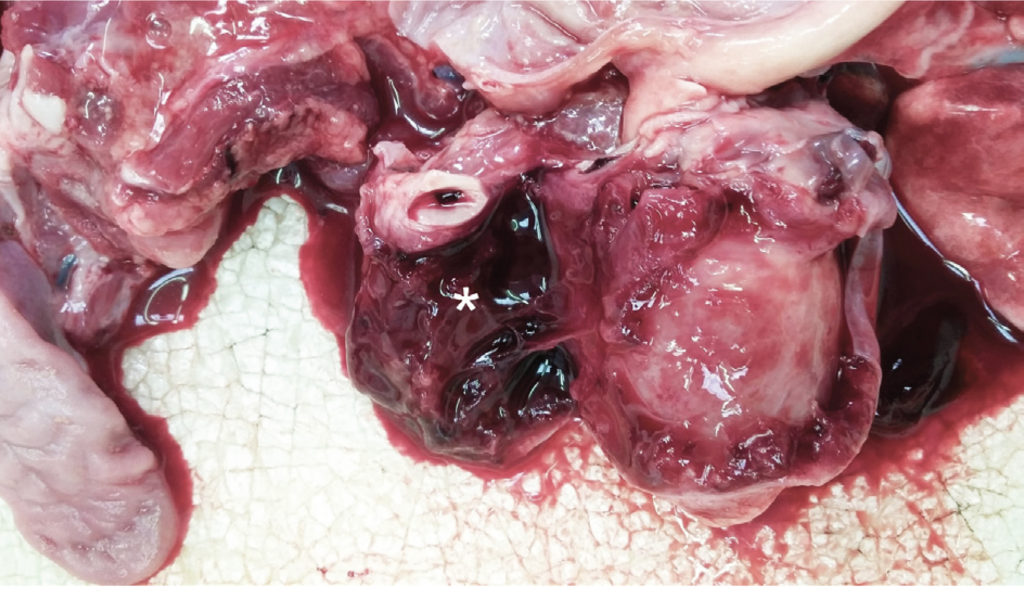 |
| Рис. 4. Фотография патолого-анатомического вскрытия. Околосердечная сумка рассечена и отогнута в сторону, чтобы показать эпикард. Отметьте явные фиброзные изменения на поверхностях эпикарда и околосердечной сумки, свойственные сдавливающему (констриктивному) перикардиту. Фотография сделана авторами |
Обсуждение
Перикардиальный выпот, включающий септический перикардит, в большинстве случаев возникает у крупных пород собак [11]. В одном отчёте о септическом перикардите у йоркширского терьера этиологическая причина была неизвестна [25]. В нашем случае об истинной причине можно только предполагать.
Распространение инфекции с током крови вследствие периодонтита считали убедительной причиной, которая была предложена в качестве объяснения в случае с кошкой с периодонтитом после проведения стоматологической процедуры [14]. Однако подобная причина маловероятна в нашем случае, учитывая тот факт, что перикардит был вызван группой бактерий.
В случаях септического перикардита обычно описывают полибактериальные инфекции [1; 22], указывающие либо на прямое введение бактерий, колонизацию условно-патогенными бактериями или инфекцию вследствие снижения иммунитета [25]. В нашем случае причиной инфекции или миграции пузырьков газа могла стать уже зажившая на тот момент проникающая рана пищевода и околосердечной сумки. В литературе уже описывалось проникающее ранение пищевода костным инородным телом, вызвавшим септический перикардит [12]. Обзорные рентгеновские снимки грудной полости не показали признаков присутствия костно-хрящевого инородного тела пищевода у собаки при первичном обследовании. Таким образом, отсутствовало указание на необходимость применения более продвинутых методов визуальной диагностики или эндоскопии для поиска инородного тела у собаки. Тщательное ретроспективное исследование рентгеновских снимков вместе с результатами патолого-анатомического вскрытия помогло выявить возможное присутствие инородного тела пищевода у входа в грудную полость. Наконец, отсутствие видимого сообщения и воспаления средостения на вскрытии ставит под сомнение факт проникающего ранения околосердечной сумки.
Изначально перикардиальный выпот был ошибочно диагностирован как плевральный выпот на УЗИ брюшной полости из-за широкой области контакта между перикардиальным мешком и диафрагмой. Однако была правильно определена септическая природа жидкости из-за присутствия в ней реверберирующих эхогенных вкраплений, указывающих на наличие мелких пузырьков газа. На рентгеновских снимках были видны как минимум три пузырька газа в самой верхней части сердечного силуэта, что сделало возможным постановку диагноза пневмоперикарда. Пневмоперикард — это скопление газа в перикардиальной полости, редко отмечающееся у собак и обычно не связанное с перикардиальным выпотом [16]. Было показано, что экспериментально вызванный пневмоперикард влечёт за собой гемодинамические изменения, сходные с таковыми при перикардиальном выпоте, и служит причиной сердечной тампонады [20]. В литературе были описаны случаи возникновения пневмоперикарда вследствие травмы, пневмонии, эмфиземы средостения, абсцесса лёгкого, бронхо-лёгочного заболевания и сообщения между лёгкими и перикардом, однако в этих случаях пневмоперикард был более серьёзным, по сравнению с лёгким пневмоперикардом в нашем случае [3; 9]. Газ, проникший в перикардиальную полость в результате проникающей раны пищевода и перикарда, со временем бы рассосался, и, таким образом, производство газа бактериями в перикардиальной полости являлось более вероятным. У человека производство газа при тканевых инфекциях приписывают бактериям Staphylococcus aureus и Klebsiella pneumoniae [13; 21].
Лечение септического перикардита, вызванного бактериями, скудно описано в литературе. Перикардэктомия была описана в качестве эффективного метода лечения септического перикардита, а также было описано увеличение среднего времени выживания в случаях идиопатического перикардиального выпота, лечение которого проводилось с помощью перикардэктомии [1; 5; 7; 11; 24). Однако кажется, что перикардэктомия необходима в большинстве случаев для предотвращения сдавливающего (констриктивного) перикардита, который без перикардэктомии имеет плохой прогноз [1; 12; 19; 22].
Цитологическое исследование предоставляет точный диагноз в случае инфекционного перикардита [4]. Исследование культуры бактерий может помочь в диагностике бактерий, не выявленных при цитологическом исследовании [1]. В нашем случае тревожным был факт резистентности изолятов ко многим антибиотикам.
Enterococcus faecalis является симбионтом желудочно-кишечного тракта собак и считается главной больничной инфекцией с обширной устойчивостью ко многим препаратам [10]. Внебольничная инфекция MRSA, необычная для животных, однако, является эндемической инфекцией во многих человеческих лечебных учреждениях [26]. Klebsiella pneumonia это грам-отрицательная факультативно анаэробная бактерия, которая считается незначительным комменсалом, однако часто связана с оппортунистическими и госпитальными инфекциями [8]. Межвидовую передачу бактерий между собаками и человеком давно подозревали, однако подтвердить её сложно. Так как оба владельца собаки работали в области здравоохранения, они могли быть колонизированы множественными полирезистентными микроорганизмами. Из-за ограниченного и непродолжительного контакта животного с больничной средой наиболее вероятным кажется факт внебольничной инфекции полирезистентными бактериями. Однако множественные антимикробные агенты, применённые до направления собаки в больницу, возможно, играли роль в селекции полирезистентных изолятов. Полирезистентная природа инфекции подчёркивает необходимость разумного использования антимикробных препаратов во всех сферах ветеринарной практики.
Заключение
Насколько известно авторам, данный случай является только вторым описанным случаем септического перикардита, возможно, связанного с инородным телом пищевода у собаки, и первым описанным случаем пневмоперикарда вследствие септического перикардита, вызванного группой полирезистентных бактерий.
Благодарности
Авторы благодарят лабораторию клинической патологии отделения клинических наук мелких домашних животных (факультет ветеринарной медицины университета Претории, Ондерстепорт, ЮАР), за их значительный вклад в клиническую диагностику этого случая.
Конфликт интересов
Авторы заявляют об отсутствии каких-либо финансовых и личных отношений, которые могли ненадлежащим образом повлиять на написание этой статьи.
Вклад авторов
W.J.B. был главным клиницистом, ответственным за этот клинический случай, и автором обзора литературы и главной части статьи при клиническом руководстве V.M.; R.M.K. выполнил и описал визуальную диагностику данного клинического случая.
Литература
- Aronson, L.R. & Gregory, C.R., 1995. ‘Infectious pericardial effusion in five dogs’, Veterinary Surgery 24, 402–407. https://doi.org/10.1111/j.1532–950X.1995. tb01351.x.
- Berg, R.J. & Wingfield, W., 1984. ‘Pericardial-effusion in the dog — A review of 42 cases’, Journal of the American Animal Hospital Association 20, 721–730.
- Borgonovo, S., Rocchi, P.M., Raiano, V., Diana, D. & Greci, V., 2014. ‘Spontaneous pneumopericardium in a dog with bronchopulmonary disease complicated by pyothorax and pneumothorax’, Canadian Veterinary Journal 55, 1186.
- Cagle, L.A., Epstein, S.E., Owens, S.D., Mellema, M.S., Hopper, K. & Burton, A.G., 2014. ‘Diagnostic yield of cytologic analysis of pericardial effusion in dogs’, Journal of Veterinary Internal Medicine 28, 66–71. https://doi.org/10.1111/jvim.12253.
- Casamian-Sorrosal, D., Fournier, D., Shippam, J., Woodward, B. & Tennant, K., 2008. ‘Septic pericardial effusion associated with pulmonary and pericardial botryomycosis in a dog’, Journal of Small Animal Practice 49, 655–659. https:// doi.org/10.1111/j.1748-5827.2008.00605.x.
- Fuentes, V.L., Long, K.J., Darke, P.G.G. & Burnie, A.G., 1991. ‘Purulent pericarditis in a puppy’, Journal of Small Animal Practice 32, 585–588. https://doi. org/10.1111/j.1748-5827.1991.tb00893.x.
- Gilson, S.D., Soderstrom, M.J., Robertson, T.A., Gorman, S.C. & Boston, R.C., 2005. ‘Subtotal pericardectomy and epicardial excision for treatment of coccidioidomycosis-induced effusive-constrictive pericarditis in dogs: 17 cases (1999–2003)’, Journal of the American Veterinary Medical Association 111, 435–440. https://doi.org/10.2460/javma.2005.227.435.
- Glickman, L.T., 1981. ‘Veterinary nosocomial Klebsiella infections’, Journal of the American Veterinary Medical Association 179, 1389–1392.
- Hassan, E.A., Torad, F.A. & Shamaa, A.A., 2015. ‘Pneumopericardium secondary to pneumomediastinum in a golden retriever dog’, Topics in Companion Animal Medicine 30, 62–64. https://doi.org/10.1053/j.tcam.2015.07.009.
- Jackson, C.R., Fedorka-Cray, P.J., Davis, J.A., Barrett, J.B. & Frye, J.G., 2009. ‘Prevalence, species distribution and antimicrobial resistance of enterococci isolated from dogs and cats in the United States’, Journal of Applied Microbiology 107, 1269–1278. https://doi.org/10.1111/j.1365-2672.2009.04310.x.
- Johnson, M.S., Martin, M., Binns, S. & Day, M.J., 2004. ‘A retrospective study of clinical findings, treatment and outcome in 143 dogs with pericardial effusion’, Journal of Small Animal Practice 45, 546–552. https://doi.org/10.1111/j.1748-5827.2004.tb00202.x.
- Kolm, U.S., Kosztolich, A., Hoegler, S. & Kneissl, S., 2001. ‘Canine traumatic pericarditis by an esophageal foreign body’, Journal of Veterinary Cardiology 3, 17–21. https:// doi.org/10.1016/S1760-2734(06)70011-X.
- Lee, H.-L., Lee, H.-C., Guo, H.-R., Ko, W.-C. & Chen, K.-W., 2004. ‘Clinical significance and mechanism of gas formation of pyogenic liver abscess due to Klebsiella pneumoniae’, Journal of Clinical Microbiology 42, 2783–2785. https://doi. org/10.1128/JCM.42.6.2783-2785.2004.
- Lobetti, R., 2007. ‘Anaerobic bacterial pericardial effusion in a cat: Clinical communication’, Journal of the South African Veterinary Association 78, 175–177. https://doi.org/10.4102/jsava.v78i3.313.
- Majoy, S.B., Sharp, C.R., Dickinson, A.E. & Cunningham, S.M., 2013. ‘Septic pericarditis in a cat with pyometra’, Journal of Veterinary Emergency and Critical Care 23, 68–76. https://doi.org/10.1111/vec.12008.
- Maki, D.D., Sehgal, M., Kricun, M.E. & Gefter, W.B., 1999. ‘Spontaneous tension pneumopericardium complicating staphylococcal pneumonia’, Journal of Thoracic Imaging 14, 215–217. https://doi.org/10.1097/00005382-199907000-00010.
- Miller, M.W., Fox, P.R. & Saunders, A.B., 2004. ‘Pathologic and clinical features of infectious endocarditis’, Journal of Veterinary Cardiology 6, 35–43. https://doi. org/10.1016/S1760-2734(06)70056-X.
- Mohri, T., Takashima, K., Yamane, T., & Yamane, Y., 2009. ‘Purulent pericarditis in a dog administered immune-suppressing drugs’, Journal of Veterinary Medical Science 71, 669–672. https://doi.org/10.1292/jvms.71.669.
- Peterson, P.B., Miller, M.W., Hansen, E.K. & Henry, G.A., 2003. ‘Septic pericarditis, aortic endarteritis, and osteomyelitis in a dog’, Journal of the American Animal Hospital Association 39, 528–532. https://doi.org/10.5326/0390528.
- Reed, J.R. & Thomas, W.P., 1984. ‘Hemodynamics of progressive pneumopericardium in the dog’, American Journal of Veterinary Research 45, 301–307.
- Saliba, W.R., Goldstein, L.H., Raz, R., Mader, R., Colodner, R. & Elias, M.S., 2003. ‘Subacute necrotizing fasciitis caused by gas-producing Staphylococcus aureus’, European Journal of Clinical Microbiology and Infectious Diseases 22, 612–614. https://doi.org/10.1007/s10096-003-1023-2.
- Stafford Johnson, M.S., Martin, M.W.S. & Stidworthy, M.F., 2003. ‘Septic fibrinous pericarditis in a cocker spaniel’, Journal of Small Animal Practice 44, 117–120. https://doi.org/10.1111/j.1748-5827.2003.tb00131.x.
- Straw, B.E., Ogburn, P. & Wilson, J.W., 1979. ‘Traumatic pericarditis in a dog’, Journal of the American Veterinary Medical Association 174, 501–503.
- Veloso, G.F., Manteiga, E.F., Trehy, M., Freeman, A., McConnell, J.F. & McEwan, J.D., 2014. ‘Septic pericarditis and myocardial abscess in an English Springer spaniel’, Journal of Veterinary Cardiology 16, 39–44. https://doi.org/10.1016/’. jvc.2013.09.002.
- Wagner, A., Macgregor, J.M., Berg, J., Sharkley, L.C. & Rush, J.E., 2006. ‘Septic pericarditis in a Yorkshire terrier’, Journal of Veterinary Emergency and Critical Care 16, 136–140. https://doi.org/10.1111/j.1476-4431.2006.00175.x.
- Weese, J.S., Dick, H., Willey, B.M., McGeer, A., Kreiswirth, B.N., Innis, B. et al., 2006. ‘Suspected transmission of methicillin-resistant Staphylococcus aureus between domestic pets and humans in veterinary clinics and in the household’, Veterinary Microbiology 115, 148–155. https://doi.org/10.1016/j.vetmic. 2006.01.004.
Источник: Journal of the South African Veterinary Association 88(0), a1496. https://doi.org/10.4102/ jsava.v88i0.1496. Licensee: AOSIS. This work is licensed under the Creative Commons Attribution License.
СВМ № 1/2018