С. Апполонова, П. Баранов, Д. Бражникова, Н. Месонжник, Г. Родченков
ФГУП «Антидопинговый центр», лаборатория конного допинга, г. Москва
В данной статье изложены основные принципы допинг-контроля в коневодстве и конном спорте, освещены технические достижения в работе по обнаружению запрещённых препаратов, отмечена важность проведения исследований метаболизма допинговых препаратов для эффективного развития контролирующих антидопинговых программ.
В статье представлены методологические основы антидопингового контроля в конных видах спорта и освещены технические достижения в обнаружении запрещённых химических соединений в физиологических жидкостях лошадей. Особое внимание уделяется значимости исследования метаболизма этой группы веществ и созданию условий эффективного развития контролирующих антидопинговых программ. В рамках проделанной работы обсуждены подходы к проведению скрининговых исследований и подтверждающих методов анализа. Основные темы, поднятые в статье: антидопинговый контроль, запрещённые препараты, время выведения лекарственного вещества из организма лошади и исследование метаболизма.
Цель статьи — подчеркнуть значимость научных исследований в области конного допинга и введения на национальном уровне обязательного мониторинга спортивных лошадей на выявление фактов злоупотребления запрещёнными веществами.
Введение
Более сорока специализированных лабораторий во всем мире занимаются проблемой выявления запрещённых допинговых средств в организме лошади. Обширный список искомых веществ и особенности физиологических жидкостей у лошадей предъявляют самые высокие требования к оснащённости лабораторий, начиная от средств подготовки биологического материала для анализа и заканчивая лабораторной компьютерной сетью, управляющей круглосуточной работой высокоточного аналитического оборудования. ФГУП «Антидопинговый центр» имеет тридцатипятилетний опыт работы в области антидопингового контроля и является ведущим центром международного уровня в России.
В 2007 году на базе ФГУП «Антидопинговый центр» была создана лаборатория конного допинга, которая успешно прошла первое профессиональное тестирование, проводимое Ассоциацией химиков-аналитиков в конном спорте – AORC (Association of Racing Chemists).
Количество образцов биологического материала, анализируемых лабораторией конного допинга, с 2007 года выросло в 7 раз, а процент положительных проб от общего количества исследуемого материала в год снизился в 5 раз. Эта статистика отражает существенный вклад лаборатории конного допинга в борьбе за предотвращение любых попыток повлиять на спортивные качества лошади или скрыть заболевания при помощи запрещённых лекарственных препаратов. Снижение процента положительных проб указывает на то, что ветеринарные врачи, тренерский персонал и владельцы стали более ответственно подходить к медикаментозному лечению спортивных лошадей и реже нарушать этические нормы.
Антидопинговый контроль
В соответствии с правилами Международной федерации конного спорта (FEI) любое назначение медицинских препаратов должно осуществляться только в целях лечения и строго по показаниям [1]. Необходимо контролировать не только показания к назначению препарата, но и полноту, и правильность выполнения всех процедур. Следовательно, лицо, проводящее лечение, несет юридическую ответственность за наличие в организме лошадей запрещённых веществ как в период подготовки, так и в ходе проведения спортивного состязания [2]. Для признания факта нарушения правил антидопингового контроля или контроля применения медицинских препаратов нет необходимости в установлении намерения, небрежности или сознательного действия ответственного лица [1].
В антидопинговом контроле к запрещённым веществам (допингу) в конных видах спорта относятся химические соединения, способные повлиять на спортивные качества или скрыть наличие заболевания у лошади. С февраля 2010 года [1] Международной федерацией конного спорта (FEI) утверждён и введён в действие список запрещённых веществ, который насчитывает 1148 химических соединений, используемых в ветеринарии [3]. К запрещённым веществам относят препараты, применяемые в гуманитарной и ветеринарной медицине, включая биологически-активные добавки, а также их метаболиты и маркеры (химические соединения или биологические параметры, свидетельствующие о применении запрещённого вещества или метода). Для некоторых химических соединений (болденон, тестостерон, диметилсульфоксид, гидрокортизон и др.) утверждены допустимые концентрации их в плазме крови или моче животного, при превышении которых контролирующие органы могут ввести санкции по отношению к хозяину лошади. В свою очередь, использование физиотерапевтических процедур (магнитных попон и накладок, лазерной терапии), акупунктуры (в том числе и лазерной) без введения в точки меридианов запрещённых веществ, а также электролитные смеси, витамины, антибиотики и антигельминтные препараты не относят к допинговым средствам [1].
В отличие от списка запрещённых веществ ВАДА (Всемирного антидопингового агентства) для атлетов, не все химические соединения, включённые в список FEI, считают допинговыми. Соединения, входящие в список запрещённых препаратов FEI для конноспортивных состязаний, делятся на «допинговые» и «контролируемые медицинские препараты» (рис. 1).
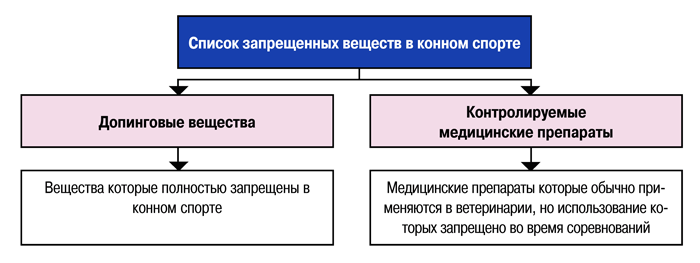 |
| Рисунок 1. Классификация списка запрещённых веществ в конных видах спорта |
Силами нашей лаборатории за четыре года было проанализировано около 1000 проб, отобранных на национальных соревнованиях РФ, в 50 из которых были найдены запрещённые вещества. Ниже приведены препараты, которыми наиболее часто злоупотребляют в нашей стране.
| 1) флюниксин | 7) кетапрофен |
| 2) кодеин/морфин | 8) кофеин |
| 3) фенилбутазон | 9) фуросемид |
| 4) ментол | 10) дипирон |
| 5) дексаметазон | 11) эфедрин |
| 6) лидокаин | 12) метенолон |
Большую часть перечисленных веществ относят к «контролируемым медицинским препаратам», которые можно применять в период между состязаниями по конным видам спорта и строго по предписанию ветеринарного врача. Более того, владелец, тренер и любое другое лицо, имеющее непосредственное отношение к лошади, должны знать время выведения того или иного химического соединения из организма животного.
Технические достижения в обнаружении допинговых средств
За последние 30 лет рост производства новых лекарственных средств значительно ускорился, но и антидопинговые технологии, позволяющие определять эти средства в биологических средах, постоянно модернизируются. Фармацевтическая промышленность выпустила на рынок большой перечень различных лекарственных препаратов с более высокой эффективностью, что позволило снизить их терапевтическую дозу. В связи с этим лаборатории, занимающиеся допинг-контролем лошадей, разработали более чувствительные методы скринингового количественного анализа биологических сред у лошади.
Интересно проследить, как для решения этой проблемы менялась технология подготовки и инструментального анализа проб биологических жидкостей лошадей. В 1980-х годах для определения запрещённых веществ у лошадей, принимающих участие в конных видах спорта, в основном применяли метод высокоэффективной жидкостной хроматографии с ультрафиолетовым методом детектирования (ВЭЖХ-УФ) с порогом чувствительности в мкг/мл (микрограмм в миллилитре), что позволяло в одном образце определять лишь десятки различных соединений. В 1990-х годах стал широко доступен метод газовой хроматографии в сочетании с детектором для проведения масс-спектрального анализа (ГХ-МС). Эта технология имеет более высокую чувствительность (до нг/мл – нанограмма в миллилитре), что позволяет в одном образце исследуемого материала проводить скрининг сотен различных химических соединений.
С 2000 года и по настоящее время метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим способом детектирования (ВЭЖХ-МС) широко применяется во время спортивных состязаний как в допинг-контроле спортсменов, так и в допинг-контроле лошадей. Развитие данного метода, прежде всего, было направлено на сокращение времени проведения анализа, автоматизацию способов подготовки анализируемого образца и на разработку методов многокомпонентного скрининга. Применение данного метода позволило решить стратегическую задачу анализа запрещённых веществ в конном допинге – определение широкого круга ксенобиотиков с помощью минимума методов за короткий промежуток времени с порогом чувствительности в пг/мл (пикограмм в миллилитре).
Таким образом, в лабораториях антидопингового контроля лошадей чувствительность тестирования за 20 лет увеличилась в миллион раз!
Научная литература по применению в последние годы ВЭЖХ-МС в области допингового контроля чрезвычайно обширна. В качестве иллюстрации позволим привести здесь лишь несколько примеров. Это многокомпонентные методы для одновременного определения анаболических стероидов, кортикостероидов, а также соединения с кислотными и основными свойствами [4–7].
Более того, применяя комплексный подход к определению допинговых веществ в биологических средах лошади с использованием таких высокочувствительных технологий, как ГХ-МС и ВЭЖХ-МС (рис. 2), удалось расширить протокол скринингового анализа до тысячи различных химических соединений.
Раньше в связи с относительно низкой чувствительностью методов исследования для проведения одного анализа приходилось использовать большой объем материала (обычно до 10 мл), что ограничивало количество тестов. С усовершенствованием технологий удалось значительно повысить уровень обнаружения допинговых веществ и уменьшить необходимый объем исследуемого образца, что особенно актуально для анализа крови. Таким образом, на сегодняшний день с помощью современных методов исследования в биологических средах лошади определяют тысячи различных допинговых веществ и их метаболитов, не требуя для проведения полного анализа большого объема мочи или крови.
 |
| Рисунок 2. Современные приборы, применяемые в антидопинговом контроле. (А) ГХ-МС; (Б) ВЭЖХ-МС |
Важность осведомлённости о метаболизме медицинского препарата для эффективного развития контролирующих программ
Для эффективного антидопингового контроля необходимо знать метаболизм лекарственных средств (ЛС), входящих в запрещённый список. Небольшое число ЛС выводится почками в неизменном виде. Чаще всего эти препараты представляют собой низкомолекулярные химические соединения или находятся в ионизированном состоянии при физиологических значениях рН. Однако большинство фармакологически активных органических соединений липофильны и не ионизируются при нормальном КЩС. Эти ЛС обычно связаны с белками плазмы, плохо фильтруются почечными клубочками и легко реабсорбируются в почечных канальцах. Метаболизм ЛС направлен на увеличение его растворимости, что способствует выведению лекарственного средства из организма с мочой. Иными словами, липофильные ЛС превращаются в легко выводимые гидрофильные (рис. 3).
В метаболизме препаратов различают две фазы:
I фаза – модификация, создающая или освобождающая функциональные группы;
II фаза – коньюгация, т.е. присоединение к ним других групп или молекул.
Метаболизм ЛС также может зависеть от пола и возраста животного. В антидопинговом контроле при доказательстве незаконного применения запрещённого вещества часто довольно эффективным оказывается определение метаболита данного ЛС. Использование данного подхода даёт нам возможность более длительного обнаружения метаболитов ЛС по сравнению с самим ЛС.
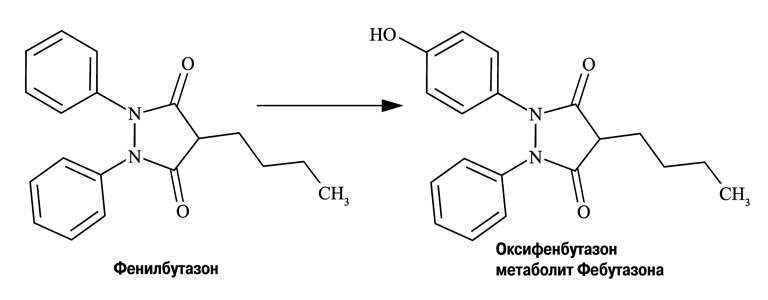 |
| Рисунок 3. Метаболизм фенилбутазона |
Наиболее удобным материалом для проведения антидопингового контроля лошадей, участвующих в конных видах спорта, считается моча. Моча как материал для исследования имеет следующие преимущества:
- забор мочи осуществляется неинвазивным способом;
- обнаружение метаболитов ЛС в моче может служить дополнительным доказательством применения лекарственного препарата;
- концентрация ЛС и/или его (их) метаболитов в моче по сравнению с содержанием в крови относительно выше.
Важно знать, какие вещества и с какой вероятностью после назначения лекарственного препарата выводятся с мочой, потому что это позволяет:
- использовать разработанный скрининг-тест для определения соответствующего вещества (веществ) или его (их) метаболитов;
- определить промежуток времени, в течение которого вещество можно обнаружить.
Без этой информации невозможно создавать скрининговые методы анализа запрещённых веществ.
Типичный процесс тестирования, проводимый антидопинговыми лабораториями
Идентификация запрещённых препаратов в организме лошади по ряду причин считается более сложной задачей, чем определение допинговых веществ в организме человека. Во-первых, это связано с тем, что в перечень запрещённых препаратов для лошади входят классы химических соединений, не относящиеся к списку запрещённых препаратов ВАДА. Это так называемые кислотно-основные соединения, прежде всего нестероидные противовоспалительные средства, барбитураты и оксикамы (релаксанты), для определения которых требуется создание новых методов с применением новейшего оборудования. Во-вторых, для подготовки исследуемого материала к анализу необходимы специальные антидопинговые технологии, обеспечивающие выделение искомых химических соединений из биологического материала. Моча лошадей содержит большое количество слизи и оксалатов. Следовательно, традиционные методы подготовки биологического материала, полученного от человека, оказываются непригодны. Не все лошади могут дать мочу в нужное время, что вызывает необходимость дополнительного забора крови, которая также требует подготовки к проведению анализа (рис. 4).
Актуальность решения этой задачи обусловлена как рядом проблем на международном уровне (российские лошади попадаются на допинг-контроле), так и неуклонным ростом популярности конных видов спорта в России. В регулярно проводимые скачки на призы Президента России, Министерства сельского хозяйства и мэра Москвы вовлечены большие деньги, и они требуют проведения допинг-контроля в соответствии с требованиями Международной федерации конного спорта (FEI).
Выявление «традиционного допинга», например анаболических стероидов, также требует иных методов, чем у спортсменов, поскольку организм лошади продуцирует болденон и нандролон, а биотрансформация стероидов тестостеронового ряда варьируется в зависимости от пола и проведенной операции (кастрации).
Антидопинговый контроль на спортивных конных состязаниях включает следующие этапы:
- отбор проб
- подготовку проб для проведения анализа
- аналитическое исследование
- интерпретацию полученных результатов анализа.
Перечисленные этапы исследования необходимо выполнять при строгом соблюдении всех правил и рекомендаций согласно ИСО/МЭК 17025, AORC и FEI.
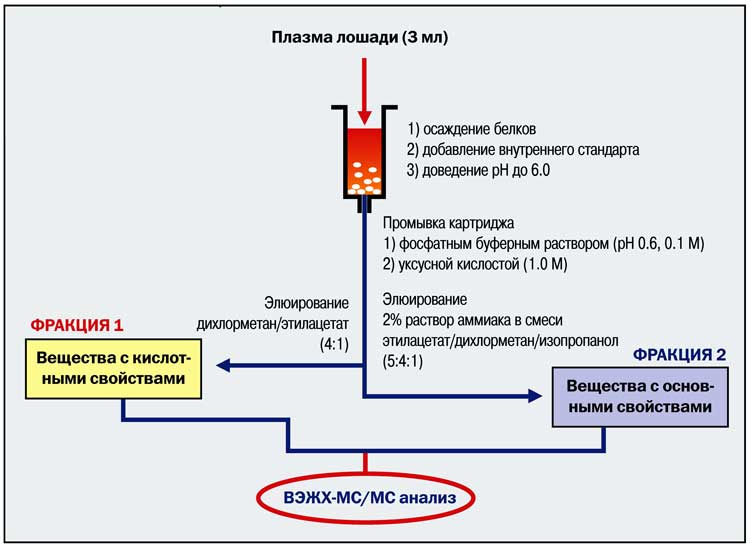 |
| Рисунок 4. Одна из схем проведения пробоподготовки образца крови лошади |
Аналитическое исследование делится на два этапа: скрининг-анализ и подтверждение. Скрининг – это быстрое определение целевых веществ в пробе. Если результат скрининга отрицательный, то дальнейшее исследование не проводят. Положительный результат требует подтверждения, после которого делается окончательный вывод.
Время выведения лекарственного препарата из организма лошади
Современное аналитическое оборудование, используемое центрами антидопингового контроля, позволяет определять запрещённые химические соединения и их метаболиты в течение недель и даже месяцев после введения препарата, когда действие активного вещества уже не влияет на результаты спортивного состязания. Чтобы избежать ложноположительных результатов, которые могут сильно испортить карьеру лошади и наездника, участвующих в конных видах спорта, для запрещённых веществ и их метаболитов были установлены концентрации, при которых они перестают оказывать действие на организм. Время достижения такой концентрации называется временем обнаружения (detection time) и является фармакологической характеристикой препарата [8]. Однако индивидуальные особенности лошади (пол, нагрузка и пр.) могут замедлить реальное снижение концентрации. В связи с этим при назначении препарата необходимо учитывать так называемое время выведения (withdrawal time), которое определяется для каждой особи ветеринарным врачом исходя из его опыта и знаний путем добавления гарантийного резервного времени к времени обнаружения (рис. 5) [9].
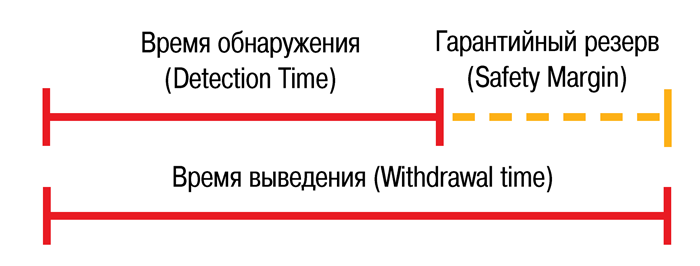 |
| Рисунок 5. Схема определения времени выведения лекарственного препарата из организма лошади |
Время обнаружения лекарственного вещества зависит от формы и природы химического соединения, а также дозы, способа и периодичности введения ЛС. Время выведения вещества зависит, помимо перечисленного, от индивидуальных особенностей животного (возраст, вес, пол, генетический фактор – порода, хроническое заболевание). При этом в расчётах учитывается допустимая погрешность [8,9]. Следовательно, время выведения лекарственного средства из организма – это фактор, позволяющий минимизировать вероятность его обнаружения.
Несмотря на то, что антидопинговые исследования по определению времени выведения лекарственных препаратов из организма проводят более 40 лет, в настоящее время статистически достоверное время выведения известно лишь для двух химических соединений [10]. При однократном введении фуросемида в дозе 150–500 мг внутривенно концентрация последнего в плазме крови через 96 часов составляет менее 100 нг/мл. При однократном введении флюниксина в дозе 250–500 мг концентрация этого вещества в моче лошади спустя 24 часа опускается ниже 50 нг/мл. На данный момент создаются многочисленные информационные базы данных по времени выведения химических соединений из организма животных. Наиболее полная и постоянно обновляющаяся информация представлена Консорциумом по применению и тестированию лекарственных средств в конных видах спорта (RMTC) [11]. В таблице 1 представлены данные FEI и RMTC по времени выведения фармакологических препаратов у лошадей при различных способах введения.
Заключение
Методологической основой определения запрещённых веществ в биологических жидкостях лошадей и спортсменов считается применение комплекса современных аналитических методов исследования, осуществляемых с помощью высокоэффективной жидкостной и газовой хроматографии в сочетании с масс-спектральными детекторами различных типов. Благодаря применению этих антидопинговых технологий удалось сократить время и объем биологического материала для проведения анализа, охватить больший перечень классов химических соединений, повысить чувствительность и достоверность результатов исследования.
Благодаря развитию ветеринарной медицины и наличию средств для осуществления допинг-контроля появилась возможность строго соблюдать регламент по применению лекарственных препаратов, ориентируясь при этом не только на личный опыт ветеринарного врача, но и на физиологические особенности лошади.
Таблица 1. Время выведения фармакологических препаратов у лошадей при различных способах введения
| НАЗВАНИЕ | ПУТЬ ВВЕДЕНИЯ | ДОЗА | ВРЕМЯ ВЫВЕДЕНИЯ |
| Азаперон | Внутримышечный | 40 мг | 36 часов |
| Альбутерол | Пероральный | 2–16 мг/32 мг | 24 часа / 5 дней |
| Альбутерол | Ингаляционный | 8,5 мг/12 мг | 48 часов / 96 часов |
| Альтреногест | Пероральный | – | До 96 часов |
| Аминокапроновая кислота | Пероральный | – | До 72 часов |
| Аминокапроновая кислота | Внутривенный | 1,25–2,5 г | 2–4 часа |
| Аминокапроновая кислота | Внутривенный | 2,5 г совместно с фуросемидом | 4 часа |
| Атропин | Местный в офтальмологии | 9 мг | 48–96 часов |
| Ацебутолол | Различные пути введения | – | До 96 часов |
| Ацепромазин | Пероральный | Менее 150 мг | 24–96 часов часа |
| Ацепромазин | Внутривенный | 40 мкг / 25–50 мг | 24 часа / 36–96 часов |
| Ацепромазин | Внутримышечный | 5–50 мг | 48 часов – 7 дней |
| Ацетаминофен | Пероральный | 10 мг | 96 часов |
| Ацетилсалициловая кислота | Пероральный | 480–960 г | 24 часа |
| Беклометазон | Различные пути введения | – | 48 часов |
| Беклометазон | Внутривенный | 500 мг | 48 часов |
| Бензокаин | Различные пути введения | – | 72 часа |
| Бетаметазон | Различные пути введения | – | 24–48 часов |
| Бетаметазон | Внутривенный | 30 мг | 24 часа |
| Бетаметазон | Внутримышечный | 3–2 мг / 12–35 мг | 24 часа / 48 часов |
| Болденон | Различные пути введения | – | До 45 дней |
| Болденон | Внутримышечный | 500 мг (однократно) | 60 дней |
| Бупивакаин | Различные пути введения | – | 48 часов |
| Буторфанол | Различные пути введения | – | 24 часа – 7 дней |
| Буторфанол | Внутривенный | 5–10 мг /
20–50 мг |
48–72 часа /
72 часа и более |
| Буторфанол | Внутримышечный | 10 мг | 96 часов |
| Гентамицина сульфат | Различные пути введения | – | 24 часа |
| Гидроксизин | Различные пути введения | – | До 96 часов |
| Гидроксизин | Пероральный | 250–500 мг | 96 часов – 5 дней |
| Гликопирролат | Различные пути введения | – | 24–96 часов |
| Гризеофиллин | Пероральный | – | 48 часов |
| Гуанабенз | Различные пути введения | – | 48 часов |
| Дантролен | Различные пути введения | – | 24–72 часа |
| Дантролен | Пероральный | 100 – 300 мг /
1 г |
72 часа /
36 часов – 3 дня |
| Дексаметазон | Различные пути введения | – | 24 часа – 6 дней |
| Дексаметазон | Пероральный | 5–20 мг | 48 часов |
| Дексаметазон | Внутривенный | 20–40 мг | 24–48 часов |
| Дексаметазон | Внутриартериальный | 40 мг | 24 часа |
| Дексаметазон | Ингаляционный | 80–220 мг | 24 часа |
| Дексаметазон | Различные пути введения
(данные FEI) |
– | 48 часов – 2 дня |
| Депомедрол | Внутримышечный | 40 мг | 48 часов |
| Дембрексин | Различные пути введения
(данные FEI) |
– | 120 часов – 5 дней |
| Детомидин | Различные пути введения | – | 24–96 часов |
| Детомидин | Внутривенный | 5–20 мг | 72 часа |
| Детомидин | Внутримышечный | 15 мг | 72 часа |
| Детомидин | Различные пути введения
(данные FEI) |
– | 48 часов – 2 дней |
| Диазепам | Различные пути введения | – | 72 часа – 7 дней |
| Диазепам | Внутривенный | 2–10 мг | 48 часов |
| Диазепам | Внутривенный | 25–50 мг | 7 дней |
| Диазепам | Внутримышечный | 2–10 мг | 48 часов |
| Диазепам | Внутримышечный | 25–50 мг | 7 дней |
| Диклофенак | Различные пути введения | – | 3–7 дней |
| Дипирон | Различные пути введения | – | 24 часа – 5 дней |
| Дипирон | Внутривенный Внутримышечный | 2,5 г / 5–10 г / 10 г и более | 72 часа / 36–120 часов / Более 5 дней |
| Дипирон | Различные пути введения (данные FEI) | – | 72 часа – 3 дня |
| Дифиллин | Различные пути введения | – | 120 часов |
| ДМСО | Различные пути введения | – | До 36 часов |
| ДМСО | Топикальный | 19,8 г / 100 г | 24 часа / 36 часов |
| ДМСО | Внутривенный | – | 24 часа |
| Зомепирак | Различные пути введения | – | 120 часов |
| Ибупрофен | Различные пути введения | – | 24–72 часа |
| Ибупрофен | Пероральный | 200–400 мг / 2–12 г | 24 часа / 48–72 часа |
| Изоксуприн | Различные пути введения | – | 24 часа – 7 дней |
| Изоксуприн | Пероральный | 3 – 300 мг / 500 мг | 24–72 часа / 7 дней |
| Изофлюпредон | Различные пути введения | – | 24–72 часа |
| Изофлюпредон | Внутримышечный | 15 – 20 мг /
40 мг |
24–48 часов /
36–72 часа |
| Изофлюпредона ацетат тетракаиновая соль | Различные пути введения | – | 96 часов |
| Изофлюпредона неомицина сульфат | Различные пути введения | – | 48 часов |
| Ипратропия бромид | Различные пути введения | – | 48 часов |
| Камбендазол | Различные пути введения | – | 72 часа |
| Кетамин | Различные пути введения | – | 120 часов |
| Кетамин | Внутривенный | 700 мг | 96 часов |
| Кетопрофен | Различные пути введения | – | 48–72 часа |
| Кетопрофен | Внутривенный | 1–1,5 г | 72 часа |
| Кетопрофен | Различные пути введения
(данные FEI) |
– | 96 часов – 4 дня |
| Кеторолак | Различные пути введения | – | 96 часов |
| Кленбутерол | Различные пути введения | – | 24 часа – 7 дней |
| Кленбутерол | Пероральный | 30–40 мг / 0,8 мг на кг / 360 мкг | 72 часа / 72 часа – 96 часов / 5 дней |
| Кленбутерол | Внутривенный | 30 мг | 72 часа |
| Кленбутерол | Различные пути введения (данные FEI) | – | 168 часов – 7 дней |
| Кромолин | Различные пути введения | – | 48 часов |
| Кромолин | Пероральный | 1 г | 48 часов |
| Кромолин | Ингаляционный | 80 мг | 24–36 часов |
| Ксилазин | Различные пути введения | – | 24–96 часов |
| Ксилазин | Внутривенный | 20 мг / 100–250 мг | 32 часа / 48 часов |
| Ксилазин | Внутримышечный | 1 г | 24 часа |
| Кутамина гидрохлорид | Различные пути введения | – | 72 часа |
| Лидокаин | Различные пути введения | – | 96 часов – 7 дней |
| Лидокаин | Топикальный | 100–150 мг / 500 мг |
24–96 часов / 36 – 120 часов |
| Лидокаин | Внутривенный | 50–200 мг | 5–7 дней |
| Лидокаин | Различные пути введения (данные FEI) | – | 48 часов – 2 дня |
| Меклофенамовая кислота | Различные пути введения | – | 48–96 часов |
| Меклофенамовая кислота | Пероральный | 1 г | 48–72 часа |
| Мепивакаин | Различные пути введения | – | 48 часов – 7 дней |
| Мепивакаин | Внутриартериальный | 60–400 мг | 48–96 часов |
| Мепивакаин | Различные пути введения
(данные FEI) |
– | 48 часов – 2 дня |
| Метилпреднизолон | Различные пути введения | – | 24 часа – 5 дней |
| Метилпреднизолон | Внутримышечный | 40–200 мг / 200 мг и более | 24–96 часов |
| Метилпреднизолон | Внутриартериальный | 40–240 мг | 48–96 часов |
| Метилэргоновин | Различные пути введения | – | 24–48 часов |
| Метилэргоновин | Внутривенный | 2–4 мг | 36–60 часов |
| Метокарбамол | Различные пути введения | – | 24–96 часов |
| Метокарбамол | Пероральный | 5 г / 7,5 г /
10 г и более |
24 часа / 72–96 часов /
5 дней |
| Метокарбамол | Внутривенный | 500 мг / 2 – 5 г | 48 часов / 48 часов |
| Набуметон | Различные пути введения | – | 120 часов |
| Налтрексон | Различные пути введения | – | 48 часов |
| Нандролон | Различные пути введения | – | 12–60 дней |
| Нандролон | Внутримышечный | 100–200 мг | 45–60 дней |
| Напроксен | Различные пути введения | – | 48–120 часов |
| Напроксен | Пероральный | 2–5 г | 96–120 часов |
| Напроксен | Внутривенный | 5 мг/кг | 96 часов |
| Омепразол | Различные пути введения | – | 24 часа |
| Омепразол | Пероральный | 2,2 г | 24 часа |
| Пентазоцин | Различные пути введения | – | До 96 часов |
| Пентазоцин | Внутримышечный | 400 мг | 72 часа |
| Пентоксифиллин | Различные пути введения | – | 72–96 часов |
| Пентоксифиллин | Пероральный | 2–4 г | 48 часов |
| Пентоксифиллин | Внутривенный | – | 72 часа |
| Пириламин | Различные пути введения | – | 24 часа – 20 дней |
| Пириламин | Пероральный | 300 мг–7,1 г | 72–96 часов |
| Пириламин | Внутривенный | 500 мг | До 72 часов |
| Пириламин | Внутримышечный | 500 мг | 36 часов |
| Преднизолон | Различные пути введения | – | 24–48 часов |
| Преднизолон | Пероральный | 125–500 мг | 48 часов |
| Преднизолон | Внутримышечный | 75–150 мг | 24–48 часов |
| Преднизолон | Внутривенный | 75–500 мг | 48 часов |
| Преднизолона натрия сукцинат | Различные пути введения | – | 48 часов |
| Преднизон | Различные пути введения | – | 24–48 часов |
| Преднизон | Пероральный | 200 мг–1 г | 24–48 часов |
| Преднизон | Внутримышечный | 100–400 мг | 24 часа |
| Прокаина гидрохлорид | Различные пути введения | – | 72 часа |
| Прокаина пенициллиновая соль | Различные пути введения | – | 24 часа – 30 дней |
| Прокаина пенициллиновая соль | Внутримышечный | 2–6 млн Ед | 10–17 дней |
| Прокаина пенициллиновая соль | Пероральный | 4 млн Ед | 60 часов |
| Прокаина пенициллиновая соль | Топикальный | 200 000 Ед | 48 часов |
| Промазин | Различные пути введения | – | До 120 часов |
| Промазин | Внутримышечный | 250–400 мг | 96 часов |
| Промазина гидрохлорид | Различные пути введения | – | 96 часов |
| Пропантелин | Различные пути введения | – | 48 часов |
| Пропиленгликоль | Различные пути введения | – | 24 часа |
| Пропионилпромазин | Различные пути введения | – | 96 часов |
| Пропранолол | Различные пути введения | – | 96 часов |
| Ранитидин | Различные пути введения | – | 24 часа |
| Ранитидин | Пероральный | 150–300 мг | 24 часа |
| Резерпин | Различные пути введения | – | 7 дней – 2 месяца |
| Резерпин | Внутримышечный | 2,5 мг | Минимум 30 дней |
| Сальметерол | Различные пути введения | – | 96 часов |
| Станозолол | Различные пути введения | – | 30–60 дней |
| Станозолол | Внутримышечный | 250–500 мг | 304-5 дней |
| Сукралфат | Пероральный | – | 24 часа |
| Сульфадиметоксин | Различные пути введения | – | 48 часов |
| Сульфаметозин | Различные пути введения | – | 48 часов |
| Теофиллин | Различные пути введения | – | 120 часов |
| Тербуталин | Различные пути введения | – | 96 часов |
| Тестостерон | Различные пути введения | – | 24 часа – 60 дней |
| Тестостерон | Внутримышечный | 75 мг–1 г | 45–60 дней |
| Тиосалициловая кислота | Внутривенный | 1 г | 30 часов |
| Тиосалициловая кислота | Внутримышечный | 1 г | 30 часов |
| Триамцинолон | Различные пути введения | – | 24–96 часов |
| Триамцинолон | Внутримышечный | 10–18 мг / 20 мг | 24 часа / 96 часов |
| Триамцинолон | Внутриартериальный | 6–18 мг | 24 часа |
| Триамцинолона ацетонид | Различные пути введения | – | 13 дней |
| Триамцинолона ацетонид | Различные пути введения
(данные FEI) |
– | 168 часов – 7 дней |
| Трибендазол | Различные пути введения | – | 72 часа |
| Триметоприм сульфадиазин | Различные пути введения | – | 48 часов |
| Трихлорметиазид | Различные пути введения | – | 24–72 часа |
| Трихлорметиазид | Пероральный | 100–200 мг / 200–400 мг | 24 часа / 48 часов |
| Трихлорметиазид | Внутримышечный | 100 мг | 36 часов |
| Фенилбутазон | Пероральный | 1–2 г | 48–72 часа |
| Фенилбутазон | Внутримышечный | До 2 г | 24–72 часа |
| Фенилбутазон | Различные пути введения
(данные FEI) |
– | 168 часов – 7 дней |
| Фенитоин | Различные пути введения | – | 96 часов – 9 дней |
| Фенитоин | Пероральный | 1 – 2,5 г | 72–96 часов |
| Фенитоин | Внутривенный | 2,8–16,3 мг/кг | 96 часов |
| Фенотерол | Различные пути введения | – | 48 часов |
| Фенспирид | Различные пути введения | – | 96 часов |
| Флюметазон | Различные пути введения | – | 24 часа |
| Флюниксин | Различные пути введения | – | 48 часов – 5 дней |
| Флюниксин | Пероральный | 500 мг | 24–48 часов |
| Флюниксин | Внутривенный | 250–500 мг | 48–72 часа |
| Флюниксин | Различные пути введения
(данные FEI) |
– | 144 часов – 6 дней |
| Флюфеназин | Различные пути введения | – | До 7 дней |
| Флюфеназин | Внутримышечный | 25–50 мг / Более 30 мг | 7 дней / Более 30 дней |
| Фуросемид | Различные пути введения | – | 48 часов |
| Фуросемид | Внутривенный | До 500 мг | Минимум 4–8 часов |
| Хлорпромазин | Различные пути введения | – | До 120 часов |
| Хлорпромазин | Внутримышечный | 100 мг | 96 часов |
| Циметидин | Различные пути введения | – | 24–48 часов |
| Циметидин | Пероральный | 400–1600 мг / 4 г | 24 часа / 48 часов |
| Эргоновин | Различные пути введения | – | 96 часов |
Список литературы
- FEI Equine Anti-Doping and Controlled Medication Regulations. 1st Edition, effective 5 April 2010.
- FEI Veterinary Regulations. 12th Edition, effective 5 April 2010.
- FEI Prohibited Substances List, effective 5th April 2010.
- N.H.Yu, E.N.M. Ho, F.P.W. Tang, T.S.M. Wan, A.S.Y. Wong. Comprehensive screening of acidic and neutral drugs in equine plasma by liquid chromatography–tandem mass spectrometry. J. Chrom. A, 1189 (2008), 426–434.
- S.M.R. Stanley, W.K. Wee, B.H. Lim, H.C. Foo. Direct-injection screening for acidic drugs in plasma and neutral drugs in equine urine by differential-gradient LC–LC coupled MS/MS. J. Chrom. B, 848 (2007), 292–302.
- E.N.M. Ho, D.K.K. Leung, T.S.M. Wan, N.H. Yu. Comprehensive screening of anabolic steroids, corticosteroids, and acidic drugs in horse urine by solid-phase extraction and liquid chromatography–mass spectrometry. J. Chrom. A, 1120 (2006), 38–53.
- G.N.W. Lung, E.W. Chung, E.N.M. Ho, W.H. Kwok, D.K.K. Leung, F.P.W. Tang, T.S.M. Wan, N.H. Yu. High-throughput screening of corticosteroids and basic drugs in horse urine by liquid chromatography-tandem mass spectrometry. J. Chrom. B, 825 (2005), 47–56.
- The AAEP’s Guidelines to Drug Detection Times, Vol. 1-3. American Association of Equine Practitioners, 2001.
- Drugs and the Performance Horse. Thomas Tobin. Springfield. 1981.
- Equine Sports Veterinary Manual. V Van Weezel Errens, Lotlorien BV. The Hague, The Netherlands, 2007.
- Racing Medication and Testing Consortium (http://www.rmtcnet.com).
Материал предоставлен Конским ветеринарным объединением
СВМ № 6/2010



