Введение
Реанимационная эндоваскулярная баллонная окклюзия аорты (РЭБОА) — это внутрисосудистое вмешательство, которое используют для контроля кровотечений. РЭБОА была впервые описана в период Корейской войны. В настоящее время эта методика снова набирает свою популярность как альтернатива экстренной торакотомии (ЭТ, торакотомии с наложением зажима на аорту) у пациентов с травмой. ЭТ ассоциирована с низким уровнем выживаемости и представляет значительные риски травматизации для персонала, который её выполняет. При том, что с помощью ЭТ можно обеспечить контроль кровотечения, торакотомия сама по себе наносит значительные повреждения пациенту и значительно увеличивает время восстановления. При применении РЭБОА поток крови в аорте можно контролировать путём введения баллонного катетера внутрь аорты, обычно через бедренную артерию. РЭБОА позволяет контролировать кровотечение посредством прерывания аортального кровотока баллоном, таким образом способствуя формированию тромба и гемодинамической стабилизации. РЭБОА также усиливает кровоток в органах, расположенных краниальнее места окклюзии, включая мозг и сердце. Разработка катетеров для РЭБОА с тонким профилем и недавние прикладные и клинические исследования позволили значительно продвинуться в её использовании. РЭБОА была прежде всего разработана для ведения пациентов с неконтролируемыми полостными кровотечениями, возникшими вследствие травмы. На сегодняшний день эта методика находит применение в других областях, таких как контроль кровотечений после родов и плановых оперативных вмешательств. Также существует нарастающий объём исследований по использованию РЭБОА в сердечно-сосудистой реанимации (СЛР). Этот обзор рассматривает применение некоторых стратегий РЭБОА (полная, периодическая и частичная окклюзия), освещает с критической точки зрения её пользу и ограничения, а также описывает возможное применение в ветеринарной медицине.
Ключевые слова: кровотечение, травма, неконтролируемые полостные кровотечения, внутрисосудистое лечение травм, шок.
Сокращения: ОПН — острая почечная недостаточность, СЛР — сердечно-лёгочная реанимация, САД — среднее артериальное давление, РЭБОА — реанимационная эндоваскулярная баллонная окклюзия аорты, ЭТ — экстренная торакотомия.
Реанимационная эндоваскулярная баллонная окклюзия аорты: применение
Описание катетеров, пригодных для РЭБОА
На сегодняшний день коммерчески доступны катетеры, которые обычно используют для РЭБОА в медицинской клинической практике. Первый — это CODA — проводниковый баллонный катетер (Cook Medical, Bloomington, IN) диаметром 12 Fr, который вводится через интродьюсер диаметром 12 Fr, с объёмом баллона 60 мл. Второй — это CODA-LP®, баллонный катетер (Cook Medical, Bloomington, IN) диаметром 9 Fr, который вводится через интродьюсер диаметром 9 Fr. Это также система с проводником, с объёмом катетера 30 мл. Третий катетер — ER-REBOA® (Prytime Medical, Boerne, TX) — катетер диаметром 7 Fr, который не требует проводника и может быть установлен через интродьюсер диаметром 7 Fr (илл. 1). Объём его баллона составляет 24 мл и имеет краниальный порт для забора образцов артериальной крови и прямого измерения кровяного давления. ER-REBOA — на сегодняшний день единственный коммерчески доступный катетер, специально разработанный для РЭБОА. Более новый катетер (pREBOA-PRO, Prytime Medical, Boerne, TX), разработанный для частичной окклюзии аорты, недавно был применён на свиньях и на момент написания статьи недоступен в продаже. Другие приспособления включают: баллонный катетер для экстренной окклюзии (Rescue Balloon Occlusion Catheter, Tokai Medical Products, Kasugai, Japan) диаметром 7 Fr, с баллоном 40 мм, RELIANT® — стент-графт баллонный катетер (диаметром 12 Fr, с баллоном 10–46 мм, Medtronic, Dublin, Ireland), окклюзионный катетер Fogarty® (диаметр интродьюсера 5 Fr, объём баллона 11 мм, Lifesciences, Irvine, CA) (илл. 1), стентграфт баллонный катетер Q50® PLUS (диаметр интродьюсера 12 Fr, баллон 10–15 мм) и окклюзионный баллонный катетер ResQ™ (диаметр 12 Fr, баллон 10–38 мм, Qx Medical, Roseville, MN). Независимо от типа катетера баллон для РЭБОА выполнен из эластичного материала и заполняется 0,9% раствором натрия хлорида.
Установка катетера для РЭБОА и выбор зоны окклюзии
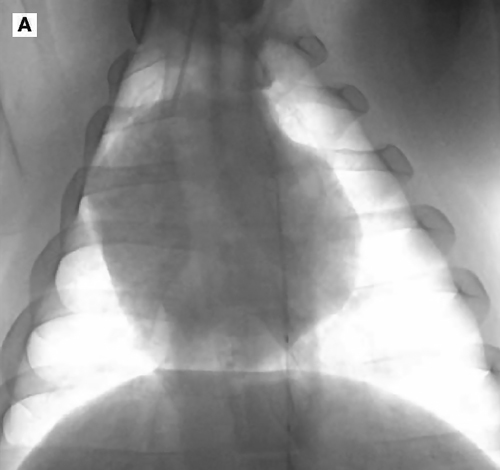
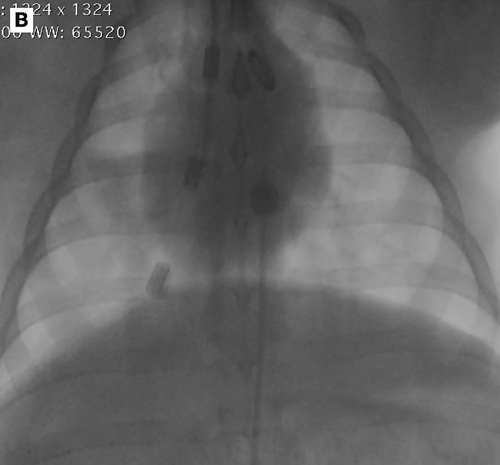
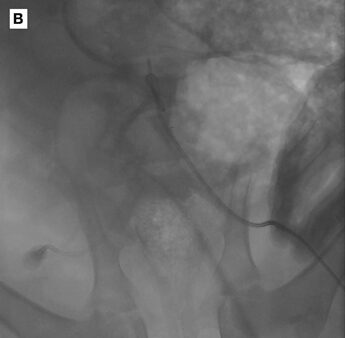
Техника РЭБОА была описана для людей и некоторых животных-моделей, на сегодняшний день нет описания клинического использования РЭБОА у собак и кошек. Изложенное ниже приведено на основании клинической практики в медицине человека. Обеспечить доступ через бедренную артерию можно с помощью пальпации пульса или используя анатомические ориентиры. Так как пациенты с выраженным геморрагическим шоком могут поступать со слабым пульсом или с отсутствием пульса, ультразвуковой контроль является популярным инструментом для корректного введения катетера у людей. Использование ультразвука позволяет дифференцировать сосуды и избежать катетеризации вены, а также оценить вызванные пункцией осложнения, такие как гематомы или расслоение стенки сосуда. Бедренную артерию можно отличить от бедренной вены с помощью ультразвука по пульсации, меньшему диаметру и устойчивости к сжатию при надавливании ультразвуковым датчиком (илл. 2). При использовании метода Сельдингера интродьюсер вводится в бедренную артерию. Баллон на кончике катетера для РЭБОА может быть расположен на разных уровнях или зонах аорты. Зона 1 охватывает сегмент аорты между левой подключичной артерией и чревным артериальным стволом, зона 2 распространяется от чревного артериального ствола до самой каудальной почечной артерии, а зона 3 расположена между каудальной почечной артерией и бифуркацией аорты. Таким образом у пациентов с глубоким геморрагическим шоком вследствие абдоминальной травмы и кровотечением в брюшной или тазовой полости, если источник кровотечения неизвестен, баллон может быть расположен в зоне 1. Если считается, что повреждение расположено ниже почки, как у пациентов с сильными переломами таза, баллон может быть расположен в зоне 3. Расположение в зоне 2 применяется редко. Правильное расположение баллона можно контролировать с помощью рентгеноскопии (илл. 3 А, В), ультразвука, рентгеновских снимков или ручной пальпации во время лапаротомии. Измерение глубины введения катетера с использованием анатомических ориентиров было описано как у людей, так и у собак, что помогает перенести методику в ветеринарную клиническую практику.
Зона установки баллона и продолжительность окклюзии
Общая допустимая продолжительность окклюзии зависит от зоны расположения баллона. Для пациентов с повреждениями, расположенными каудально от чревной артерии и краниально от почечных артерий рекомендована зона окклюзии 1; для тех, у кого повреждения каудальнее почечных артерий, можно использовать зону 3. На сегодняшний день для зоны 1 допускается окклюзия на 30–45 минут, в то время как окклюзия в зоне 3 может продолжаться до 60 минут. Применение охлаждения внешней поверхности конечностей у свиней, которым выполнили окклюзию в зоне 3 после геморрагического шока на 6 часов, снизило повреждение мышц конечностей, что видно по сниженной активности циркулирующей креатинкиназы, однако отсутствие функциональных тестов оставляет данный метод крайне противоречивым. Чтобы воспользоваться преимуществами окклюзии в зонах 1 и 3, был предложен новый алгоритм РЭБОА: у пациентов с травмой и сниженным давлением (систолическое АД менее 90 мм рт. ст.), если повреждение грудной аорты исключено (рентгенография, отсутствие жидкости в грудной полости при ультразвуковом исследовании), баллон для РЭБОА можно вводить в зону 1. Если нет эффективного ответа, экстренная лапаротомия должна быть выполнена для определения источника кровотечения. Если кровяное давление пациента повышается и есть геморрагическая жидкость в брюшной полости, лапаротомия может быть отложена, а реанимационные мероприятия (переливание продуктов крови, жидкостная терапия и/или вазопрессоры) продолжены. Пациентам, которые отвечают на окклюзию в зоне 1, при отсутствии жидкости в брюшной полости, следует сделать рентген таза. Если есть переломы таза, баллон можно переместить из зоны 1 в зону 3, чтобы снизить степень ишемии органов брюшной полости. Если переломы таза не обнаружены, вероятно, что кровотечение у пациента удалось купировать реанимационными мероприятиями и окклюзия в зоне 1 дала возможность сформироваться тромбу и стабилизировать пациента.
Наполнение баллона
После установки катетера баллон наполняют, используя 0,9% раствор натрия хлорида. Сначала баллон должен быть заполнен до полной окклюзии аорты, такая методика называется полной РЭБОА. Полную окклюзию можно подтвердить отсутствием пульсации каудальнее баллона определяемой пальпацией или прямым измерением АД через порт в бедренной артерии. Полная окклюзия аорты позволяет прекратить кровотечение, сформировать тромб, а также перенаправить кровоток в органы, расположенные краниальнее баллона (мозг и сердце). При этом полная РЭБОА сопровождается значительной ишемической нагрузкой каудальнее баллона. Современные инструкции по РЭБОА рекомендуют не превышать общего времени окклюзии в 30–45 минут в зоне 1, что соответствует данным ретроспективных исследований. Более длительное время окклюзии часто приводит к серьёзным ишемическим повреждениям.
Тактика наполнения баллона
В целях снижения ишемической нагрузки, клинические и прикладные исследования были направлены на изучение частичной РЭБОА. После непродолжительного периода полной РЭБОА (около 10–15 минут), баллон спускается до появления кровотока небольшого объёма вокруг катетера, чтобы обеспечить поступление кислорода к тканям, расположенным каудальнее баллона, и снизить ишемическую и реперфузионную нагрузку, наблюдаемую до и после спускания баллона. В соответствии с настоящей официальной позицией, термин «частичная РЭБОА» следует использовать «для описания методики частичного наполнения баллона катетера для спасения физиологически нестабильного пациента, с двойной целью: минимизировать нисходящее ишемическое повреждение и контролировать кровотечение» (Williams TK, Neff LP, Horer TM, Moore LJ, Brenner ML, DuBose JJ, et al. «What’s in a Name?» A consensus proposal for a common nomenclature in the endovascular resuscitative management and REBOA Literature. J Endovasc Resusc Trauma Manag. 2017, 1:9–12). На сегодняшний день не существует катетеров с возможностью измерения кровотока, а большинство методов основано на пальпации пульса или на оценке артериального давления краниально и каудально от баллона. При частичной окклюзии баллон для РЭБОА спускают до тех пор, пока не появится пульс каудальнее баллона или сигнал кровотока в каудальных отделах аорты. Точное титрование аортального потока необходимо для поддержания каудальной перфузии под контролем риска остановки сердца и дыхания. Исследования на свиньях показали, что повышение каудального САД на 10 мм рт. ст. выше его показателя при полной окклюзии соответствует кровотоку в аорте, равному 250–500 мл/мин., в зависимости от тяжести шока. К примеру, если каудальное САД во время полной окклюзии было 15 мм рт. ст., следует спустить баллон и восстановить аортальный кровоток до того момента, пока каудальное САД не достигнет 25 мм рт. ст. Другие исследования рекомендуют титровать аортальный кровоток на основании краниального систолического давления или измерения диаметра аорты. Использование высокоточных шприцев (Encore 26 Advantage Kit, Boston Scientific Corporation, Marlborough, MA) может быть полезным при титровании кровотока. Идёт процесс разработки программного обеспечения, способного точно изменять объём баллона (по шкале микролитров каждые несколько секунд) для контроля кровотока в аорте, а также краниального и каудального САД. Такая динамическая автоматизированная и точно контролирующая эндоваскулярный аортальный баллон программа называется эндоваскулярным вариабельным аортальным контролем (EVAC).
Альтернативой частичной РЭБОА является периодическое полное спускание баллона с последующим его наполнением, что даёт короткий период перфузии; такая тактика называется периодической РЭБОА. Периодическая РЭБОА была описана у свиней и может быть выполнена с учётом САД или времени окклюзии. При протоколе, ориентированном на время окклюзии, баллон спускают в заданные промежутки времени и снова наполняют. При протоколе, основанном на САД наполнение баллона происходит, когда САД падает ниже 30–20 мм рт. ст. Этот подход ещё не был сравнен в исследованиях с техникой частичной РЭБОА, и пока недостаточно данных клинических исследований для понимания того, как много дополнительного времени даёт периодическая РЭБОА.
Реанимация и контроль источника кровотечения
Введение катетера для РЭБОА — это дополнительное вмешательство, которое позволяет контролировать геморрагический шок. Как только кровотечение купировано с помощью наполнения баллона и пациент стабилизирован, могут быть предприняты последующие реанимационные мероприятия, такие как введение продуктов крови, кристаллоидов и применение вазопрессоров. С помощью методов визуальной диагностики следует оценить масштабы повреждений в брюшной полости. Также возможно введение контраста через катетер для РЭБОА для визуализации повреждений с помощью компьютерной томографии. Более того, экстренная диагностическая лапаротомия или эндоваскулярные вмешательства могут потребоваться для последующего контроля кровотечения.
Спускание баллона и продолжение реанимации
После начала инфузионной поддержки и окончательного купирования кровотечения с помощью хирургии или интервенционной рентгенографии эндоваскулярный аортальный баллон можно спустить. Это сопровождается значительным реперфузионным повреждением. Спускание баллона при этом тщательно контролируется для предотвращения остановки сердца и дыхания. Баллон обычно спускают постепенно за 10 минут, при этом время спускания должно соответствовать времени окклюзии. Более быстрое спускание лучше переносится при непродолжительной окклюзии. Ручное спускание баллона может привести к непредсказуемым изменениям аортального кровотока и САД. В одном исследовании на свиньях удаление 0,5 мл 0,9% натрия хлорида из баллона катетера для РЭБОА каждые 30 сек. стало причиной широкого спектра изменений в аортальном кровотоке и САД. Более того, восстановление первоначального аортального кровотока было непредсказуемым. Снижение артериального давления при спускании баллона является распространённой проблемой в прикладных научных исследованиях и клинической практике у людей. Баллон может быть постепенно спущен в контролируемой динамической технике для предупреждения индуцированной реперфузией гипотонии. Этот новый подход назван эндоваскулярным усилением перфузии для интенсивной терапии (EPACC). При EPACC баллон медленно спускают с помощью программы. Когда пациент становится гипотоничен (обычно с САР <65 мм рт. ст.), баллон снова наполняют, пока краниальное САД не достигнет предустановленной отметки (обычно 65 мм рт. ст.). Пациенты могут получать инфузионную поддержку и вазопрессоры в сочетании с повышением краниального САД с помощью наполнения баллона. Автоматизированное программное обеспечение ежеминутно делает изменения в объёме катетера и контролирует кровяное давление в предустановленном промежутке. При сравнении с полной РЭБОА частичная РЭБОА и EVAC сопровождаются меньшей ишемической и реперфузионной нагрузкой на момент спускания баллона, что видно по сниженной концентрации лактата в плазме крови, а также по более низкой потребности в изотонических кристаллоидах и вазопрессорах.
Дополнительные сложности РЭБОА
Осложнения, сопровождающие использование катетеров для РЭБОА, связаны либо с техникой выполнения окклюзии, либо с ишемическим и реперфузионным повреждением (таблица 1).
Таблица 1. Технические и метаболические осложнения, связанные с реанимационной эндоваскулярной баллонной окклюзией аорты (РЭБОА)
| Тест | Технические осложнения | Метаболические осложнения |
| Осложнения, связанные с установкой интродьюсера | Установка в другой сосуд
Повреждение сосуда Воздушная эмболия Дистальная ишемия Кровотечение Тромбоз |
Острое повреждение почек
Печеночная недостаточность Инфаркт спинного мозга Ишемия кишечника Некроз мышц Потеря конечности Гиперкалиемия |
| Неправильное расположение баллона | Неверное место наполнения баллона:
• Кровотечение не остановлено • Повреждение артерии при наполнении баллона в мелкой артерии (чревной, почечной, брыжеечной) |
Метаболический ацидоз
Тромбоз Гипотензия Повреждение миокарда Продолжающееся кровотечение после наполнения баллона Смерть |
| Перенаполнение баллона | Смещение баллона
Разрыв баллона Расслоение стенки сосуда |
|
| Осложнения при удалении интродьюсера | Разрыв сосуда
Кровотечение Ишемия конечностей Вазоспазм |
Технические сложности
Появление катетеров с маленьким диаметром повысило безопасность РЭБОА. Использование более мелких катетеров, вводимых через интродьюсеры толщиной 7 Fr вместо 11–12 Fr, требует меньшего объёма сосудистого доступа, снижает вероятность эмболии дистальных отделов конечностей и уровень смертности. Интродьюсер может быть случайно установлен в бедренную вену вместо бедренной артерии. Правильное место установки можно определить после дифференциации бедренной вены от бедренной артерии (размер, анатомические ориентиры, пульс, податливость сжатию (илл. 2), прямого измерения давления через интродьюсер и анализа газов крови, полученной из интродьюсера. Введение катетера для РЭБОА может осложняться повреждением сосуда и образованием гематом во время введения или в момент извлечения интродьюсера. Баллон катетера даже при правильной установке катетера может смещаться.
Метаболические осложнения
Список распространённых метаболических осложнений РЭБОА представлен в таблице 1. Пациенты с травмой поступают с повреждениями тканей различного генеза. Эти повреждения тканей могут осложняться ишемией от геморрагического шока и значительным ишемическим и реперфузионным повреждением при использовании РЭБОА. Ишемические и реперфузионные повреждения часто встречаются на животных моделях при РЭБОА, данных о патогенезе этих повреждений недостаточно. Обычно маркеры ишемического и реперфузионного повреждения включают рН плазмы крови и избыток оснований, наряду с концентрацией лактата в плазме и концентрацией калия. Эти наблюдения были подтверждены интраперитонеальным микродиализом с измерением концентраций лактата и пирувата.
Часто сообщается о повреждениях почек, печени, желудочно-кишечного тракта и спинного мозга. У пациентов с неконтролируемым полостным кровотечением, которым была выполнена РЭБОА, есть риск острого повреждения почек. Острое повреждение почек в таком случае, по всей видимости, носит многофакторный характер. В соответствии с недавним систематическим исследованием, сообщается о повреждении почек в 3/3 исследований по травме у людей при РЭБОА. Интересно отметить, что только в 1/3 из этих исследований использовалась окклюзия в зоне 1 (в 1/3 исследований не сообщалось о зоне окклюзии), это значит, что даже аортальная окклюзия ниже почечной артерии ассоциирована с острым повреждением почек. Подобные наблюдения часто упоминаются и в исследованиях у животных. Гиперкалиемия также часто наблюдается после РЭБОА, она, скорее всего, является результатом выхода калия из повреждённых клеток при сниженной почечной экскреции. После реперфузии важны аккуратный мониторинг электролитов, особенно концентраций калия и кальция, и правильное лечение нарушений их баланса.
Высокое артериальное давление краниальнее от точки окклюзии во время РЭБОА вызвало беспокойство относительно повреждения органов, расположенных краниальнее баллона. Использование РЭБОА противопоказано у пациентов с кровотечением краниальнее левой подключичной артерии из-за риска усиления кровотечения в краниальной части грудной клетки. Сообщается о повреждении миокарда, сопровождающем РЭБОА. Это связывают с увеличением постнагрузки, которое приводит к увеличению степени растяжения миокарда в комплексе с реперфузионным повреждением, сопровождающим окклюзию аорты. Различные модели у свиней с геморрагическим шоком показали повышение уровней циркулирующего тропонина наряду с гистопатологическими признаками повреждения миокарда.
Более ранние клинические данные вызвали опасения по поводу возникновения внутричерепного кровотечения у пациентов с неконтролируемым полостным кровотечением и травматическим повреждением головного мозга из-за повышения артериального давления. Однако прикладные исследования показали, что РЭБОА, особенно стратегии частичной РЭБОА, не усиливает внутричерепное кровотечение при травматическом повреждении головного мозга, однако требуются более крупные обсервационные исследования у людей.
Современные показания к РЭБОА
Неконтролируемое полостное кровотечение
Неконтролируемое полостное кровотечение на сегодняшний день является наиболее распространённым показанием к РЭБОА. Термин «неконтролируемое полостное кровотечение» долгое время использовался в литературе для обозначения кровотечения в такой локации, где невозможно найти точку компрессии для контроля кровотечения. В соответствии с более свежим определением, неконтролируемое полостное кровотечение определяется у пациентов с одним или несколькими повреждениями из описанных ниже: травма грудной клетки, повреждение паренхиматозных органов (печень, почки, или селезёнка), повреждение крупных сосудов туловища или перелом таза с разрывом кольца. В дополнение эти пациенты должны иметь признаки геморрагического шока (систолическое артериальное давление менее 90 мм рт. ст.) или нуждаться в экстренной операции. Установленное определение неконтролируемого полостного кровотечения позволило повысить уровень доказательности за счёт включения в исследования гомогенной популяции пациентов в сходном состоянии. В частности, это определение позволило отделить пациентов с неконтролируемым полостным кровотечением от пациентов с множественными повреждениями туловища, которые представляют собой популяцию с риском развития неконтролируемого полостного кровотечения, без геморрагического шока.
Большинство оригинальных данных о РЭБОА взяты из военных исследований. Данные из Объединённого штаба по регистрации травм показали, что 68% ранений, полученных на поле боя, были проникающими, у мирного населения они встречаются реже (11%). Новое индивидуальное защитное обмундирование для военных, наряду с новыми протоколами догоспитальной помощи и улучшением помощи в пути от места получения ранения до медицинского учреждения позволили снизить смертность и инвалидизацию при ранениях на поле боя. Также более широкое использование кровоостанавливающих жгутов и гемостатических материалов привело к снижению количества смертей из-за кровотечений конечностей, а использование бронежилетов улучшило защиту грудной клетки бойцов. Таким образом абдоминальные кровотечения и кровотечения в местах сочленения конечностей и туловища остались основными причинами смертности и инвалидизации. Современные исследования разделяют пациентов с летальным исходом на: имевших шансы на выживание, потенциально имевших шансы на выживание или летальный исход, который можно было предотвратить. Эти исследования позволили возобновить работу в области лечения неконтролируемых полостных кровотечений. Обзор случаев смерти в отрядах специального назначения между 2001 и 2004 годом показал, что из 82 смертей 15% (12/82) имели повреждения, с которыми люди потенциально могли выжить. Неконтролируемые полостные кровотечения были причиной смерти у 50% таких пациентов. Похожие результаты показали, что неконтролируемые полостные кровотечения — это причина значительного количества смертей, которые были предотвратимы в других выборках. Неконтролируемые полостные кровотечения также представляют значительную проблему у мирного населения, особенно во время природных или техногенных катастроф. Исследование, проведённое на основании материалов Национального банка данных по травмам, включало 1,8 миллиона пациентов между 2007 и 2009 годом, показало, что из 249505 пациентов с кровотечениями из крупных сосудов туловища 20414 (8,2%) имели неконтролируемые полостные кровотечения, с уровнем смертности 7 и 45% соответственно.
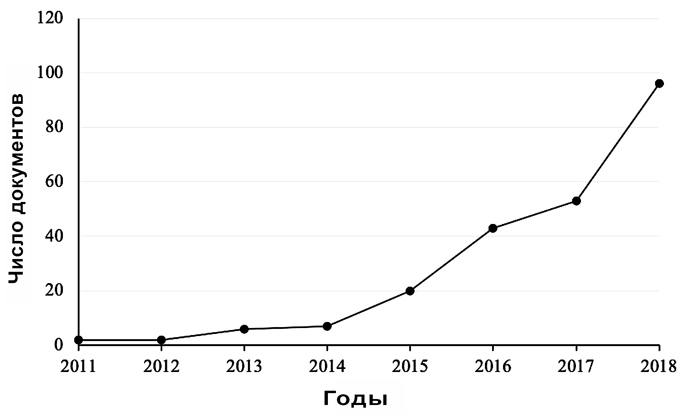
За последние годы произошёл всплеск количества публикаций, связанных с РЭБОА, ввиду её потенциальной пользы как минимально инвазивной помощи при неконтролируемых полостных кровотечениях (илл. 4). Недавно разработанный катетер для РЭБОА с диаметром 7 Fr (ER-REBOA®, Prytime Medical, Boerne, TX), возможно, тоже вызвал растущий интерес к РЭБОА, так как доступ толщиной 7 Fr не требует ушивания стенки артерии у людей. РЭБОА является более безопасной для медицинского персонала, чем экстренная торакотомия, и применение РЭБОА становится всё шире во внегоспитальных условиях. РЭБОА сейчас используется в полевых условиях, как у мирного населения, так и у военных.
Расширенное использование РЭБОА
Интраоперационное применение, не связанное с лечением травмы
РЭБОА была использована в качестве вспомогательного средства при многих хирургических процедурах, сопровождающихся большой кровопотерей, не связанных с лечением травм, например: контроль гемостаза у пациентов с обширным кишечным кровотечением, разрывом аневризмы брюшной аорты или у пациентов при удалении множественных опухолей. РЭБОА также применялась у женщин с патологиями плаценты, с риском угрожающего жизни кровотечения. В описании одного клинического случая РЭБОА позволила контролировать кровотечение и провести кесарево сечение и гистерэктомию у представительницы свидетелей Иеговы с вросшей плацентой — процедура, обычно летальная в этой популяции пациентов. Подобное интраоперационное использование может быть потенциально применимо в ветеринарной практике при соответствующих размерах пациента.
Сердечно-лёгочная реанимация
Катетер для РЭБОА может быть установлен пациентам с травматической и нетравматической остановкой сердца и дыхания. Окклюзия аорты в ходе СЛР позволяет повысить перфузию миокарда и головного мозга. Исследование на свиньях при нетравматической остановке сердца и дыхания показало, что окклюзия аорты на уровне диафрагмы привела к повышению среднего и диастолического артериального давления и последующему повышению давления в коронарных артериях. Более того, окклюзия аорты также улучшила показатели ишемического повреждения (более высокий рН и более низкая концентрация лактата в сыворотке крови) по сравнению с группой контроля и группой, в которой окклюзия была выполнена на уровне сердца. Похожие исследования у животных показали повышение давления перфузии миокарда при использовании РЭБОА во время сердечно-лёгочной реанимации. Повышение артериального давления при баллонной окклюзии аорты также было описано у людей при СЛР. Одно из исследований по использованию внутриаортального введения вазопрессина в комбинации с баллонной окклюзией аорты показало, что в дополнение к повышению давления перфузии данный подход может оказывать положительное влияние на кровоток в головном мозге до восстановления нормальной циркуляции крови. Норадреналин не оказал значительного положительного влияния на давление перфузии головного мозга при введении подобным образом. Исследование по выживаемости у свиней показало, что внутриаортальное введение адреналина в комбинации с баллонной окклюзией аорты не улучшает прогноз.
Будущее РЭБОА в ветеринарной медицине
Размер катетера
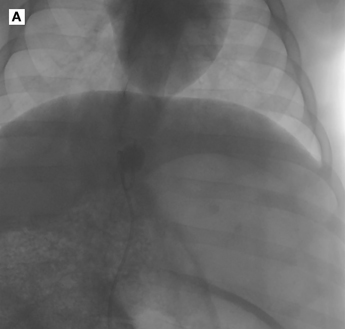
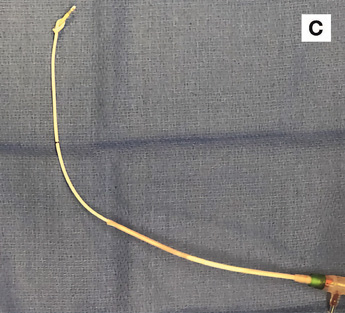
Помимо стоимости, возможность применения катетеров для ветеринарных пациентов является значительным ограничением для адаптации РЭБОА в клиническую ветеринарную практику. Инструкции для ветеринарной медицины отсутствуют, а использование доступных на сегодняшний день специализированных катетеров для РЭБОА возможно лишь у собак средних и крупных пород. Подобная проблема существует и в педиатрии человека. Из-за размеров сосудов дети до 8 лет слишком малы, чтобы использовать для них катетер с интродьюсером диаметром 7 Fr. Катетеры, разработанные не для РЭБОА, использовались у свиней, которые сходны по размерам с детьми (илл. 3В, данные не опубликованы), но эти катетеры недостаточно жёсткие, и баллон иногда может смещаться (илл. 5А) или завязываться в узел (илл. 5 В, С).
Вклад экспериментальной медицины
Значительное количество литературы о РЭБОА было получено на основании исследований на животных. При этом свиньи были использованы чаще всего. Существует также несколько исследований об использовании РЭБОА на овцах, однако они встречаются не так часто. Важно отметить, что собаки также были использованы в качестве модели для РЭБОА, особенно в случаях с СЛР, что даёт возможность внедрить этот метод в ветеринарную практику. РЭБОА была использована у собак с нетравматическим геморрагическим шоком. После 34 минут кровотечения и с САД около 50 мм рт. ст. животные, которых лечили с помощью окклюзии аорты и болюсного введения гипертонического натрия хлорида или натрия ацетата, показали улучшение сердечно-сосудистой функции по сравнению с теми, которым выполнили аортальную окклюзию и вводили изотонический раствор натрия хлорида, с переменными увеличениями показателей сердечной функции (сердечный индекс, систолический индекс и давление наполнения сердца). Остальная литература по собакам об эндоваскулярной баллонной окклюзии основана на исследованиях СЛР. В исследовании у собак с остановкой сердца и дыхания, индуцированной фибрилляцией желудочков, окклюзия в зоне 1 привела к повышению давления перфузии миокарда и чаще сопровождалась восстановлением циркуляции. В этом исследовании баллон был наполнен через 3 минуты после начала СЛР и спущен через 2 минуты у тех животных, которые показали восстановление спонтанного кровообращения хотя бы на 6 минут. В исследованиях при СЛР с открытой грудной клеткой у собак, которым выполнили эндоваскулярную баллонную окклюзию аорты, кровоток в миокарде и головном мозге был лучше, по сравнению с контрольной группой. Использование эндоваскулярной окклюзии аорты при остановке сердца и дыхания привело к усилению кровотока в дуге аорты, при этом препараты для реанимации, включая растворы, вводились через аортальный баллонный катетер. Исследования у собак установили положительное влияние перфузии дуги аорты на давление перфузии миокарда и остановку сердца и дыхания, индуцированную фибрилляцией желудочков.
Клиническое использование в ветеринарной медицине
РЭБОА может быть применима в ветеринарной медицине, особенно если будут разработаны доступные катетеры маленького диаметра. Одно из исследований показало, что баллон катетера для РЭБОА был успешно установлен у 15/15 трупов собак, при этом в качестве внешнего ориентира использовали 12-й грудной позвонок. В этом исследовании использовали катетер для РЭБОА с интродьюсером диаметром 7 Fr. Доступ через бедренную артерию был достигнут путём разреза или с помощью ультразвукового контроля. Катетер был установлен собакам с весом от 10 до 48 кг. Баллон был заполнен из расчёта в среднем 0,4 мл/кг (интервал 0,21–0,67) раствора йогексола. Мы хотели бы предостеречь практикующих врачей, что не стоит ориентироваться на общий объём баллона при его наполнении для окклюзии, чрезмерное наполнение баллона представляет значительную проблему при данной процедуре. Осложнения (продольный дефект и локальное расслоение) наблюдались у двух из пяти трупов, которые были вскрыты.
Мы использовали окклюзионный катетер Fogarty® у поросят с весом 20–30 кг (неопубликованные данные). При том, что нам удалось выполнить полную окклюзию аорты при геморрагическом шоке, нередко наблюдалось каудальное смещение баллона (илл. 5А). Кончики некоторых катетеров в нашем исследовании завязались в узел (илл. 5 В, С). Такие катетеры вводятся без проводника и не могут быть достаточно жёсткими, чтобы выдержать повышенные значения САД.
Существует множество применений для РЭБОА у ветеринарных пациентов, при условии, что есть катетер, который можно безопасно вводить маленьким пациентам. Кроме травматического геморрагического шока, РЭБОА может быть применена в нескольких сценариях у ветеринарных пациентов, к примеру: нестабильные пациенты с нетравматическим гемоперитонеумом, удаление нескольких опухолей, реанимация при интраоперативном ятрогенном повреждении. Как пример, мы наблюдали ятрогенный разрыв аорты при фенестрации межпозвоночных дисков, окклюзия аорты в данном случае могла бы облегчить стабилизацию пациента и восстановление аорты.
Так как ведение пациентов при РЭБОА требует особого внимания во время и после процедуры, требуется соответствующее обучение персонала. Так же как в медицине человека, ветеринарные специалисты учатся выполнять сложный сосудистый доступ и работать с осложнениями при эндоваскулярных вмешательствах. У людей курс основных эндоваскулярных навыков при травме от Американского хирургического колледжа даёт основополагающую информацию по безопасному применению РЭБОА. Циклы наполнения/спускания баллона могут быть выполнены с помощью программного обеспечения, специально разработанного с учётом патофизиологических особенностей ветеринарных пациентов, которым показана РЭБОА. Клиницисты должны иметь в виду осложнения, возникающие после удаления интродьюсера (обширное кровотечение, вазоспазм или тромбоз, ведущий к ишемии). Восстановление артериальной стенки — это редкая процедура у ветеринарных специалистов, она требует специализированной подготовки. Истинные показания для установки катетера для РЭБОА обсуждаются в литературе по травмам. Необходимо адекватно выбирать пациентов, привлекать обученный персонал и обеспечивать подходящие условия.
Реанимационная эндоваскулярная баллонная окклюзия аорты: заключение
Методика РЭБОА претерпела значительные усовершенствования, по большей части касающиеся снижения степени ишемического и перфузионного повреждения. Исследования у животных при травме и нетравматических патологиях дали ценную информацию об этой развивающейся методике, получающей всё более широкое применение. Несмотря на отсутствие на сегодняшний день опубликованных исследований по клиническому применению данного метода у домашних любимцев, РЭБОА может быть применена в ветеринарной практике. Обучение всем этапам процедуры и мультидисциплинарный подход, включая реанимацию, интенсивную терапию, анестезию и хирургию, способны улучшить исход для пациента.
Вклад авторов. GH, ET, CB, MS и ED выполнили обзор литературы, GH и ET составили рукопись. CB, MS, ED, EF, LN, JG, IS, TW и MJ редактировали рукопись. ET, CB, MS, ED, EF, LN, JG, IS, TW и MJ предоставили детальную информацию о применении РЭБОА у человека и свиней.
Финансовая поддержка. Данная работа выполнена при поддержке Аппарата помощника министра обороны по вопросам здоровья через Военную программу медицинских исследований и развития, по решению № W81XWH-16–2–0043.
Благодарности. Авторы хотели бы поблагодарить Capt. K. Yamashiro, медицинского доктора, специалиста в области рентгеноскопии у молодняка свиней.
Предупреждение. Взгляды, представленные в этой статье, принадлежат авторам и не отражают официальной позиции или политики правительства США, Министерства обороны, Фонда развития военной медицины имени Генри М. Джексона или Департамента ВВС. Мнения, интерпретации, выводы и рекомендации принадлежат авторам и не обязательно поддерживаются Министерством обороны. Ультразвуковые и рентгеноскопические снимки животных были сделаны, обработаны и использованы в публикации в соответствии с актом о благополучии лабораторных животных 1966 года с обновлениями и Руководством по содержанию и использованию лабораторных животных Национального совета по научным исследованиям. Работа была выполнена как клиническое исследование, одобренное Начальником медицинской службы ВВС США под номером FDG20180024A и FDG20180028A. Эта рукопись представляет собой часть работы для Программы постдипломного участия в научных исследованиях в Медицинском центре Дэвида Гранта ВВС США, База для клинических исследований под патронажем Окриджского института науки и образования по межведомственному соглашению между Департаментом энергетики США и Медицинского центра Дэвида Гранта ВВС США.
Комментарий о конфликте интересов: MJ, LN и TW — основатели Certus Critical Care, Inc. — организации, которая занимается разработкой катетеров для РЭБОА. Упомянутые выше авторы заявляют, что исследование было выполнено в отсутствие каких-либо коммерческих или финансовых взаимоотношений, которые могли быть истолкованы как потенциальный конфликт интересов.
Источник: Emergency and Critical Care. Journal Frontiers in Veterinary Science 6:197. Copyright © 2019 Hoareau, Tibbits, Beyer, Simon, DeSoucy, Faulconer, Neff, Grayson, Stewart, Williams and Johnson. This is an open-access article distributed under the terms of the Creative Commons Attribution License (CC BY). Печатается без списка литературы.
СВМ № 5/2021
Вам также могут быть интересны статьи:
EVECCS. Прогноз ответа на инфузионную терапию: тест с пассивным подъёмом ног (ТППН)
Прогностическая значимость нарушения функции внутренних органов у кошек с политравмой