От редакции
Когда в рамках MVC-2015 был заявлен мастер-класс «Эфферентный метод терапии в ветеринарии. Плазмаферез и плазмасорбция», на него записался один (!) ветеринарный врач. Что характерно, это был представитель региональной клиники, оценивший возможность применения безаппаратных систем (приобретение аппарата только планировалось). Конечно, в таких крупных городах, как Москва, Санкт-Петербург и другие, экстракорпоральные методы лечения давно использовались в ряде ветеринарных клиник. На Осенней ветеринарной конференции в 2014 году производители специально предлагали слушателям лекций по нефрологии аппаратуру и диализные колонки, адаптированные к размерам домашних любимцев. Но в целом информированность об этой области ветеринарной практики невысока, поэтому мы рады представить вам две статьи — два нескучных и понятных рассказа о различных методах экстракорпоральной терапии. Гемодиализ
Экспериментальный гемодиализ (ГД) у собаки был выполнен в 1913 году. [1, с. 650]. В 1990 году было сформировано первое в мире диализное отделение для домашних животных в Калифорнийском университете в Дэвисе. Сейчас ветеринарные диализные службы есть в США, Канаде, Англии, Италии, Португалии, Германии, Индии, Корее, Австралии, Японии, Таиланде и ряде других стран. Экстракорпоральные (ЭК) методы лечения пока не нашли широкого применения в отечественной ветеринарии. Обнадёживает, что интерес к ним значительно возрос за последние годы. Эта статья для врачей, которые хотят разобраться, когда рационально применять ЭК способы лечения в своей практике. Чтобы понимать, какой метод ЭК лечения подойдёт пациенту в конкретной клинической ситуации, нужно знать, каков физический смысл его действия. ЭК технологии создавались для разных целей и обладают, соответственно, различными возможностями и ограничениями.
Термин «экстракорпоральная терапия» говорит о том, что мы «берём» кровь и что-то с ней делаем вне тела пациента. На современном этапе развития ЭК процедур кровь забирается из организма при помощи специальных аппаратов. Она проходит через фильтр, благодаря которому очищается от ненужных компонентов. Все экстракорпоральные методы можно представить себе на основе этой общей схемы (илл. 1), но сходство между ними на этом и заканчивается. В фильтрах могут быть использованы очень разные по свойствам материалы и физико-химические процессы.
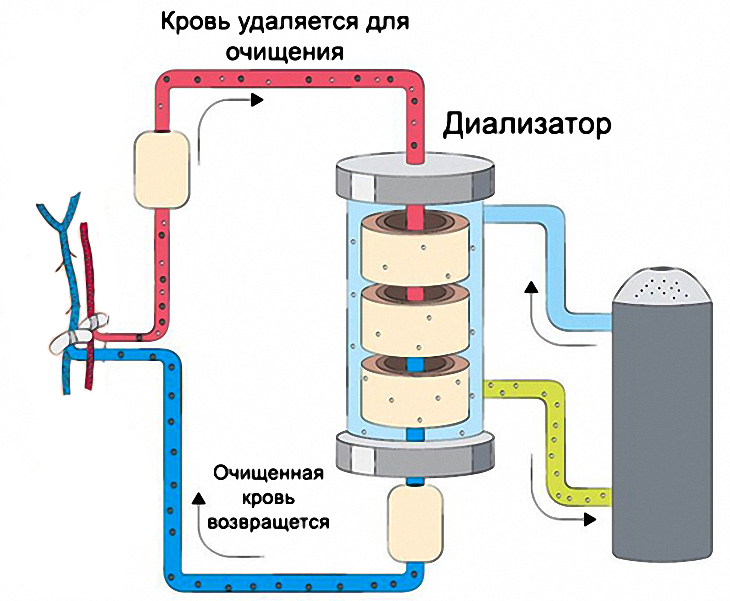 |
| Илл. 1 |
Диализные процедуры
Словом «диализ» называют целую группу методов, основанных на использовании мембранных диализаторов.
Гемодиализ наиболее эффективен для удаления некрупных водорастворимых молекул. Чтобы понять, почему это именно так, обратимся к физическим основам метода.
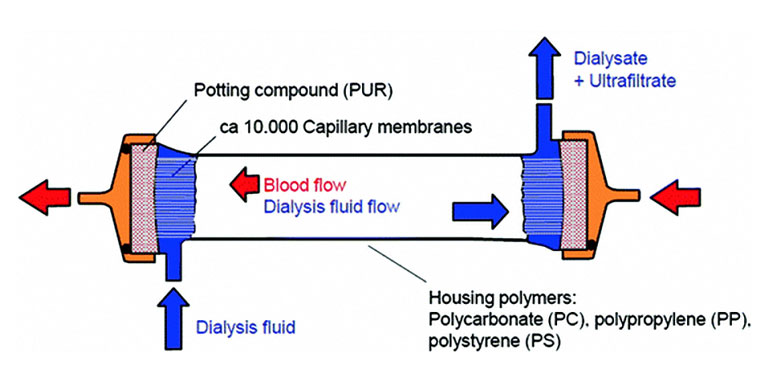
В фильтрах для гемодиализа, диализаторах, находится синтетическая пористая мембрана. Она организована в виде множества микротрубочек. Внутри этих полых волокон протекает кровь пациента. Таким образом, кровь всё время остаётся в замкнутом объёме экстракорпорального контура. С наружной стороны капилляры мембраны омываются постоянно обновляющимся диализирующим раствором (илл. 2). Диализирующий раствор — это сложный раствор электролитов с буфером, иногда с глюкозой, в воде высокой степени очистки. Его состав подбирается исходя из нужд конкретного пациента.
Первый ключевой момент для диализных процедур таков, что кровь и раствор разделены полупроницаемой мембраной. Они нигде не смешиваются и обмениваются компонентами только через неё. В связи с этим возможности диализного фильтра очистить кровь от тех или иных веществ во многом зависят от свойств мембраны, в первую очередь от размеров и числа пор в ней.
Вторая важная характеристика диализных процессов — протекание в водной среде, как и всех процессов в живых организмах.
Третий фактор, влияющий на возможность удаления вещества диализом, — это свойства самих удаляемых молекул: размер, гидрофильность, связь с белками крови.
Свойства молекул также влияют на объём их распределения, то есть способность проникать в различные жидкостные компартменты тела. Для ряда мелких молекул (например, мочевина, этанол) при экстракорпоральных методах лечения даже клеточная мембрана не является преградой, и они равномерно распределяются во всей воде тела, в том числе и во внутриклеточной. Другие мелкие и средние молекулы свободно проходят в интерстиций, они содержатся во всей внеклеточной жидкости, а не только в крови. Объём внутриклеточной и интерстициальной воды тела примерно в одиннадцать раз больше объёма жидкой части внутрисосудистого содержимого. Поэтому при проведении диализных процедур не совсем верно говорить об «очищении крови». Конечно, кровь — это та среда, с которой мы можем непосредственно взаимодействовать в отличие от внутриклеточного объёма, но, когда мы имеем дело с мелкими молекулами, наша основная задача — опосредованно через кровь очистить «воду тела».
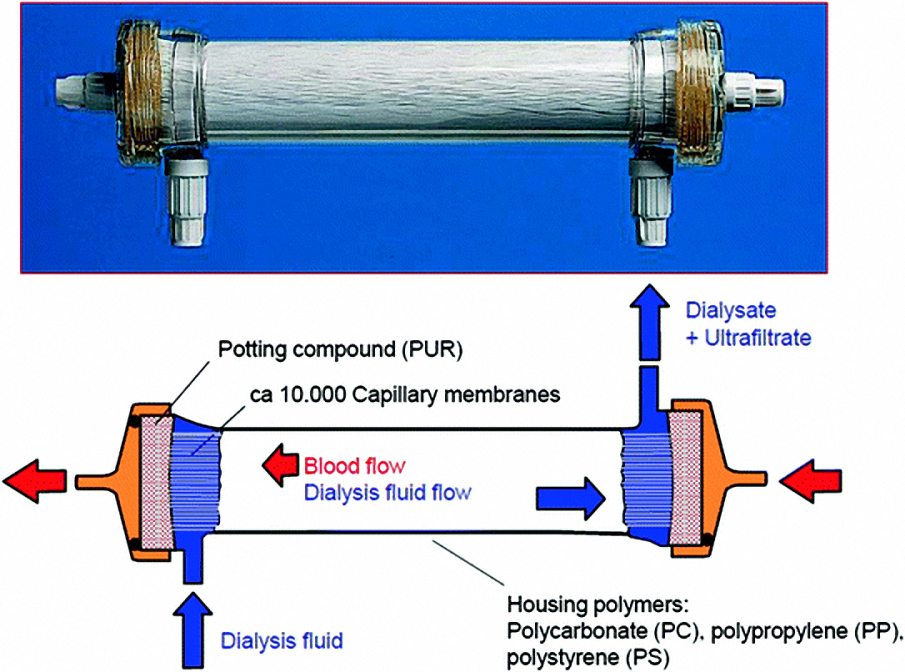 |
| Илл. 2 |
Давайте теперь рассмотрим, за счёт каких физических процессов происходит очищение во время гемодиализа и как указанные факторы на это влияют. Имея два раствора, разделённых полупроницаемой мембраной, мы можем создавать градиент концентрации или градиент гидростатического давления по обе её стороны или использовать их комбинацию. Если создаётся градиент концентрации, то происходят диффузия и осмос. Если создаётся градиент гидростатического давления, то одновременно протекают процессы ультрафильтрации и конвекции.
Градиент концентрации и сопутствующая ему диффузия — явление хорошо известное нам из повседневной жизни. Просто понять, что происходит во время диализа, основываясь на бытовом опыте. Каждому доводилось заваривать чай из пакетика. В тот момент, когда мы только наливаем воду в чашку с пакетиком и раствор начинает постепенно окрашиваться, мы собственными глазами можем увидеть, как начинается диффузия. Договоримся, что наш пакетик содержит большое количество условных «молекул чая». В кипятке «молекул чая» совсем не было, поэтому из пакетика по градиенту концентрации они начинают распространяться в чашку, окрашивая раствор во всё более интенсивный цвет. Рано или поздно наступит такой момент, когда более крепкий чай мы уже не сможем получить, так как концентрации внутри пакетика и снаружи уравновесятся. Сам пакетик при этом прекрасно иллюстрирует идею полупроницаемой мембраны. Раствор в чашке содержит только «молекулы чая», а все чаинки, крупные элементы, остаются внутри пакетика. То же самое происходит и во время процедуры гемодиализа. В крови пациента находятся некие «вредные» молекулы, от которых мы хотим избавиться, а в диализирующем растворе их совсем нет, поэтому они по градиенту концентрации удаляются в раствор при экстракорпоральных методах лечения. Возможен и обратный процесс, так как мембрана проницаема в обоих направлениях. Например, если у пациента гипокальциемия. Пользуясь услугами диффузии, мы можем его восполнить: ионы кальция по градиенту концентрации поступят из раствора в кровь. Точно так же восполняется дефицит бикарбоната при ацидозе. Диффузией лучше всего удаляются мелкие молекулы, так как они наиболее подвижны и диффундируют активнее, чем молекулы средних и крупных размеров.
Роль осмоса, происходящего в процессе гемодиализа, менее значима, чем при выполнении перитонеального диализа. Осмос — перемещение растворителя, то есть воды. Для этого в процессе ГД используется ультрафильтрация, которая основана на градиенте гидростатического давления и обладает гораздо более мощным эффектом. Градиент создаётся в современных аппаратах специальным насосом, и вода высасывается из крови сквозь мембрану. Если наша цель — удалить только воду, такая процедура носит название изолированной ультрафильтрации (ИУФ). Самостоятельно она используется редко, поскольку служит только для контроля гидробаланса. В сочетании с гемодиализом она необходима у пациентов с олиго- и анурией, задержкой жидкости, и является жизнеспасающей.
Интересно, что ультрафильтрация обуславливает возникновение ещё одного физического процесса, конвекции. Конвекция — перенос растворённых веществ с током растворителя. При этом с водой удаляются все вещества, способные пройти сквозь поры мембраны, в той концентрации, в которой они в ней содержатся. Возвращаясь к примеру с пакетиком чая, если мы его вытащим из чашки и отожмём, выжмется чай, то есть раствор, а не просто вода. На этом явлении основан конвекционный клиренс, который используется в ряде экстракорпоральных процедур. Важно понимать его отличие от ИУФ. ИУФ применима только для устранения гипергидратации, потому что мы удаляем только ту воду, которую можно безопасно убрать из плазмы крови пациента. Если мы будем продолжать этот процесс слишком долго, то в какой-то момент мы получим такую гемоконцентрацию, что фильтр затромбируется или, что ещё хуже, у пациента возникнет гипотония из-за созданной нами гиповолемии [1, с. 666]. Ограничения довольно строгие, и то количество воды, которое можно безопасно удалить, недостаточно для «очищения крови». Помните, в начале статьи мы говорили, что мелкие молекулы прекрасно распределяются не только в сосудистом русле, но и за его пределами? Поэтому, если мы хотим использовать конвекцию, логично было бы не просто удалять воду, но и восполнять эквивалентным объёмом замещающей жидкости. Если мы заварили чашку слишком крепкого чая, то можно его разбавить. Для этого необходимо не только выплеснуть его часть, ведь концентрация в оставшемся объёме останется прежней, но и долить чистой воды. Так и происходит, когда используется конвекционный клиренс, только объёмы замещения могут быть примерно равны массе тела пациента и более. Такая процедура называется гемофильтрация (ГФ). Она нужна, если требуется удалить так называемые «средние» молекулы, те, что способны пройти сквозь диализную мембрану, но плохо удаляются диффузией из-за меньшей подвижности. ГФ можно использовать совместно с гемодиализом, чтобы увеличить эффективность очищения в единицу времени, одновременно задействуя и диффузионный, и конвекционный клиренс. Такая процедура называется гемодиафильтрация. Конвекция используется и при мембранном плазмаферезе для удаления очень крупных молекул.
Для диализных процедур берутся мембраны с порами сравнительно небольшого размера. Даже высокопроницаемые диализаторы для острого ГД пропускают молекулы весом до 30 тысяч дальтон. Сравните это с мембранами для плазмафереза, например, способными отфильтровать и 2 миллиона дальтон. Совершенно очевидно, что через слишком маленькие поры физически не могут «протиснуться» очень крупные молекулы, как бы мы ни старались их удалить конвекцией. Это могло бы показаться недостатком, но в тех клинических ситуациях, когда нужен гемодиализ, это достоинство, так как мы избегаем потерь необходимых организму белков крови.
Из этих теоретических выкладок можно сделать вывод о том, что диализные процедуры эффективны для удаления мелких и средних водорастворимых молекул и самой воды.
Что же это за «плохие» молекулы на практике, в экстракорпоральных методах лечения? Показания к началу диализной терапии делятся на классические, почечные, и нетрадиционные, для полиорганной поддержки. К внепочечным показаниям относятся, например, экзогенные отравления и передозировка лекарственных средств, острый панкреатит, септический шок, острый респираторный дистресс-синдром, обеспечение инфузионной и нутритивной поддержки, ряд других. Многие из них до сих пор дискутабельны и в медицине человека, а о ветеринарных данных вообще не приходится говорить в связи с их скудностью. Наиболее практически значимыми показаниями для ГД являются острые отравления и классические, почечные, о них и поговорим подробнее.
Методы, основанные на диффузионно-конвекционном клиренсе, способны удалять экзотоксины и медикаменты, но в различной степени, при некоторых отравлениях с ними успешно конкурирует гемокарбоперфузия. Условия для применения гемодиализа на низкопроницаемых мембранах при отравлениях — водорастворимые токсины, с низким белковым связыванием и молекулярным весом менее 500 дальтон. Успешность лечения также зависит от особенностей метаболизма и объёма распределения данного вещества. ГД показан при отравлении этиленгликолем, метанолом, этанолом, изопропанолом, салицилатами, габапентином, фенобарбиталом, ацетаминофеном, аминогликозидами, ацикловиром, трициклическими антидепрессантами. Хотя обычно отравление изониазидом достаточно эффективно лечится пиридоксином, можно прибегать к ГД в случае, если пациент не отвечает на стандартную терапию при очень сильной интоксикации. Гемодиализ одновременно корректирует кислотно-щелочные и электролитные отклонения, которые могут сопровождать некоторые отравления (например, этиленгликоль и салицилаты). ГД и ГФ на высокопроницаемых мембранах удаляет токсины более высокого молекулярного веса, до 20–40 тысяч дальтон.
При отравлениях экстракорпоральная терапия показана в следующих ситуациях:
- полученная доза является токсичной (примерным ориентиром может служить справочная ЛД 50);
- вещество элиминируется из организма слишком медленно, чтобы избежать нежелательных последствий, или вызывает повреждение органов, ответственных за его метаболизм и выведение;
- интоксикация приводит к грубым гемодинамическим нарушениям (например, дигоксин) или значительному угнетению ЦНС (например, фенобарбитал), угрожающему остановкой дыхания или сердцебиения.
Лечение отравлений довольно сложная задача в ветеринарной медицине. экстракорпоральные методы будут действительно эффективны, только если они используются своевременно: когда яд циркулирует в крови, и мы можем его оттуда убрать. Если яд или его метаболиты поразили органы-мишени, мы, конечно, тоже будем лечить такого пациента, в том числе и экстракорпоральными методами, если это необходимо. Однако прогноз будет хуже. К сожалению, обычным поводом обращения владельцев в клинику служит развёрнутая симптоматика. Нередко к нам доставляют пациента в терминальном состоянии. В такой ситуации не приходится надеяться на мгновенное выздоровление после первой процедуры. Ведь гемодиализ не какое-то волшебное средство, а способ лечения, имеющий определённые возможности исходя из объективных физических и патофизиологических процессов.
Чаще всего всем нам, думаю, приходится сталкиваться с отравлением этиленгликолем. Это наиболее яркий пример необходимости экстренного вмешательства. Гемодиализ очень эффективен для удаления как самого этиленгликоля, так и его токсичных метаболитов. Поэтому, сделав процедуру в первые сутки отравления, мы проводим этиотропное лечение и спасаем пациента [1, с. 669]. Большинство животных поступает к нам с анурией спустя двое-трое суток после отравления, и нам остаётся только бороться с симптомами почечной недостаточности. Такой пациент может провести на диализе месяц и более, пока не произойдёт восстановление почечной функции, если это вообще возможно.
Наиболее очевидным показанием для начала гемодиализа в ветеринарии является острая почечная недостаточность (ОПН). Поэтому в литературе часто можно увидеть, что диализные методики называют заместительной почечной терапией (ЗПТ).
При почечной недостаточности мы можем обнаружить у пациента множество мелких молекул, от которых нам бы хотелось избавиться. Это гиперазотемия (мочевина, креатинин), гиперкалиемия, ацидоз (как органический, так и неорганический), фосфат. Ещё большее число «вредных» молекул в обычной клинической практике мы никак не идентифицируем. На данный момент известно уже более ста различных молекул «уремических токсинов», задерживающихся в организме при хронической болезни почек. В медицине человека исследованиями в этой области занимается Европейская рабочая группа по уремическим токсинам (EUTOX), обновления по открытиям новых молекул публикуются на сайте www.uremic-toxins.org. Подобные исследования в группах пациентов с острым повреждением почек (ОПП) проводить сложнее, поэтому таких данных практически нет. Даже оставаясь неузнанными, эти вещества продолжают причинять вред организму. Благо, что диализирующему раствору при экстракорпоральных методах лечения безразлично, мочевина это или другой «уремический токсин», всё, что растворимо в воде и имеет небольшие размеры, будет удалено в раствор, так как в нём этих веществ не содержится.
При лечении пациентов с ОПП возникает и другой вопрос, представляющий собой отдельную проблему. Когда нужно начинать диализ? Как долго можно выжидать ответа на консервативное лечение, если у пациента олигурия или высокий уровень азотемии?
Вопрос этот до сих пор однозначно не решён даже в медицине человека. Есть общепризнанные критерии начала ЗПТ, которые продолжают исследоваться и уточняться. Очевидным прогрессом медицины человека в данной области за последнее время является постепенный переход от не совсем определённых рекомендаций к более конкретным пороговым точкам инициации ЗПТ. Дело осложняется тем, что в терапии острых пациентов затруднительно проводить масштабные клинические исследования с хорошей мощностью для получения результатов высокой степени доказательности. В ветеринарии дела обстоят ещё хуже, так как у ряда наших пациентов явным ограничивающим фактором для начала диализного лечения становится его высокая стоимость и отсутствие доступных диализных центров в регионах. Таким образом, основное, на что мы можем ориентироваться в своей работе, это медицинские рекомендации и небольшой объём ветеринарных источников от наших зарубежных коллег.
Гипергидратация и неадекватный диурез
Объёмная перегрузка — один из наиболее значимых критериев экстренной инициации ЗПТ в медицине человека. Этой проблеме уделяется большое внимание, и на данный момент существует целый ряд качественных исследований, доказавших, что гипергидратация неблагоприятно влияет на исход любых заболеваний даже без повреждения почек. Играет роль не только величина, но и длительность объёмной перегрузки. У пациентов с ОПП установлена достоверная связь между объёмной перегрузкой и летальностью [5]. Данные о неблагоприятном влиянии гипергидратации на исход постепенно накапливаются и в ветеринарной медицине [3].
Эта информация должна побуждать практикующего врача более внимательно относиться к учёту баланса жидкости в организме пациента и максимально быстро принимать решение о начале ЗПТ в случае появления признаков перегрузки объёмом.
Обычно ветеринарный пациент оказывается гипергидратированным уже в процессе лечения, то есть находясь в клинике под наблюдением врачей. В таких ситуациях наиболее обидно, что само лечение фактически становится причиной гибели животного, если мы не обеспечиваем ему достаточный мониторинг. Оптимально, с прогностической точки зрения, начинать диализ не тогда, когда уже развились жизнеугрожающие осложнения в виде отёка лёгких или мозга, а когда намечается тенденция к положительному водному балансу. Необходимым средством мониторинга в этом плане является почасовой диурез. В практической работе следует учитывать, что олигурия от 6 до 12 часов — более важный критерий инициации ЗПТ, чем азотемия. Важно также понимать, что у животного с нормальным давлением и гидратацией, находящегося на инфузии, при диурезе менее 1 мл/кг/ч констатируется абсолютная олигурия [1, с. 521; 8, с. 4667]. Кроме того, согласно многочисленным медицинским исследованиям, при критических состояниях длительное выжидание ответа на диуретики ассоциировано с ухудшением выживаемости независимо от восстановления диуреза. В одном из последних крупном плацебо-контролируемом исследовании показано, что фуросемид не снижает прогрессирование ОПП, не улучшает восстановление почек, не снижает потребности в диализе; его использование было ассоциировано с большими электролитными нарушениями [6].
По этой причине в настоящее время рекомендуется применять диуретики только для лечения перегрузки объёмом и гиперкалиемии у пациентов с сохранённым диурезом
[2, с. 504], а не для лечения олигоанурии. При отсутствии восстановления диуреза в ответ на инфузионную терапию диализное лечение должно быть начато как можно скорее. На практике приходится учитывать ещё и время, которое затрачивается на организацию доставки пациента в клинику с диализным оборудованием.
Электролитные нарушения и нарушения кислотно-основного соотношения (КОС)
Критерием инициации ЗПТ являются жизнеугрожающие электролитные нарушения и нарушения КОС. На данный момент имеется крупное ретроспективное исследование, показавшее связь электролитных нарушений с увеличением летальности у кошек [4]. Наиболее частой проблемой у пациентов с олигоанурией или обструкцией является гиперкалиемия. К сожалению, критический уровень калия, при котором необходимо проводить диализное лечение у животных, точно не установлен. Диализ рекомендуется, если повышенный калий не снижается на обычной инфузионной терапии или продолжает расти в течение первых 12–24 часов стационарного лечения [8, с. 4670]. У людей безусловным критерием экстренной инициации ЗПТ является калий от 6,5 ммоль/л или быстро возрастающий сывороточный калий [7]. При этом, чтобы принять решение о начале экстракорпоральной терапии, классические изменения ЭКГ считаются необязательными. Начинать диализ нужно до момента появления осложнений.
Показанием для гемодиализа может стать гипернатриемия свыше 170 ммоль/л, не поддающаяся традиционной терапии. Поскольку гипернатриемия ассоциирована с риском церебральных дисфункций и летальных исходов, она обоснована как критерий инициации диализного лечения. Аналогичная ситуация со значительно пониженным натрием (менее 115 ммоль/л) [7].
Диализ эффективно решает проблемы нарушения КОС. Чаще всего приходится сталкиваться с ацидозом. Критерием инициации ЗПТ считаются такие показатели, как дефицит ВЕ > −8–12 ммоль/л и рН < 7,2 [7]. Традиционная инфузионная терапия бикарбонатом натрия не должна проводиться бесконечно, поскольку несёт риск гипернатриемии и гиперволемии и отсрочит начало диализного лечения. Здесь тоже работает принцип, что, если мы не добились успеха в коррекции ацидоза за 12–24 часа консервативной терапии, то следует срочно прибегнуть к диализному лечению.
Азотемия
При каких значениях мочевины и креатинина делать диализ? Такой вопрос чаще всего возникает у ветеринарных врачей, хотя этот критерий является не столь жизнеугрожающим, как тяжёлые электролитные нарушения, ацидоз или гипергидратация. Тем не менее, проблема остаётся актуальной, так как до сих пор во многих клиниках это единственные доступные биохимические маркеры. Есть мнения, что оптимально начинать ЗПТ до перехода ОПП в стадию 4 или 5 по IRIS [2, с. 511], ассоциированных с худшим прогнозом. Это выглядит вполне логичным, но пока нет исследований, подтвердивших влияние времени начала ЗПТ в зависимости от уровня азотемии на выживаемость ветеринарных пациентов. Если же сделать обзор по ветеринарным статьям и оценить, когда чаще всего начинали диализ, выясняется, что это происходит при уровне мочевины более 90–100 мг/дл (в привычных для нас ммоль/л это примерно 15–17) и креатинина выше 6–10 мг/дл (530–884 мкмоль/л). Понятно, почему так происходит на практике. Животные обычно либо поступают с уже очень высокой азотемией, либо врачи и владельцы могут пытаться оттянуть начало ЗПТ в связи с высокой стоимостью процедур до тех пор, пока состояние пациента не начнёт ухудшаться. Тем не менее, при ОПН рекомендуют начинать диализ, если азотемия у животного прогрессирует в течение 6–12 часов или не снижается на консервативном лечении в течение 24 часов.
Важным клиническим аспектом, связанным с уровнем азотемии считается то, как она влияет на состояние данного пациента. Среди тяжёлых последствий уремии чаще всего можно наблюдать энцефалопатию, нейропатию, гастроинтестинальные симптомы вплоть до перитонеальных. Следует сохранять настороженность по поводу геморрагического синдрома. Клиническую манифестацию уремии у пациента считают достаточным основанием для раннего начала ЗПТ вне зависимости от уровня мочевины и креатинина, даже если диурез сохранён или повышен, так как при ОПН и небольшая уремическая интоксикация может быть очень значимой ввиду отсутствия времени на адаптацию. Поэтому, если состояние животного остаётся тяжёлым, несмотря на консервативное лечение в течение 12–24 часов [1, с. 651], или же происходит ухудшение, лучше начать диализное лечение, чтобы избежать прогрессирования симптомов и развития осложнений.
Резюмируя сказанное, отмечу, что для принятия решения о начале гемодиализа при ОПН важен индивидуальный и комплексный подход в оценке критериев инициации ЗПТ, внимание к динамике в первые сутки лечения. Основные цели лечения: при объёмной перегрузке достичь постоянного нулевого водного баланса уже в течение первых-вторых суток, минимизировать клинико-лабораторные проявления ОПН и ориентироваться на динамику органных дисфункций. Если результата не удаётся добиться традиционными терапевтическими средствами, есть все основания прибегнуть к экстракорпоральной поддержке. Как и любое другое лечение, гемодиализ эффективен только при своевременном применении. Необходимо начинать лечение до наступления необратимых структурных нарушений в почках и развития тяжёлых системных осложнений.
Сложность, затратность и узкая направленность применения ГД будет ограничивать его широкое распространение в ветеринарной практике. Тем не менее, нет альтернативной терапии, столь же эффективной для животных с тяжёлой уремией, рефрактерной олигурией, угрожающей жизни гиперволемией или острым отравлением.
Литература
- Fluid, Electrolyte and Acid-Base Disorders in Small Animal Practice 3rd Edition, Stephen DiBartola, Saunders, 2005, 720 pp., Chapter 22 Fluid Therapy During Intrinsic Renal Failure, Dennis J. Chew Jennifer A. Gieg; Сh 29 Hemodialysis, Larry D. Cowgill And Thierry Francey.
- Nephrology and urology of small animals / edited by Joe Bartges, David J. Polzin, Blackwell Publishing, 2011, 904 рp., Chapter 49 Acute kidney insufficiency Larry D. Cowgill and Cathy Langston.
- Retrospective evaluation of fluid overload and relationship to outcome in critically ill dogs. Cavanagh A.A., Sullivan L.A., Hansen B.D. J Vet Emerg Crit Care (San Antonio), 2016.
- Multivariable analysis of the association between electrolyte disturbances and mortality in cats Robert Goggs, Sage De Rosa and Daniel J Fletcher Journal of Feline Medicine and Surgery, 2017.
- Zhang L, Chen Z, Diao Y, et al. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: a systematic review and meta-analysis. J Crit Care 2015.
- Bagshaw S.M. et al The effect of low-dose furosemide in critically ill patients with early acute kidney injury: A pilot randomized blinded controlled trial (the SPARK study). J Crit Care. 2017.
- Критерии инициации заместительной почечной терапии при критических состояниях, Пособие для врачей, Т.В. Мухоедова, Новосибирск, 2011.
- Textbook of Veterinary Internal Medicine 8th Edition, Stephen J. Ettinger, Edward.
- Feldman, Etienne Cté, Elsevier, 2017, 5875 pp., Chapter 322 Acute Kidney Injury, Cathy E. Langston.
СВМ № 5/2018