Elbieta Gabriela Giza, Marta Ponek, Józef Marian Nicpo and Marcin Adam Wrzosek
Department of Internal Medicine and Clinic of Horses, Dogs and Cats, Faculty of Veterinary Medicine, Wroclaw University of Environmental and Life Sciences, Wroclaw, Poland
Резюме
Введение. Периферическая нейропатия является наиболее частым первым признаком гипотиреоза у собак. Данных об исследованиях с использованием электродиагностики у собак с гипотиреозом в сочетании с полинейропатией существует достаточно мало, и обычно эти исследования не включают в себя контрольную оценку состояния пациентов после заместительной терапии гормонами. Целью данной работы стал детальный ретроспективный анализ находок на электромиографии (electromyography, EMG), исследованиях скорости проведения импульса по мотонейронам (motor nerve conduction velocity, MNCV), исследования F-волн и реакции на звуковую стимуляцию ствола мозга (brainstem auditory evoked response, BAER) у 24 собак с полинейропатией и подозрением на первичный гипотиреоз со сравнением результатов этих тестов до и после проведения терапии левотироксином и оценкой клинического исхода.
Результаты. Результаты исследований собак с гипотиреозом показали значительное снижение MNCV при проксимально-дистальной и срединно-дистальной стимуляции, снижение амплитуды сложных потенциалов действия мышечной ткани (compound muscle action potentials, CMAP), увеличение продолжительности CMAP и задержки дистального сигнала перед началом лечения. У 50% собак отмечалось увеличение задержки F-волн. Нормальные показатели BAER регистрировались у 78% пациентов с гипотиреозом, не имеющих вестибулярных нарушений. У остальных пациентов отмечалось билатеральное удлинение V пика и интервала между I–V пиками. У собак с сопутствующими вестибулярными нарушениями отмечалось гомолатеральное удлинение пиков с нормальными межпиковыми интервалами и снижение амплитуд I и II волн. Сравнение результатов до и после двух месяцев терапии выявило снижение патологической активности на EMG, улучшение проксимальных, срединных и дистальных амплитуд CMAP и повышение скорости проксимально-дистальной проводимости у всех собак. Длина F-волн нормализовалась у 38% собак. Повторная оценка BAER выявила устойчивую пролонгацию длины I, II, III и V пиков и снижение амплитуды I волны на стороне поражения у всех собак с проявлениями вестибулярных расстройств. А у собак без вестибулярных расстройств длины V пика и I–V межпиковых интервалов снизились до нормальных значений после курса лечения.
Выводы. Результаты демонстрируют явления демиелинизации и аксональный характер полинейропатии у собак с подозрением на гипотиреоз. У большинства собак без вестибулярных расстройств не наблюдалось нарушения проводимости периферических или центральных слуховых нервных путей, сопутствующих генерализованной нейропатии. Последующие осмотры демонстрируют благоприятные клинические исходы и только частичное улучшение результатов электрофизиологических тестов.
Введение
Гипотиреоз является самым распространённым видом эндокринопатий у взрослых, средних и крупных размеров собак и характеризуется разнообразной клинической манифестацией [1, 2]. И при том, что классические признаки заболевания легко распознаваемы, о корреляции между гипотиреозом и неврологической дисфункцией известно значительно меньше [3]. На данный момент и центральная, и периферическая неврологическая симптоматика подробно описаны в ветеринарной литературе [4]. Однако, хотя считается, что мозг у животных достаточно устойчив к влиянию гипотиреоза [5], в литературе довольно часто встречаются описания судорог, дезориентации, комы и нарушений функции ствола мозга у собак с гипотиреозом [3, 6, 7]. К периферическим неврологическим синдромам, встречающимся у собак с гипотиреозом, относятся краниальная нейропатия (дисфункция тройничного, лицевого, преддверно-улиткового нервов), ларингеальный паралич, мегаэзофагус и, чаще всего, нейромышечная симптоматика генерализованного характера [4, 7, 8].
Патофизиология полинейропатии при гипотиреозе изучена не до конца [9]. Основываясь на исследованиях из области человеческой медицины, можно предположить, что снижение метаболизма в нейронах может вести к нарушению аксонного транспорта и, как следствие, аксональной атрофии [10, 11]. Другое объяснение полинейропатии — демиелинизация, вызванная накоплением мукополисахаридов в цитоплазме шванновских клеток и соединительной ткани нерва [9, 12]. Это также может быть результатом сосудистых повреждений из-за нарушения гемато-нейронного барьера [13, 14].
Полинейропатия и миопатия, ассоциированные с гипотиреозом, у собак могут проявляться как снижение толерантности к нагрузкам, одышка, напряжённая походка, мышечная атрофия, преходящая слабость конечностей, пара- и тетрапарезы [15, 16, 17]. У животных с гипотиреозом ухудшается проприоцепция, понижается артериальное давление и ослабевают — а иногда и совсем отсутствуют — спинальные рефлексы [15]. Согласно предыдущим отчётам, клиническая симптоматика периферической нервной дисфункции и центральных вестибулярных нарушений у собак с гипотиреозом обычно разрешается после 2-месячного курса левотироксина [6, 18, 19].
Электродиагностические находки у таких собак с неврологической симптоматикой включают в себя усиление произвольной активности и патологическую спонтанную активность на электромиографии (EMG), снижение амплитуд сложных потенциалов действия мышечной ткани (CMAP), снижение скорости проведения импульса волокон моторных нейронов (MNCV) и отклонения при звуковой стимуляции ствола мозга (BAER) [6, 8, 9]. Большинство исследований в этой области ветеринарии проводилось на очень малых группах собак (доклады случаев и доклады серий случаев). В большинстве случаев проводилась единовременная электродиагностика без повторной оценки после курса лечения, особенно в случаях, когда удавалось добиться полного разрешения клинической симптоматики.
Целью данного исследования стала ретроспективная оценка результатов тестов EMG, MNCV, F-волн и BAER у 24 собак с предположительно спонтанно развившимся гипотиреозом и периферической нейропатией, а также сравнение результатов до и после проведения курса заместительной терапии левотироксином с оценкой клинического исхода.
Методы
Отбор случаев
Записи электродиагностики 34 собак, направленных на консультацию к неврологу в Клинику лошадей, собак и кошек при Университете естественных наук Вроцлава в период с февраля 2010 по февраль 2014 года, были проанализированы ретроспективно.
Группа А состояла из 24 собак с предположительным диагнозом гипотиреоза и полинейропатии на основе следующих критериев: 1) гипотиреоидный статус с высокой вероятностью первичного гипотиреоза на основании клинических проявлений, анализах крови и тестирования функции щитовидной железы (снижение Т4, fТ4 и увеличение сТТГ; если сТТГ в норме — наличие других лабораторных отклонений и как минимум 2 клинических не нейрогенных признака гипотиреоза); 2) неврологические признаки прогрессирующего, генерализованного нарушения дистальных отделов моторных нервных путей; 3) подтверждённая электродиагностикой периферическая нейропатия; 4) положительный ответ на заместительную гормональную терапию; 5) отсутствие находок на УЗИ брюшной полости, рентгенограммах грудной клетки, при анализе спинномозговой жидкости; 6) отсутствие патологических находок на МРТ головы в случаях с клиникой краниального нервного дефицита. Чтобы быть включёнными в исследование, пациенты не должны были иметь в анамнезе травмы, операции, контакты с токсинами и терапию фенобарбиталом.
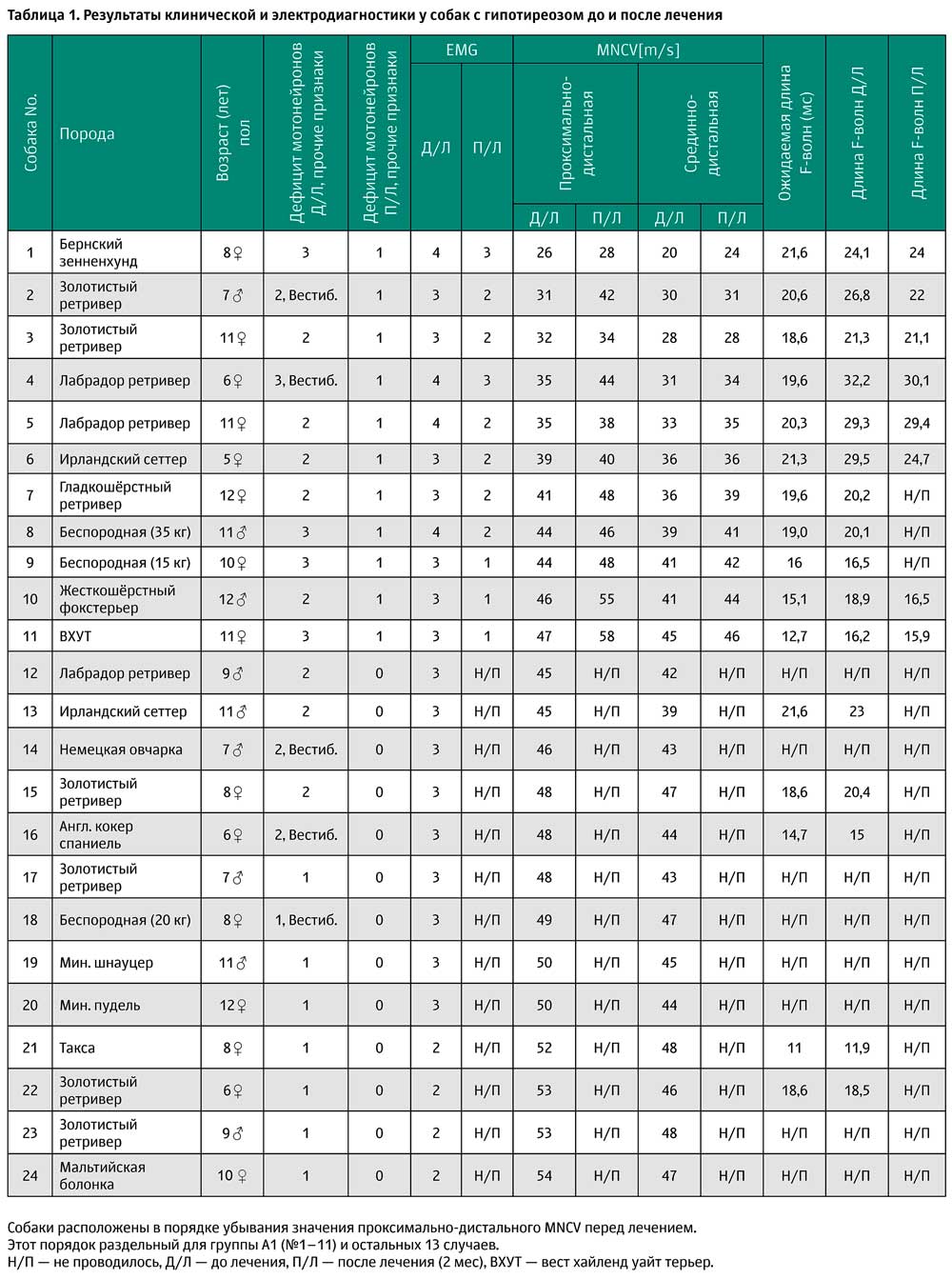
Возраст осмотренных собак с полинейропатией и гипотиреозом (предположительные диагнозы) при поступлении составил от 5 до 12 лет (в среднем 9 лет), 9 из них были кобелями (1/9 кастрированы) и 15 суками (11/15 стерилизованы). Подгруппа А1 состояла из 11 собак, прошедших повторную электродиагностику после вух месяцев заместительной гормональной терапии. Подробная информация, касающаяся породы собак, анамнеза и результатов электродиагностики, приведена в таблице 1.
Группа B (контрольная) состояла из 10 собак, направленных на неврологический осмотр, но получивших в результате диагноз ортопедического профиля и в остальном не имевших нарушений здоровья. Возраст этих собак приблизительно соответствовал собакам из группы А — от 5 до 10 лет (среднее 8 лет). В эту группу вошли 4 кобеля и 6 сук (4/6 стерилизованы). Вес находился в промежутке от 11 до 46 килограмм (среднее 23 кг). Гипотиреоз у собак в этой группы был исключён на основании анализа крови. Результаты тестов MNCV и BAER, а также длины, амплитуды и задержки CMAP были задокументированы. Все результаты были оценены как нормальные с учётом возраста, размера и длины конечностей, на основании сравнения с предыдущим отчётом [20].
Клинический осмотр
Все собаки прошли клинический, ортопедический и неврологический осмотр. Нарушения проводимости моторных нервов оценивались по следующей шкале: 0 — нормальная моторная функция и мышечная сила; 1 — умеренный моторный дефицит, мышечная слабость, амбулаторный парез; 2 — выраженный моторный дефицит, неамбулаторный парез; 3 — тяжёлый дефицит, полная потеря мышечной силы, плегия. Всем собакам был проведён стандартный для нейромышечных расстройств профиль анализов по Cuddon [9], включая гемато-биохимический анализ и исследование мочи на уринолизис. Функция щитовидной железы оценивалась по уровню общего тироксина (Т4; норма 1,4–4,5 мкг/дл), свободного тироксина (fT4; норма 8–40 пмоль/л) и тиреотропного гормона собак в сыворотке (cTSH; норма 0,01–0,50 нг/мл).
Электрофизиологический осмотр проводился при комнатной температуре 22°C с использованием портативного оборудования (Nicolet Viasys Healthcare; программное обеспечение Viking Quest v 11.0). Перед тестированием собаки получали премедикацию в виде комбинации медетомидина (20 мкг/кг) и буторфанола (0,1 мг/кг) внутримышечно. Само тестирование проводилось под общим наркозом, индуцированным пропофолом в дозе 1–4 мг/кг и с поддерживающей дозой 0,1–0,4 мг/кг/мин.
Электромиография проводилась всем собакам во всех группах путём внутримышечного введения игольчатого электрода в аппедикулярные и аксиальные мышцы, минусовой электрод располагался подкожно на боку животного. Получислительная цифровая шкала от Kimura [21] была доработана и адаптирована для целей данного исследования для оценки степени выраженности изменений EMG (таблица 2).
Таблица 2. Модифицированная получислительная цифровая шкала для электромиографической оценки силы патологических потенциалов
| Степень | Описание |
| 0 | Нет патологических потенциалов |
| 1 | Очень редкие потенциалы денервации |
| 2 | Спорадическая патологическая активность, регистрируемая в двух и более местах |
| 3 | Частая патологическая активность, регистрируемая вне зависимости от расположения иглы |
| 4 | Стойкая патологическая активность, регистрируемая вне зависимости от расположения иглы |
Исследование MNCV и F-волн проводилось с использованием: (1) двух стимулирующих игольчатых электродов, (2) концентрического записывающего игольчатого электрода, установленного в плантарную межкостную мышцу и (3) заземляющего электрода, установленного между стимулирующим и записывающим электродами. Измерения MNCV у всех собак — с гипотиреозом и полинейропатией и без — проводились по седалищному/большеберцовому нервам путём супрамаксимальной электростимуляции в течение 0,1 мс в трёх точках стимуляции по Walker et al. [22]: проксимальная — каудальнее большого вертела бедренной кости; срединная — на уровне надколенника, каудальнее к дистальному концу бедренной кости; дистальная — над подколенным сухожилием, латеральнее к связке икроножной мышцы. Записи параметров MNCV и CMAP анализировались и сравнивались между группами А и B. Те же параметры отдельно анализировались для пациентов из группы А1 до начала курса лечения.
Характеристика F-волн оценивалась на основании сравнения записанных данных с ожидаемыми, которые вычислялись по формуле: 3,45 + 0,33 × длина конечности (см) [20]. Длина конечностей измерялась на разогнутой конечности от уровня большого вертела до дистального конца III пальца. После стимуляции 16 импульсами измерялся и записывался наименьший период задержки до появления F-волн.
Тест BAER проводился в обеих группах собак по ранее описанной методике [20]. Коротко — стандартные подкожные игольчатые электроды устанавливались в области сосцевидного отростка (М): записывающий — на его вершине, добавочный — у основания уха, а минусовой электрод располагался в проекции середины I шейного позвонка.
Звуковая стимуляция осуществлялась через внутриканальные наушники сигналом 90 дБ. В контлатеральное ухо периодически посылался маскирующий шум в 60 дБ. Записи BAER у всех пациентов включали в себя регистрацию I–V волн, измерение их амплитуд и задержек и выявление I–V межпиковых задержек (interpeak latency, IPL). Все переменные сравнивались между группами А и В. У всех пациентов с выявленными отклонениями результатов BAER дополнительно проводилось сравнение с результатами этого теста после лечения. Тесту BAER всегда предшествовал отоскопический осмотр.
Повторные осмотры, включающие в себя оценку клинического и неврологического статуса, а также функции щитовидной железы, проводились примерно через 1 месяц после начала гормонозаместительной терапии в дозе 20 мкг/кг 2 раза в день у всех собак в группе А (с гипотиреозом и полинейропатией). Доза в дальнейшем корректировалась на основании клинического ответа и результатов анализов крови. Электродиагностика повторно проводилась через 2 месяца после начала терапии и всегда тем же специалистом, который проводил её в первый раз. Подробная информация для каждого случая представлена в таблице 1.
Результаты измерений подверглись статистическому анализу в программах Excel 6.0 и StatSoft Inc Statistica 10. Для сравнения непараметрических значений в группах А и В использовался непараметрический U-тест Mann–Whitney. Для сравнения показателей до и после курса терапии применялся t-тест Student. Показательными считались значения P<0,05.
Результаты
Клинические и электродиагностические находки перед началом курса лечения
Все 24 собаки в группе А (с гипотиреозом и полинейропатией) были представлены на осмотр с явлениями слабости и гипорефлексии. Сонливость отмечалась в 16/24 случаев, избыточный вес в 14/24 случаев, брадикардия — в 8/24 случаев и типичные дерматологические признаки — у 5/24 собак. Моторный дефицит был оценён на «1» у 8/24 собак, «2» — 11/24, «3» — у 5/24 пациентов (таблица 1). У 5 пациентов в дополнение к этому отмечались признаки периферической вестибулярной дисфункции (покачивание головы, горизонтальный нистагм, вестибулярный страбизм). Длительность проявления симптоматики варьировалась от 1 до 12 недель (в среднем 6 недель) с медленным прогрессированием явлений слабости конечностей у всех собак. Из опроса владельцев известно, что у 7 из 24 собак до поступления отмечалось резкое усиление явлений моторного дефицита. Манифестация вестибулярных симптомов также происходила остро во всех случаях.
Диагноз гипотиреоза у собак группы А ставился на основании лабораторных находок, в том числе снижения tT4 (24/24), увеличения cTSH (15/24). У всех собак с нормальным уровнем cTSH (9/24) отмечалась умеренная либо выраженная гиперхолестеролемия (натощак), у 7/9 собак отмечалась гипертриглицеридемия (натощак), у 4/9 — нормоцитарная анемия, у 2/9 — умеренное повышение АСТ и КК активности. В целом, у 22/24 собак в группе А выявлена гиперхолестеролемия, у 18/24 — гипертриглицеридемия, у 7/24 — анемия и у 6/24 собак была умеренно повышена активность АСТ и КК.
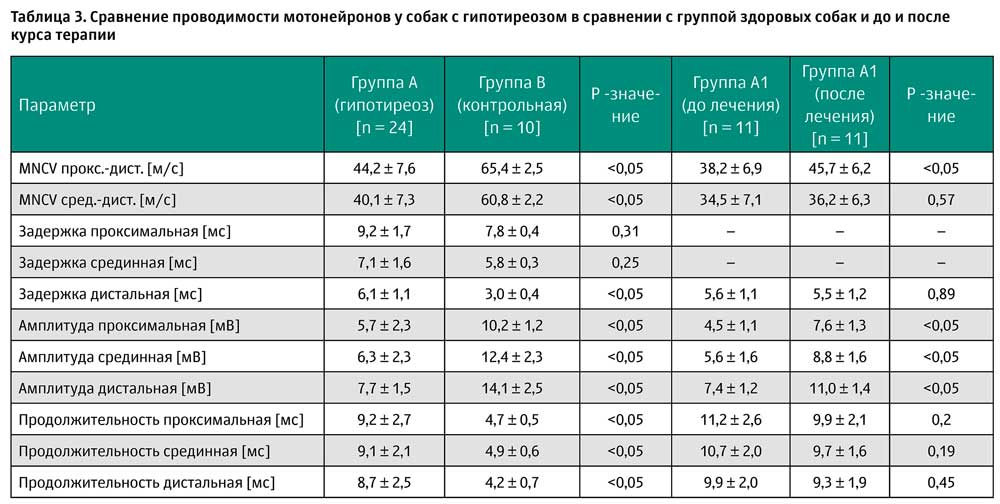
На EMG в группе А было выявлено увеличение произвольной активности у 14/24 собак, мультифокальные паттерны потенциалов фибрилляции (fibrillation potentials, Fps) — у всех 24 пациентов и заострение положительной фазы волн — у 18/24. Изменения были значительны во всех конечностях у всех пациентов в группе А. Аномальная активность одинаково оценивалась в проксимальных и дистальных отделах передних и задних конечностей. Потенциалы фибрилляции регистрировались в аксиальных мышцах у восьми собак. Выраженность изменений EMG для каждого пациента представлена в таблице 1. Исследование MNCV в группе А статистически значимое снижение проводимости при проксимально-дистальной (26–54 мс) и срединно-дистальной (20–48 мс) по сравнению с контрольной группой (таблица 3). Детальный анализ измерений CMAP выявил увеличение дистальной задержки, снижение амплитуды и увеличение продолжительности независимо от расположения точки стимуляции. F-волны исследовались у 16\24 собак
(№ 1–11, 13, 15, 16, 21, 22). Их задержка была увеличена на более чем 2 мс у 8 пациентов (50%) по сравнению с ожидаемой, вычисляемой для каждого пациента индивидуально (№ 1–6, 10, 11) (таблица 1).
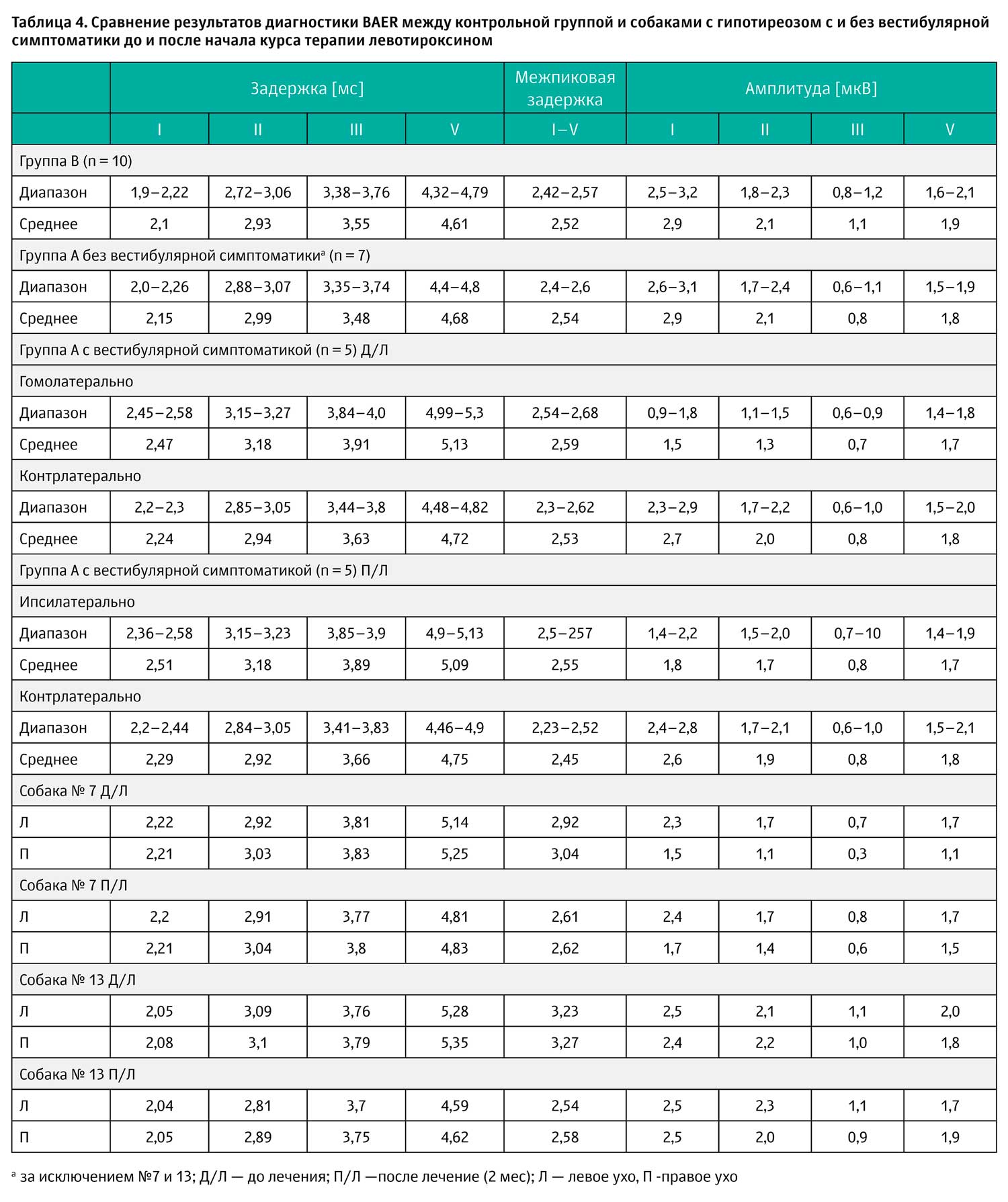
Исследование BAER проводилось у 14 пациентов в группе А, включая пять собак с вестибулярной симптоматикой. У собак № 2, 4, 14, 16 и 18, имеющих вестибулярные расстройства, определялись увеличенные пиковые задержки I, II, III и V волн с нормальной межпиковой задержкой I–V и снижение амплитуды волн I и II на поражённой стороне (таблица 4). Результаты BAER у 7/9 собак с гипотиреозом без вестибулярной дисфункции не имели значимых отличий от таковых у контрольной группы. У двух оставшихся собак (№ 7 и 13) наблюдалось билатеральное повышение пика V и увеличение межпиковой задержки I–V. У собаки № 5 отмечалось унилатеральное снижение амплитуды всех волн (таблица 4).
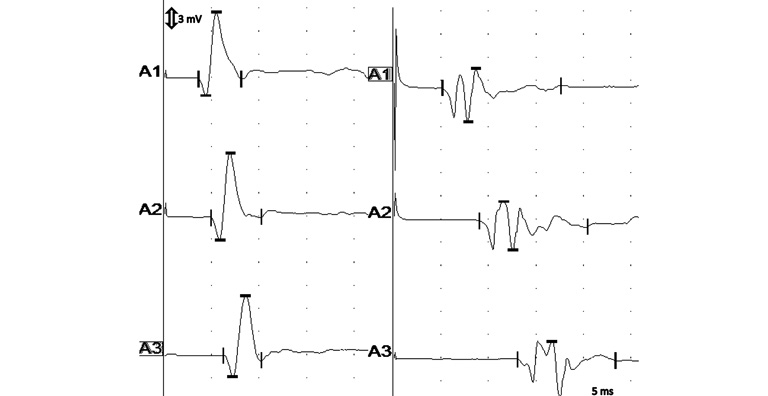
Результаты клинического, неврологического осмотра и лабораторных анализов у пациентов из группы В были в пределах нормы. Исследование EMG у этой группы показало отсутствие аномальных потенциалов активности и нормальную произвольную активность. MNCV при проксимально-дистальной стимуляции составила от 62 до 71 м/с, при срединно-дистальной — от 57 до 64 м/с. Сравнение нервной проводимости между двумя группами представлено на рисунке 1. Показатели F-волн не превышали ожидаемые более чем на 2 мс. Результаты теста BAER представлены в таблице 4.
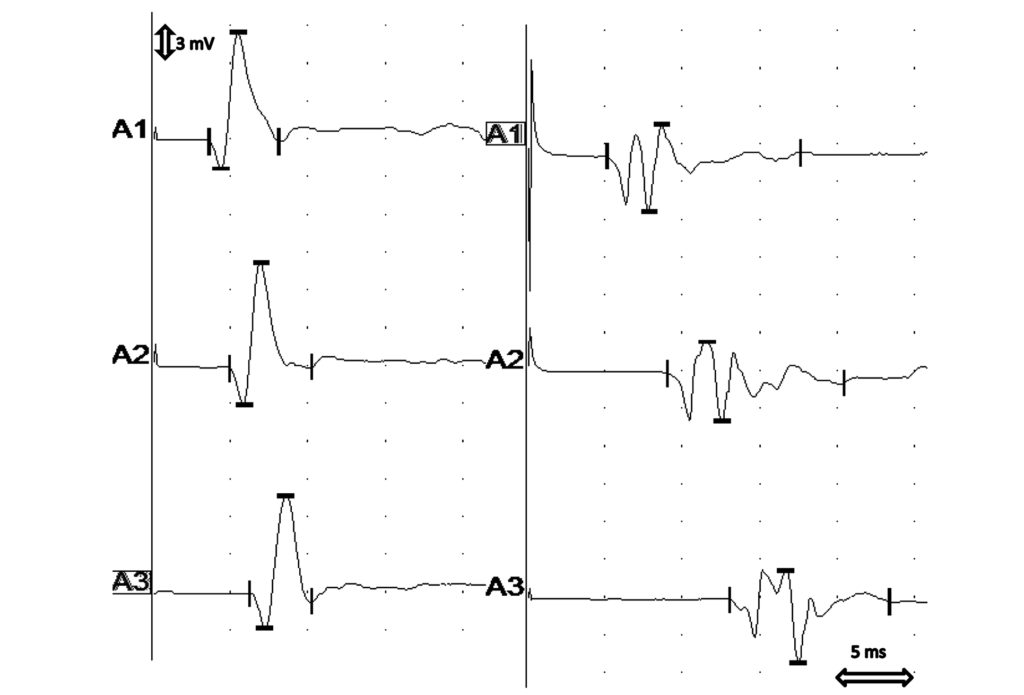 |
| Рисунок 1. Сравнение нервной проводимости у собак между группами А и В. Слева представлены измерения, полученные на 8-летней беспородной собаке из группы В. Значение MNCV составило 61–64 м/с, что было признано нормой. Справа представлены измерения у 7-летнего золотистого ретривера с подозрением на первичный гипотиреоз. MNCV снижено до 30–31 м/с. Сниженная амплитуда CMAP и увеличенная продолжительность CMAP во все точках стимуляции (дистальная А1, срединная А2, проксимальная А3) |
Клинические и электродиагностические находки после курса левотироксина
В группе А, первый контрольный осмотр был проведён через один месяц после начала курса левотироксина. К этому времени все собаки с гипотиреозом были более внимательны и активны. Неврологический осмотр выявил улучшение моторной функции как минимум на 1 степень у 19/24 собак. Собакам, у которых не было отмечено улучшений, со сниженным уровнем tT4 (№ 4 и 8), был назначен левотироксин в двойной дозе (40 мкг/кг 2 р/сут). У собак № 1, 5 и 9 уровень tT4 был в пределах норме или незначительно снижен. Поскольку заметного улучшения клинического состояния у этих собак также не отмечалось, доза левотироксина была увеличена до 30 мкг/кг 2 р/сут. У собаки № 19 уровень tT4 в сыворотке крови умеренно повышен, поэтому дозу препарата снизили до 15 мкг/кг 2 р/сут.
Через два месяца после начала курса результаты контрольного осмотра и лабораторных анализов были в норме у всех 24 собак. Все собаки с избыточным весом потеряли вес, однако, у 8 из них он все ещё оставался избыточным. У большинства собак вестибулярная симптоматика разрешилась. У трёх собак отмечалось лёгкое, но стойкое покачивание головы (№ 2, 16,18). Полное восстановление моторной функции (Степень «0») отмечалось у 13/24 собак (№ 12–24). У 11 собак, у которых на первом осмотре были диагностированы степени «3» (5/11) и «2» (6/11), на контрольном осмотре они снизились до «1» (амбулаторный тетрапарез). Эта группа была направлена на повторную электродиагностику и выделена в подгруппу А1.
На EMG снижение патологической активности отмечалось у всех собак — с гипотиреозом и без. Как видно в таблице 1, наблюдалась следующая картина улучшений: степень нарушения моторной функции у 2/11 собак снизилась с «4» до «3», у 2/11 — с «4» до «2», у 4/11 — с «3» до «2» и у 3/11 — с «3» до «1». Анализ записи MNCV выявил статистически значимое улучшение проксимальной, срединной и дистальной амплитуд CMAP и скорости проксимально-дистальной проводимости, по сравнению с результатами до лечения (таблица 3). Скорость срединно-дистальной проводимости, задержки и длины CMAP значительно не отличались до и после терапии в группе А1 (таблица 3). У восьми собак с увеличением задержки F-волн на первичном осмотре (№ 1–6 и 10, 11) было проведено повторное исследование. У 5/8 собак не наблюдалось значительных улучшений, у 2/8 задержка F-волн достигла нормальных показателей, у одной (№ 6) значительно уменьшилась, но всё же превосходила ожидаемую более чем 2 мс (таблица 1).
Измерение BAER повторно проводилось у пяти собак с вестибулярной симптоматикой (№ 2, 4, 14, 16, 18) и у двух собак с отклонениями в этом тесте при первичном осмотре (№ 7 и 13). Повторное исследование выявило устойчивое удлинение I, II, III и V пиков и снижение амплитуды I волны на поражённой стороне у всех собак с вестибулярной симптоматикой. После курса терапии амплитуда II волны значительно увеличилась у всех собак в этой группе (таблица 4). У собак без вестибулярной симптоматики (№ 7 и 13) после начала терапии значения задержки V пика и межпиковой задержки I–V достигли нормы. Амплитуды у собаки № 7, сниженные на первичном осмотре, на повторном значительно увеличились. Тем не менее, они все ещё были ниже значений, полученных на контрлатеральном ухе (таблица 4).
Обсуждение
Диагноз полинейропатии при гипотиреозе
Недостаточность секреции гормонов щитовидной железы рассматривается как вероятная причина полинейропатии у 2–4% людей [23]. Неврологические расстройства описываются у 6–29% собак с первичным гипотиреозом [1]. Периферическая нейропатия является наиболее подробно описанным неврологическим проявлением этого заболевания у собак [8, 18]. Тем не менее, точный диагноз первичного гипотиреоза собак довольно сложен [2]. Высокой точностью в выявлении гипотиреоза у собак (более 90%) обладает анализ уровня cTSH; уровни T4 и fT4 обычно понижены [24]. В то же время, у 20–40% собак с первичным гипотиреозом уровень cTSH находится в пределах нормы, что говорит о низкой чувствительности этого метода [2]. Аналогичный процент собак с нормальным уровнем cTSH и сниженными уровнями Т4 и fТ4 (37,5 %) наблюдался и в данном исследовании. Следует быть осторожным при постановке диагноза гипотиреоидной нейропатии, основываясь только на низком уровне гормонов щитовидной железы [9]. Следовательно, чтобы подтвердить диагноз первичного гипотиреоза у собак при нормальном уровне cTSH, в этом исследовании было необходимо выявить типичные клинические и неврологические признаки и сопутствующую гипохолестеролемию. Но даже несмотря на большое количество тестов, проведённых, чтобы исключить большинство системных заболеваний, нельзя полностью исключать негормональный этиогенез заболевания. Более того, нельзя исключать возможности того, что полинейропатия у собак, не вызванная гипотиреозом в некоторых случаях, самостоятельно разрешилась за двухмесячный период. Таким образом, в исследование могли не предумышленно войти случаи хронической воспалительной демилиенизирующей полинейропатии и дистальная денервационная болезнь [9].
Результаты демонстрируют наличие и демиелинизирующего, и аксонального характеров нейропатии у собак с недостаточностью гормонов щитовидной железы. И обычно достаточно сложно однозначно выделить один из этих процессов в качестве первичного (так как нейропатия с интенсивной демиелинизацией обычно сопровождается некоторой аксональной дегенерацией)[21]. У людей с гипотиреозом обычно присутствуют явления и аксоно-, и миелопатии с небольшим (52–57 %) преобладанием демиелинизирующего процесса [11, 23, 25]. В нашем исследовании демиелинизирующий процесс у пациентов подтверждался увеличением задержек CMAP и F-волн, снижением скорости нервной проводимости и темпоральной дисперсией. Снижение амплитуд CMAP и находки EMG свидетельствуют об аксональном характере процесса [26]. В то же время, они могут свидетельствовать о миелопатии, особенно в случаях с увеличенной активностью АСТ и КК [27]. В исследовании, проведённом Rossmeisl [27], у собак с хроническим гипотиреозом единственной находкой на электродиагностике была субклиническая миелопатия. У девяти собак с искусственно индуцированным гипотиреозом в ходе эксперимента не было выявлено никаких признаков полинейропатии — ни клинических, ни электродиагностических. Было выдвинуто предположение, что при спонтанно развившемся первичном гипотиреозе нарушению работы периферической нервной системы способствует нарушение иммунорегуляции [27].
Электродиагностические исследования в ходе лечения левотироксином
После начала курса ГЗТ у людей описывается широкий спектр электрофизиологических находок. Согласно Kececi et al. [25], явления полинейропатии у пациентов с гипотиреозом разрешаются в течение 3 месяцев ГЗТ. Авторы сообщают о значительном улучшении картины MNCV, нормализация значений задержек и амплитуд моторных потенциалов. Nemni et al. [28] описывает полное восстановление клинического статуса и значительное улучшение моторной и сенсорной проводимости, нормализацию значений задержек и амплитуд моторных потенциалов у трёх пациентов через трёх месяца ГЗТ. Схожие явления отмечались ещё у двух пациентов после 6 месяцев терапии. С другой стороны, другие авторы описывают отсутствие каких-либо изменений электродиагностической картины даже после длительного периода ГЗТ [11, 23]. Докладов, описывающих электродиагностические исследования до и после курса ГЗТ в ветеринарной медицине очень мало. Budsberg et al. [15] отмечает полное отсутствие патологической активности на EMG у трёх из четырёх собак и частичное улучшение картины у четвёртой собаки после двух месяцев лечения левотироксином. Похожие результаты у Jaggy et al. [8]: полное восстановление EMG активности и показателей MNCV у одной собаки с гипотиреозом и признаками полинейропатии через два месяца ГЗТ. В нашем исследовании отмечалось, что, независимо от клинического исхода, значительно улучшались только некоторые электродиагностические показатели (амплитуды CMAP, проксимально-дистальная MNCV и EMG картина).
Гипотиреоз и BAER
При недостаточности гормонов щитовидной железы у людей [29] и собак [6, 8] также отмечаются нарушения слуховой и вестибулярной функций. Вестибулярная симптоматика может быть единственным проявлением скрытой сопутствующей полинейропатии [8]. Поражение преддверно-улиточного нерва может быть ассоциировано с периферической нейропатией, но может развиваться и независимо от неё [9]. У всех собак в нашем исследовании на осмотре были выявлены признаки генерализованной полинейропатии, и у 21% из них отмечалась периферическая вестибулярная симптоматика до начала лечения. Находки BAER, включающие гомолатеральное удлинение задержек пиков с нормальной межпиковой задержкой и выраженное снижение амплитуды I волны, не улучшающиеся после лечения, свидетельствуют о наличии вестибуло-кохлеарной неропатии. Унилатеральный дефицит отдельного нерва также может быть связан с микседематозным сдавлением нерва (в этом случае преддверно-улиточного), поскольку он проходит через черепное отверстие [9]. Результаты тестов BAER у собак с гипотиреозом без вестибулярной симптоматики были в пределах нормы в 78% случаев. У остальных пациентов было билатеральное удлинение V пика и межпикового интервала I–V, что свидетельствует о центральном характере нарушений. Jaggy et al. [8] докладывает о сопутствующих отклонениях на BAER у собак с генерализованной полинейропатией без вестибулярной симптоматики. Thornton and Jarvis [29] описывают значительное снижение амплитуд II и V волн и увеличение I–V межпикового интервала у людей с гипотиреозом. Они считают, что такие отклонения можно объяснить низкой температурой тела у этих пациентов, а не ретрокохлеарными расстройствами. В нашем исследовании температура тела пациентов была в пределах нормы. Следовательно, мы не можем прибегнуть к такой интерпретации. В то же время, достоверно известно, что гормоны щитовидной железы контролируют синтез белков и миелина в центральных нервных слуховых путях [30]. Кроме того, T4 также участвует в роли нейротрансмиттера в ЦНС [30]. Это может объяснить центральный характер нарушения нервной проводимости, выявленной на BAER у наших пациентов. Существует предположение о том, что отклонения на BAER и сопутствующая полинейропатия в случаях подтверждённого первичного гипотиреоза может также объясняться сегментальной демиелинизацией [6].
Двухмесячный курс левотироксина привёл у наших пациентов к значительному улучшению клинической картины периферической вестибулярной симптоматики. Очень хороший клинический исход у собак с вестибулярными расстройствами и гипотиреозом также наблюдался и другими авторами [6, 8]. И всё же, в 77% случаев у Jaggy et al. [8] и в 60% — в нашем исследовании наблюдалось стойкое умеренное покачивание головы у пациентов даже спустя два месяца ГЗТ.
Результаты повторных тестов BAER показали лишь частичное улучшение после 2 месяцев курса ГЗТ. В других отчётах, полная нормализация показателей BAER достигалась через 6 недель лечения у одной собаки [6], и через 3-5 месяцев ещё у двух [8].
Заключение
Результаты электродиагностического исследования у собак с полинейропатией и подозрением на первичный гипотиреоз показало явления димиелинизации и аксональных повреждений в периферических нервах. У большинства пациентов без вестибулярной симптоматики не наблюдалось нарушения проводимости центральных или периферических нервных путей, сопутствующих генерализованной полинейропатии. Контрольные исследования свидетельствовали о хорошем клиническом исходе и лишь частичном восстановлении электродиагностических показателей.
Сокращения
BAER — звуковая стимуляция ствола мозга (brainstem auditory evoked response)
CMA — сложные потенциалы действия мышечной ткани (compound muscle action potential)
cTSH — тиреотропный гормон собак (canine thyroid stimulating hormone)
EMG — электромиография (electromyography)
FPs — потенциалы фибрилляции (fibrillation potentials)
fT4 — свободный тироксин (free thyroxine)
IPL — межпиковый интервал (interpeak latency)
MNCV — скорость проведения импульса по мотонейронам (motor nerve conduction velocity)
T4 — общий тироксин (total thyroxine)
ГЗТ — гормонозаместительная терапия
Литература
- Scott-Moncrieff JC. Clinical signs and concurrent diseases of hypothyroidism in dogs and cats. Vet Clin North Am Small Anim Pract. 2007;37:709–22.
- Scott-Moncrieff JC. Hypothyroidism. In: Feldman EC, Nelson RW, Reusch C, Scott-Moncrieff JC, editors. Canine and Feline endocrinology. Makati City: Elsevier; 2015. p. 77–135.
- Bertalan A, Glass EN, Kent M, de Lahunta A. Hypothyroid-associated neurologic signs in dogs. Vet Med. 2013;108:242–50.
- Bischel P, Jacobs G, Oliver JE. Neurologic manifestations associated with hypothyroidism in four dogs. J Am Vet Med Assoc. 1988;192:1745–7.
- Rudas P, Ronai ZS, Bartha T. Thyroid hormone metabolism in the brain of domestic animals. Dom Anim Endocrinol. 2005;29:88–96.
- Higgins MA, Rossmeisl JH, Panciera DL. Hypothyroid associated central vestibular disease in ten dogs: 1999–2005. J Vet Intern Med. 2006;20:1363–9.
- Coates JR. Neurologic manifestations of hypothyroidism. Canine Pract. 1997;22:27–8.
- Jaggy A, Oliver JE, Ferguson DC. Neurological manifestations of hypothyroidism: a retrospective study of 29 dogs. J Vet Intern Med. 1994;8:328–36.
- Cuddon PA. Aquired canine peripheral neuropathies. Vet Clin North Am Small Anim Pract. 2002;32:207–49.
10. Cruz MW, Tendrich M, Vaisman M, Novis SA. Electroneuromyography and neuromuscular findings in 16 primary hypothyroidism patients. Arq Neuropsiquiatr. 1996;54:12–8.
- El-Salem K, Ammari F. Neurophysiological changes in neurologically asymptomatic hypothyroid patients: a prospective cohort study. J Clin Neurophysiol. 2006;23:568–72.
- Murray IPC, Simpson JA. Acroparaesthesia in myxoedema. A clinical and electromyographic study. Lancet. 1958;28:1360–3.
- Khedr EM, El Toony LF, Tarkhan MN, Abdella G. Peripheral and central nervous system alterations in hypothyroidism: electrophysiological findings. Neuropsychobiol. 2000;41:88–94.
- Quattrini A, Nemni R, Marchettini P, Fazio R, Iannaccone S, Corbo M, Canal N. Effect of hypothyroidism on rat peripheral nervous system. NeuroReport. 1993;4:499–502.
- Budsberg SC, Moore GE, Klappenhach K. Thyroxin-responsive unilateral forelimb lameness and generalized neuromuscular disease in four hypothyroid dogs. J Am Vet Med Assoc. 1993;11:1859–60.
- Suraniti AP, Gilardoni LR, Lial MGR, Echevarria M, Marcondes M. Hypothyroid associated polyneuropathy in dogs: report of six cases. Braz J Vet Res Anim Sci. 2008;45:284–8.
- Fors S. Neuromuscular manifestations of hypothyroidism in dogs. EJCAP. 2007;17:173–8.
- Indrieri RJ, Whalen LR, Cardinet GH, Holliday TA. Neuromuscular abnormalities associated with hypothyroidism and lymphocytic thyroiditis in three dogs. J Am Vet Med Assoc. 1987;190:544–8.
- Srikala D, Satish Kumar K, Tirumala Rao DS. Clinico-therapeutic management of thyroxine responsive polyneuropathies in dogs. Intas Polivet. 2011;12:96–9.
20, Cuddon PA. Electrodiagnosis in veterinary neurology: Electromyography, Nerve Conduction Studies and Evoked Responses. Colorado: Veterinary Specialists of Northhern Colorado; 2000.
- Kimura J. Electrodiagnosis in diseases of nerve and muscle: principles and practice. 3rd ed. Oxford: Oxford University Press; 2001.
- Walker TL, Redding RW, Braund KG. Motor nerve conduction velocity and latency in dog. Am J Vet Res. 1979;40:1433–9.
- Nebuchennykh M, Lseth S, Mellgren SI. Aspects of peripheral nerve involvement in patients with treated hypothyroidism. Eur J Neurol. 2010;17:67–72.
- Peterson ME, Melian C, Nichols R. Measurement of serum total thyroxine, triiodothyronine, free thyroxine, and thyrotropin concentrations for diagnosis of hypothyroidism in dogs. J Am Vet Med Assoc. 1997;211:1396–402.
- Kececi H, Degirmenci Y. Hormone replacement therapy in hypothyroidism and nerve conduction study. Clin Neurophysiol. 2006;36:79–83.
- Johnsen B, Fuglsang-Frederiksen A. Electrodiagnosis of polyneuropathy. Neurophysiol Clin. 2000;30:339–51.
- Rossmeisl JH. Resistance of the peripheral nervous system to the effects of chronic canine hypothyroidism. JVIM. 2010;24:875–81.
- Nemni R, Bottacchi E, Fazio R, Mamoli A, Corbo M, Camerlingo M, Galardi G, Erenbourg L, Canal N. Polyneuropathy in hypothyroidism: clinical, electrophysiological and morphological findings in four cases. J Neurol Neurosurg Psychiatry. 1987;50:1454–60.
- Thornton ARD, Jarvis SJ. Auditory brainstem response findings in hypothyroid and hyperthyroid disease. Clin Neurophysiol. 2008;119:786–90.
- Di Lorenzo L, Foggia L, Panza N, Calabrese MR, Motta G, Tranchino G, et al. Auditory brainstem response in thyroid diseases before and after therapy. Horm Res. 1995;43:200–5.
Источник: Acta Veterinaria Scandinavica (2016) 58:32. This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons license, and indicate if changes were made. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated.
СВМ № 5/2018