Э. С. Маилян
Паразитозы занимают первое место в патологии как среди домашних, прирученных, так и диких птиц. Пернатые хищники не являются исключением и являются обширным полем для изучения гельминтозов, разработки методов их диагностики, лечения и профилактики.
Паразитозы, и в частности гельминтозы, вызываемые различными видами нематод, трематод, цестод и скребней, занимают основное место в патологии птиц. Эндопаразитозы являются у них наиболее частой причиной расстройства аппетита и пищеварения. Отмечено, что у свободноживущих пернатых хищников частота гельминтной инвазии с субклиническим течением очень высока, причем 60% всех гельминтозов составляют нематодозы (Forbes N.A., 1996). При попадании в неволю вследствие неизбежного стресса заболевание, протекающее до этого латентно, проявляется клинически. Поэтому все отловленные птицы в обязательном порядке должны быть подвергнуты профилактической дегельминтизации или паразитологическому обследованию, включая обязательную микроскопию фекалий.
Smith A. (1993) провел прижизненное гельминтоовоскопическое исследование диких и содержащихся в неволе пернатых хищников: 115 особей, которые относятся к 15 видам отряда соколообразных (Falconiformes) и 102 особи, принадлежащие к 8 видам отряда совообразных (Strigiformes). Установлено, что степень поражения птиц различными гельминтами составила 62% для соколов и 68% для сов. Причем в обеих группах частота встречаемости паразитарной инвазии у диких птиц, находящихся на свободе, превышала таковую у особей, содержащихся в неволе (табл. 1).
Таблица 1. Паразиты, обнаруженные у диких и живущих в неволе хищных птиц (Smith A., 1993).
| Обследованные птицы | Зараженные | Нематоды | Трематоды | Цестоды | Скребни | |||||
| n | % | n | % | n | % | n | % | n | % | |
| Falconiformes | ||||||||||
| Дикие (n=71) | 50 | 70 | 42 | 59 | 33 | 46 | 3 | 4 | 1 | 1 |
| В неволе (n=44) | 12 | 27 | 12 | 27 | 4 | 9 | 0 | 0 | 0 | 0 |
| Всего (n=115) | 62 | 54 | 54 | 47 | 37 | 32 | 3 | 3 | 1 | 1 |
| Strigiformes | ||||||||||
| Дикие (n=72) | 61 | 85 | 58 | 81 | 26 | 36 | 5 | 7 | 4 | 6 |
| В неволе (n=30) | 7 | 23 | 6 | 20 | 2 | 7 | 1 | 3 | 0 | 0 |
| Всего (n=102) | 68 | 67 | 64 | 63 | 28 | 27 | 6 | 6 | 4 | 4 |
Согласно данным, собранным в соколином госпитале Deauville у 1526 пациентов (1999–2000), поступивших в клинику с различной патологией, было зарегистрировано 1185 случаев гельминтозов (табл. 2).
Таблица 2. Паразиты, обнаруженные при обследовании ловчих соколов в государстве Катар
(Маилян Э.С., Qatar, 2000)
| Паразиты | Число случаев | % |
| Гельминтозы: | ||
| Нематоды | 287 | 40,8 |
| Трематоды | 334 | |
| Цестоды | 1 | |
| Простейшие: | ||
| Трихомонады | 297 | 36,9 |
| Кокцидии | 266 | |
Следует обратить внимание, что заболевания пернатых хищников, вызываемые гельминтами, по частоте встречаемости среди регулярно диагностируемых паразитозов стоят на первом месте.
Ниже приводится краткое описание наиболее часто регистрируемых у хищных птиц гельминтозов, их возбудителей, а также методов диагностики, лечения и профилактики.
Класс Nematoda (круглые гельминты)
Подотряд Ascaridata
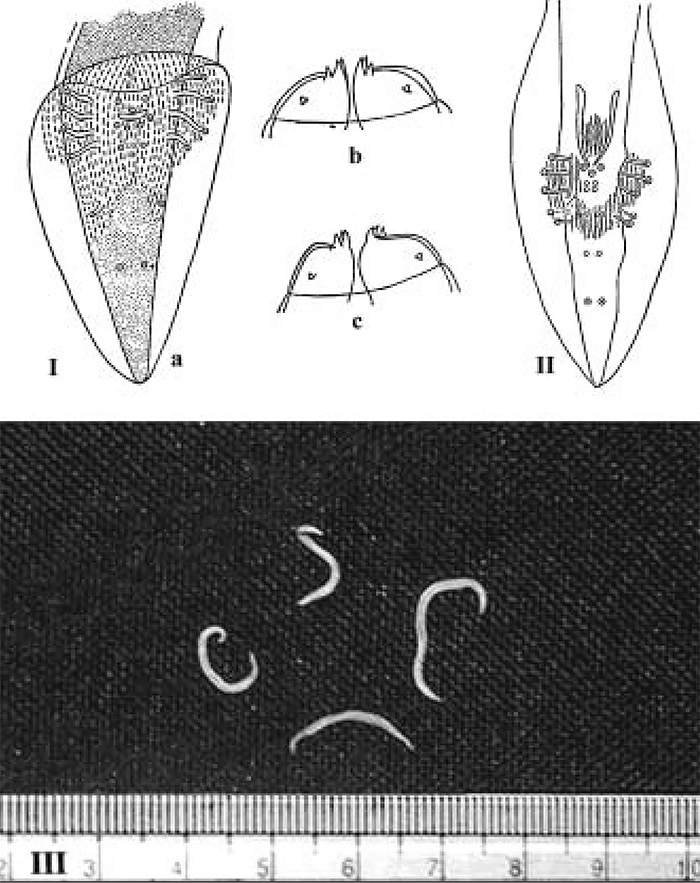
Род Ascaridia (рис. 1 – IIa, b, c) – наиболее часто встречаемые паразиты диких и содержащихся в неволе хищных птиц. Это объясняется наличием прямого цикла развития, когда заражение происходит при контакте здоровой птицы с пометом зараженной или подстилкой, где содержатся яйца паразита. Кроме того, яйца аскарид весьма устойчивы в окружающей среде и могут сохраняться в подстилке (почве) в течение нескольких месяцев. Попав в организм птицы, личинка покидает яйцо и внедряется в слизистую оболочку кишечника. После соответствующего периода развития она вновь проникает в просвет кишечника, где достигает половой зрелости через 5–6 недель.
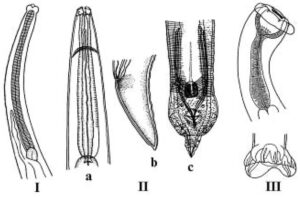 |
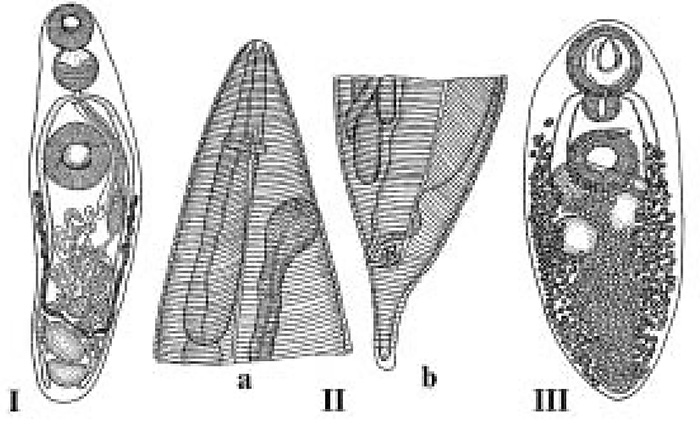
| Рисунок 1. Нематоды птиц (Дубинина М.Н., 1971): I – Porrocaecum angusticolle (передний конец тела с пищеводом); II – Ascaridia galli: a – передний конец тела с пищеводом; b – хвостовой конец самки; с – хвостовой конец самца. III – Syngamus trachea (самец: передний и задний концы тела). |
- Клинические признаки гельминтозов проявляются редко – только в случае высокой степени инвазии отмечают сонливость, анорексию, потерю веса и обтурацию кишечника вплоть до его разрыва (фото 1), особенно у молодых птиц. Иногда отмечают хромоту, по всей видимости, вызванную токсическим действием конечных продуктов обмена гельминта на организм хозяина.
-
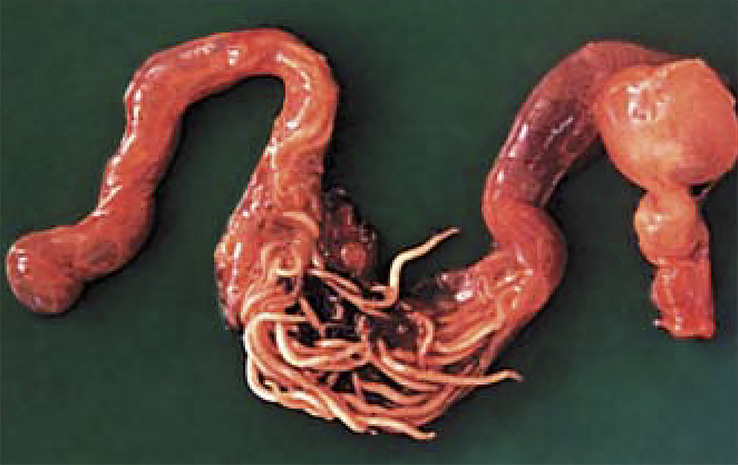
Фото 1. Высокая степень инвазии аскаридами может привести к полному разрыву кишечника (Heidenreich M., 1997).
Диагностика
Зачастую даже при наличии гельминтов в организме птицы при микроскопии фекалий яйца обнаружить не удается. Это объясняется довольно длинным препатентным периодом (5–6 недель), который необходим паразиту для достижения половой зрелости. Известны случаи отрыгивания яиц вместе с погадкой у ястребов-тетеревятников. Яйца гельминта обнаруживаются при микроскопическом исследовании фекалий (фото 2е).
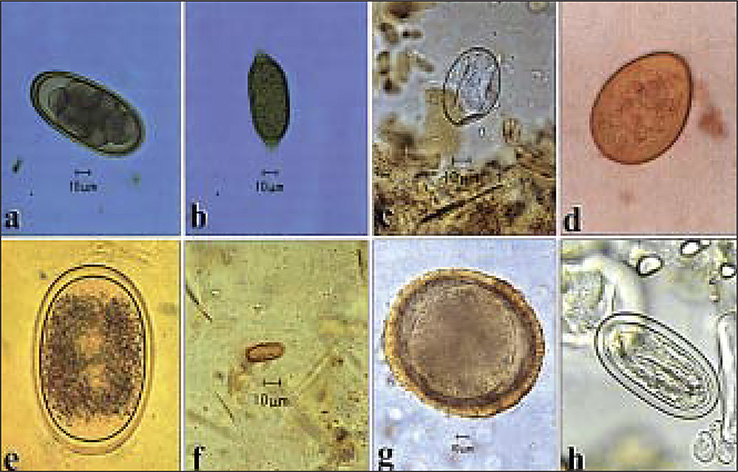 |
| Фото 2. Яйца паразитов (Heidenreich M., 1997): a – Syngamus spp.; b – Capillaria spp.; c – Serratospiculum spp.; d – Strigea falconis (Samour J., 2000); e – Ascaridia galli; f – Acanthocephala; g – Porrocaecum spp. h – Physaloptera spp. (Fox J.C., Oklahoma State University, 2002). |
Лечение (табл. 7)
Таблица 7. Дозы антигельминтиков, рекомендуемые для лечения хищных птиц по данным разных авторов.
| Класс паразита | Препарат | Схема лечения по данным авторов: | ||
| Smith S.A., 1993 | Heidenreich M., 1997 | Samour J.H., 2000 | ||
| Nematoda | Thiabendazole | 100 мг/кг п/о, повторно через 10–14 дней |
– | 250–500 мг/кг п/о, повторно через 10–14 дн.; 100 мг/кг 7–10 дней |
| Levamizole | 10–20 мг/кг п/о 2 дня | 40 мг/кг в/м или п/о | 10–20 мг/кг п/к однократно | |
| Ivermectine (Ivomec) | 0,4 мг/кг в/м, повторно через 3–4 недели; 200 мкг/кг п/о или в/м; 0,2 мл/кг в разведении 1:9 |
200 мкг/кг п/о в разведении 1:11 |
200 мг/кг п/о, п/к или в/м однократно | |
| Piperazine | 100 мг/кг п/о однократно | – | – | |
| Mebendazole | 50 мг/кг п/о, повторно через 10–14 дней |
– | 20 мг/кг п/о 14 дней | |
| Fenbendazole (Panacur) | 25 мг/кг п/о 3 дня | 25–50 мг/кг п/о 3–7 дней; 100 мг/кг однократно* | 20 мг/кг п/о 5–14 дней; 100 мг/кг п/о однократно |
|
| Benzimidazole | – | 25 мг/кг п/о, 3–5 дней; 100 мг/кг п/о однократно | – | |
| Albendazole | – | 25 мг/кг п/о 4–5 дней | – | |
| Cambendazole (Ascapilla) | – | – | 75 мг/кг п/о, 3 дня | |
| Pyrantel | 20 мг/кг п/о однократно | |||
| Trematoda | Rafoxanide | 10–15 мг/кг п/о однократно | 10–15 мг/кг п/о однократно | – |
| Praziquantel (Droncit) | 50 мг/кг п/о однократно | 10–15 мг/кг п/к или п/о, повторно через 7 дней | 5–10 мг/кг, п/к или п/о однократно | |
| Chlorsulon (Curatrem) | – | 20 мг/кг п/о 3 раза с интервалом в 2 недели | ||
| Fenbendazole (Panacur) | – | 20 мг/кг п/о 5–14 дней; 100 мг/кг п/о однократно | ||
| Cestoda | Praziquantel | 50 мг/кг п/к однократно | 5–10 мг/кг п/о или п/к, повторно через 14 дней | |
| Chlorsulon | – | 20 мг/кг п/о 3 раза с интервалом в 2 недели | ||
| * Назначение фенбендазола (fenbendazole или так называемый Panacur) в высоких дозах отрицательно сказывается на периферическом кровообращении и может привести к внезапной остановке роста нового оперения (особенно в период линьки) и его выпадению вследствие ишемии. При профилактике гельминтозов у грифов желательно избегать использования данного препарата (Heidenreich M., 1997). |
||||
Профилактика
Ввиду высокой устойчивости яиц в окружающей среде в условиях птичников рекомендуется частая уборка с тщательной очисткой пола от помета и регулярная профилактическая дача антигельминтиков.
Представители рода Porrocaecum встречаются реже и в основном у молодых птиц (рис. 1 – I. См. выше). Отдельные особи довольно крупные, обнаруживаются в мышечном желудке, а также в тонком и толстом отделах кишечника. Характерные для них крупные яйца с толстой оболочкой (фото 2g. См. выше), обнаруживаемые при микроскопии помета, достаточно устойчивы в окружающей среде.
Род Capillaria
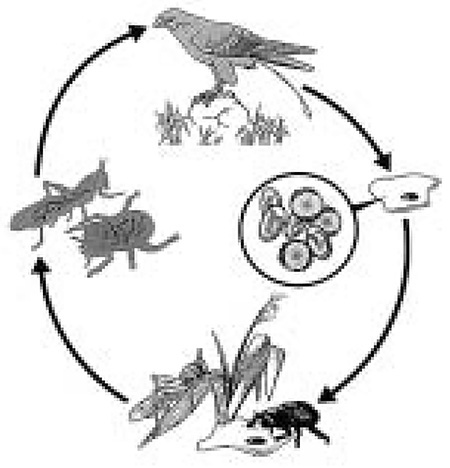
Капиллярии – обычно встречаемые паразиты у пернатых хищников. Это паразиты нитевидной формы длиной 1–5 см, нередко заселяют кишечник, пищевод и ротоглотку. Они могут иметь как прямой, так и непрямой цикл развития с участием промежуточных хозяев (табл. 3). Заражение прямое или при поедании промежуточных хозяев – моллюсков, земляных червей и т.д. (схема 1), а также через больную добычу (чайки, вороны). Препатентный период длится 3-4 недели.
Таблица 3. Гельминты рода Capillaria, паразитирующие у хищных птиц (Heidenreich M., 1997)
| Вид паразита | Цикл развития и промежуточный хозяин | Место паразитирования в организме |
| Eucoleus annulatus | Непрямой, дождевой червь | Ротоглотка и пищевод |
| Eucoleus contortus | Прямой | Ротоглотка и пищевод |
| Eucoleus dispar | Непрямой, дождевой червь | Пищевод |
| Capillaria falconis | Непрямой, дождевой червь | Тонкий кишечник |
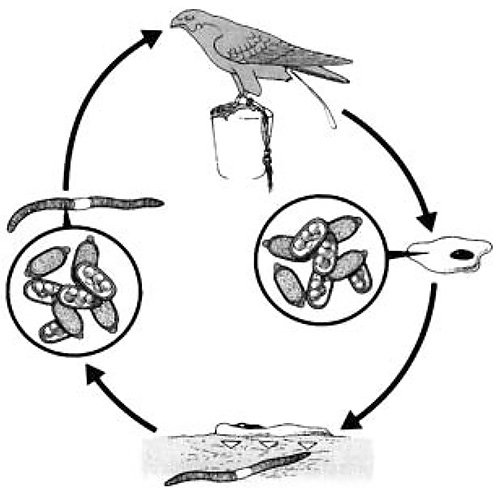 |
| Схема 1. Жизненный цикл нематод рода Capillaria требует участия переносчиков (векторов) – в данном случае дождевого червя, в теле которого не происходит дальнейшего развития паразита. Дефинитивным хозяином является птица, поедающая червей или насекомых (R. Gattung-Petith и A. Gattung у Heidenreich M., 1997). |
Клинические признаки
В зависимости от локализации различают 3 формы заболевания:
- Орофарингеальная (фото 3a) – отличается незначительным поражением слизистой оболочки с наличием легко отделяемых бледно-желтых отложений у основания языка и во внутренних уголках ротовой щели. В более серьезных случаях отмечают присутствие желтовато-коричневых гранулем значительных размеров (фото 3b), удаление которых может привести к сильному кровотечению. При последующем инфицировании таких участков возможно развитие абсцессов вплоть до вовлечения в процесс костей челюсти.
- Эзофагальная – трудно диагностируемая форма гельминтоза, особенно при отсутствии нарушений в ротовой полости. Иногда удается пальпировать характерное утолщение стенок пищевода. Очень часто данная форма обнаруживается на поздней стадии патологического процесса, иногда сопровождается разрывом кожного покрова в области шеи под воздействием быстро растущей гранулемы (фото 3с).
- Кишечная форма характерна воспалением и повреждением слизистой оболочки кишечника. Начальные признаки заболевания проявляются в виде анорексии, потери веса, диареи, слабости, что в свою очередь сказывается на качестве полета ловчих птиц вплоть до полного отказа.
Диагностика
Яйца паразита имеют форму лимона с «шапочками» на двух полюсах (фото 2b), которые обнаруживают при микроскопии фекалий, соскобов или смывов из ротовой полости, в пище и воде.
Орофарингеальную и эзофагальную формы необходимо дифференцировать от трихомоноза, кандидоза и другой схожей с данным заболеванием патологии.
Лечение (табл. 7)
Терапию необходимо сочетать с тщательной чисткой или заменой насеста и подстилки птицы.
Профилактика
В профилактику гельминтоза включают борьбу с переносчиками. Учитывая основную роль земляных червей в цикле развития и распространения капиллярий, необходимо исключить возможность контакта птицы с почвой и промежуточным хозяином:
– изолировать участок почвы вокруг места, где сидит птица (используют толстый слой гальки, гравия диаметром 2–3 мм, который насыпают поверх слоя извести) (схема 2);
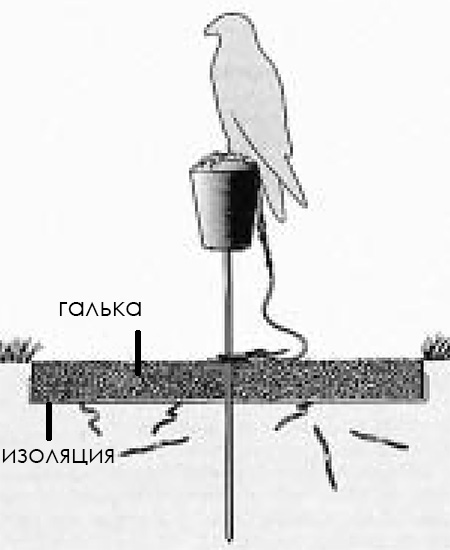 |
| Схема 2. Избежать контакта птицы с промежуточными хозяевами и переносчиками гельминтов можно, обеспечив ее чистым и сухим субстратом, изолированным от окружающей почвы (R.Gattung-Petith and A.Gattung, у Heidenreich M., 1997). |
– птицу предпочтительнее кормить с перчатки или на специальной платформе, избегая контакта корма с землей;
– ежедневно проводить тщательную чистку насестов и поилок.
Регулярное гельминтоовоскопическое исследование помета птицы задолго до появления клинических признаков позволяет обнаружить яйца паразита и своевременно начать лечение.
Подотряд Spirurata. Род Physaloptera
У хищных птиц встречаются следующие виды паразитарной инвазии: Physaloptera alata alata, Ph. acuticauda, Ph. subalata, Ph. reevesi и др.
Для завершения жизненного цикла паразита необходим беспозвоночный промежуточный хозяин.
Клинические признаки
Physaloptera alata alata встречается на слизистой верхней трети пищевода соколов, преобладает у Средиземноморского (рыжеголового) сокола (F. biarmicus) (Samour J. H., Маилян Э. С., 1999–2000). При этом отмечают анорексию, беспокойство, рвоту, потерю веса, изъязвление слизистой оболочки вплоть до гибели птицы.
Диагностика гельминтоза
Инвазия характеризуется анорексией и потерей веса.
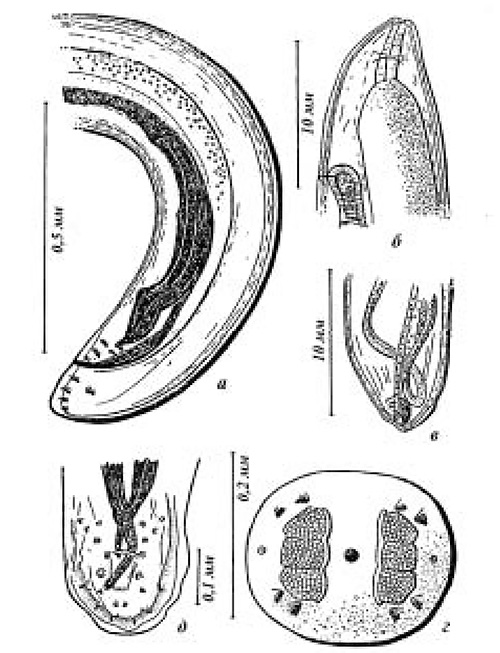
Диагностику осуществляют методом визуального обнаружения гельминтов при эндоскопии ротовой полости и просвета пищевода, а также идентификацией яиц паразита в мазке из слюны и фекалий. Размеры тела половозрелой особи достигают 35–40 мм в длину и 1–1,5 мм в диаметре (рис. 2). Яйца мелкие, овальной формы, с гладкой оболочкой и сформированной личинкой (фото 2h).
Лечение (табл. 7)
Терапия включает механическое удаление нематод из пищевода с последующим назначением антибиотиков (амоксициллин в дозе 50 мг/кг в течение 5 дней). В случае истощения и отказа птицы от корма в первые дни заболевания необходимо осуществлять принудительное кормление в сочетании с поддерживающей терапией. В качестве профилактики и для лечения используются те же препараты, что и при других нематодозах.
Другой представитель подотряда Habronema leptoptera обнаруживается в слизистой мышечного и железистого желудков, реже в пищеводе.
При микроскопии фекалий находят тонкостенные яйца с личинками.
Подотряд Filariata. Род Serratospiculum
Возбудители данного гельминтоза паразитируют в респираторном аппарате птиц, чаще встречаются у диких особей, отловленных в странах с теплым климатом (в основном в арабских странах): Serratospiculum seurati, S. tendo, S. chungi (рис. 3), S. turkestanikum, S. guttatum, S. kwangiensis, S. Congolensis, S. amaculata и др.
Цикл развития непрямой – с переносчиком (вектором), который может выступать в роли промежуточного хозяина: дождевые черви, насекомые – жуки, тараканы, кузнечики (схема 3). Заражение происходит при поедании переносчика с яйцами. У здоровых птиц патогенность гельминта невысока.
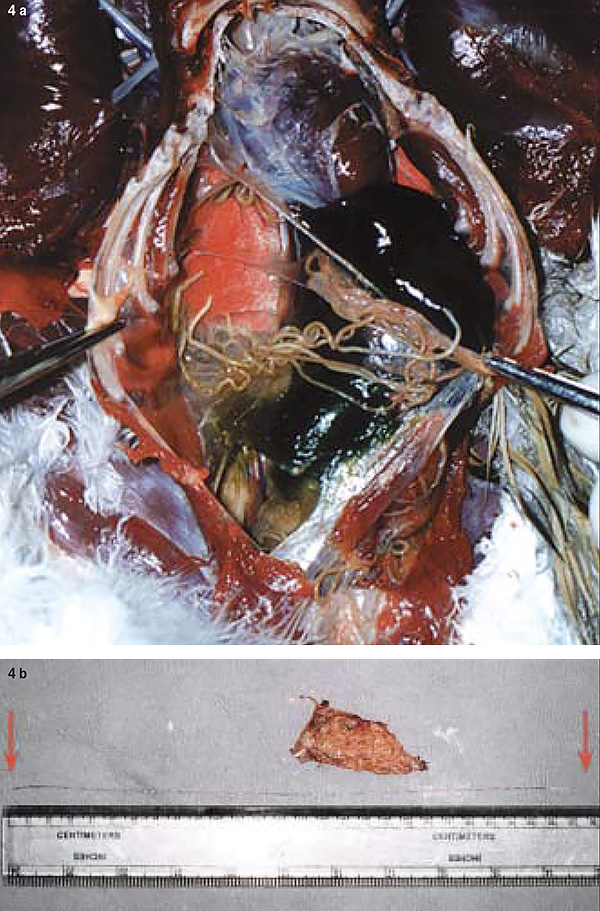
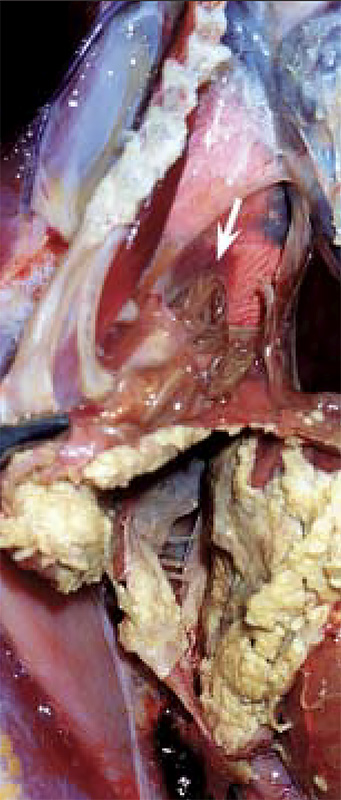
Иногда концентрация половозрелых особей гельминта в просвете воздухоносных мешков бывает настолько выраженной, что напоминает тарелку со спагетти (фото 4a, b).
При сопутствующей патологии возможно осложнение в виде аэросаккулита (фото 5). Больная птица может откашливать яйца гельминта в ротовую полость и снова заглатывать, после чего они попадают в желудочно-кишечный тракт и выделяются во внешнюю среду с пометом.
Клинические признаки гельминтоза
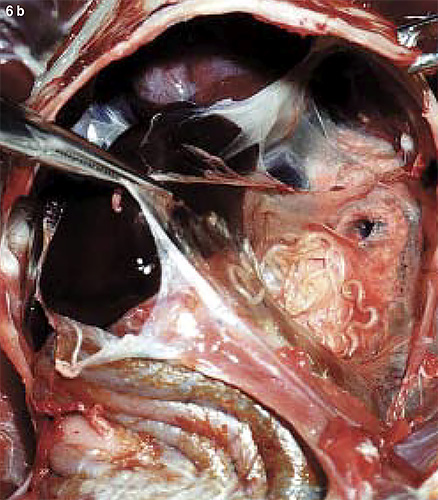
Проявляются на поздних стадиях паразитарной инвазии в форме истощения, анорексии, диспноэ, летаргического состояния (фото 6a, b), диареи, возможна рвота. Сильная степень инвазии, а также состояние стресса часто приводят к летальному исходу (Kocan and Gordon, 1976).
Диагностика
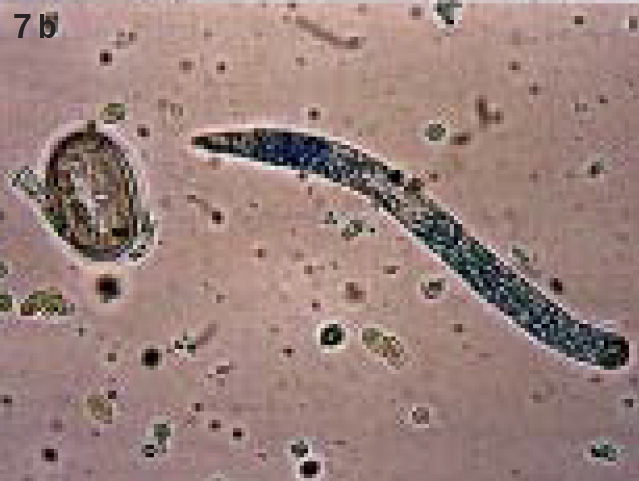
Тонкостенные яйца гельминта (фото 2c) с заключенными в них личинками обнаруживают при микроскопии фекалий, слюны и аспирируемого содержимого из полости воздухоносного мешка (фото 7a, b). Обнаружить самих паразитов в полостях воздухоносных мешков можно с помощью метода эндоскопии через каудальные грудные воздухоносные мешки. Манипуляцию проводят под общей анестезией по аналогии с определением пола у птиц.
Лечение затруднено по причине плохого кровоснабжения стенок воздухоносных мешков, где чаще всего паразитируют эти гельминты.
Антигельминтики (табл. 7) назначают в сочетании с антибиотикотерапией и последующим механическим удалением мертвых гельминтов с помощью эндоскопии (фото 8). В случае сильного истощения птицы необходим постоянный мониторинг ее состояния, принудительное кормление в сочетании с поддерживающей флюидо- и витаминотерапией. Наличие мертвых гельминтов в полости воздухоносных мешков может привести к летальному исходу для пациента.
Профилактика гельминтозов
В неволе инвазии можно избежать, исключив контакт птицы с переносчиками.
Среди других часто встречаемых представителей подотряда Filariata, поражающих респираторный аппарат пернатых хищников, следует отметить Diplotriaena falconis, Aprocta lissonema, относящихся к родам Splendidofilaria, Cardiofilaria, Chandlerella и Avioserpens (Samour J., 2000).
Подотряд Strongylata
Представитель – Syngamus trachea (Рис.1-III) у соколов встречается редко, чаще – у канюков и других падальщиков.
Этот кровососущий паразит отличается половым диморфизмом (самка 20 мм, самец – 6 мм длиной). Пара (самец и самка) постоянно находится в состоянии копуляции, что придает им Y-образную форму. Цикл развития прямой, однако, зачастую векторами могут служить земляные черви и улитки. Заражение птиц происходит при поедании переносчика с яйцами. Личинка мигрирует сначала в печень, а затем в трахею. Более крупная самка прикрепляется к слизистой оболочке трахеи, вызывая сильную воспалительную реакцию с образованием большого количества слизи. Яйца гельминта, по аналогии с Serratospiculum spp., откашливаются вместе со слизью через трахею в ротовую полость, откуда при проглатывании попадают в желудок, а затем и кишечник.
Клинические признаки появляются при значительной степени инвазии: хрипы в верхних отделах респираторного аппарата, диспноэ, характерное вытягивание шеи и «заглатывание» воздуха открытым ртом, частое чихание, потрясывание головой и кашель. Отличием от аспергиллеза является то, что не наблюдают брюшного типа дыхания. Питаясь кровью, паразит может вызвать серьезную анемию. Одной из причин смерти может быть асфиксия.
Диагностика гельминтоза
Постановку диагноза осуществляют на основании осмотра верхних отделов дыхательного аппарата. Гельминтов можно обнаружить невооруженным глазом или с помощью эндоскопа.
Препатентный период длится 3 недели, после чего характерные яйца паразита могут быть обнаружены при микроскопии фекалий (фото 2a).
Лечение (табл. 7)
Проводят этиотропное лечение (антигельминтики) в сочетании с антибиотикотерапией.
Профилактика гельминтоза
Использование бетонных полов в помещении, где содержится птица, поможет предотвратить распространение моллюсков и насекомых – промежуточных хозяев паразита.
Нематоды зрительного аппарата
Подвижное третье веко, конъюнктива и слезные каналы птиц также могут быть местом локализации различных гельминтов, среди которых у хищных птиц выделяют:
– Cyathostoma lari (Simpson and Harris, 1992) – локализуется под нижним веком и в периорбитальной области пустельги (F. tinnunculus), обыкновенного канюка (B. buteo) и ястреба-перепелятника (A. nisus).
– Phylophtalmus palpebrarum (рис. 4-I) паразитирует в орбитальной полости глаз.
– Thelaziella stereura (Рис. 4-IIa, b) персистирует под мигательной перепонкой и в протоках слезных желез.
Клинические признаки гельминтоза
Как правило, варьируют в зависимости от локализации паразита и степени инвазии (Simpson and Harris, 1992). Чаще всего проявляются в виде незначительной воспалительной реакции конъюнктивы, иногда отмечают локальный некроз окружающих тканей (Heidenreich M., 1997).
Лечение
Удаление паразита осуществляют хирургическим методом с последующей топической антибиотикотерапией.
Класс Trematoda
Трематоды (сосальщики) – мелкие паразиты (0,5-5 мм), для завершения жизненного цикла которых необходим один или несколько промежуточных хозяев. Преобладают в регионах с теплым климатом.
У пернатых хищников обнаруживают несколько видов паразитарной инвазии, вызываемых представителями данного класса (табл. 4).
Таблица 4. Трематоды, выделенные от хищных птиц (Heidenreich M., 1997).
| Трематода | Дефинитивный хозяин |
| Strigea falconis | Ястреб тетеревятник (Accipit gentilis) Обыкновенный канюк (Buteo buteo) Балобан (Falco cherrug) Сапсан (Falco peregrinus) |
| Clinostomum complanatum | Белоголовый орлан (Haliaaetus leucocephalus) |
| Neodisplostomum attenuatum | Обыкновенный канюк (Buteo buteo) |
| Opistorchis sp. | Болотный лунь (Circus aeruginosus) Полевой лунь (Circus cyaneus) |
| Pseudostrigea buteonis | Обыкновенный канюк (Buteo buteo) Черный коршун (M. korshun (migrans)) Скопа (Pandion haliaetus) |
| Cryptocotyle lingua | Белоголовый орлан (Haliaaetus leucocephalus) |
| Echinostomum goldi | Болотный лунь (Circus aeruginosus) |
| Diplostomum spathaceum | Скопа (Pandion haliaetus) |
Трематоды были выделены также из желчных протоков коршуна (Samedov, 1979) и американской пустельги (Shell, 1957).
Согласно результатам исследования, проведенного в Объединенных Арабских Эмиратах (Greenwood et al., 1984), гельминты этого класса были обнаружены у 71% обследованных балобанов (F. cherrug) и 46% сапсанов (F. peregrinus).
Яйца трематод попадают в окружающую среду с пометом и трансформируются в мирацидии, для дальнейшего развития которых необходим промежуточный хозяин – как правило, моллюски. В теле улитки мирацидии превращаются в церкарии и снова выделяются во внешнюю среду. Некоторые виды проходят через еще одну стадию – метацеркарии внутри второго промежуточного хозяина (черви, насекомые и др.). Жизненный цикл завершается после пропадания метацеркарий в организм дефинитивного (окончательного) хозяина, где паразит развивается в половозрелую особь.
Диагностика гельминтоза
При микроскопии нативного мазка из свежего помета обнаруживаются тонкостенные яйца с однополюсными «шапочками» (фото 2e). Довольно часто регистрируются крупные яйца Strigea falconis (фото 2d), инвазия которой в кишечнике птицы может достигать очень высокого уровня (Маилян Э.С., 1999-2000).
Клинические признаки
Как правило, трематоды не патогенны до тех пор, пока степень инвазии не достигнет определенного высокого уровня.
Болезнь в зависимости от вида сосальщика проявляется признаками поражения печени или кишечника. У хищных птиц чаще отмечают поражение тонкого отдела кишечника. В особо тяжелых случаях наблюдается диарея, угнетение вплоть до летального исхода пациента (при сильном поражении печени).
Лечение (табл. 7)
Профилактик данной паразитарной инвазии данного возбудителя, как и при сингамозе, включает меры, предупреждающие контакт птицы с промежуточными хозяевами гельминта.
Класс Cestoda
Цестоды (ленточные гельминты) – биогельминты, развиваются при помощи одного или двух промежуточных хозяев. Они хорошо адаптированы к организму дефинитивного хозяина, поэтому редко вызывают клинически выраженную болезнь. Гельминтозы обнаруживают у хищных птиц, импортированных из стран с теплым климатом.
Наиболее часто регистрируемые виды представлены в таблице 5.
Таблица 5. Цестоды, выделенные от хищных птиц (Heidenreich M., 1997).
| Цестода | Дефинитивный хозяин |
| Hymenolepis exilis | Кречет (Falco rusticolus) Индийский балобан (Лаггар, Falco jugger) |
| Plagiorchis elegans Plagiorchis maculosus (рис. 4-III) |
Кречет (Falco rusticolus) |
| Claotaenia spp. | Многие виды семейства Falconidae |
| Dileptididae | Ястреб тетеревятник (Accipit gentilis) |
Клинические признаки
Проявляются клинически редко и варьируют в зависимости от локализации паразита.
Диагностика
Сегменты стробил и яйца паразитов обнаруживаются при микроскопии фекалий методом последовательных промываний или флотации по Фюллеборну.
Лечение (см. табл. 7).
Класс Acantocephala (скребни)
Скребни (колючеголовые) – паразиты домашних, диких млекопитающих, птиц, рыб и человека.
Это раздельнополые биогельминты, цикл развития непрямой – с участием промежуточных хозяев (ракообразные, насекомые, моллюски).
Виды, обнаруживаемые у хищных птиц, приведены в таблице 6.
Таблица 6. Скребни, выделенные от хищных птиц (по Heidenreich M., 1997).
| Птица | Вид паразита |
| Степная пустельга (Cerchneis naumanni) | Centrorhynchus buteonis Centrorhynchus spinosus Mediorchynchus papillosus Mediorchynchus micracantus |
| Обыкновенная пустельга (C. Tinnunculus) | Centrorhynchus cylindraceus |
| Ястреб-перепелятник (Accipiter nisus) | |
| Сапсан (Falco peregrinus) | Centrorhynchus globocaudatus |
| Скопа (Pandion haliaetus) | Centrorhynchus milvus |
| Степной орел (Aquila rapax) | Centrorhynchus itatsinis |
| Черный коршун (Milvus korshun (migrans)) | Mediorchynchus micracantus Centrorhynchus erraticus |
| Болотный лунь (Circus aeruginosus) | Centrorhynchus teres |
| Полевой лунь (Circus cyaneus) | Centrorhynchus amphibius |
Согласно исследованиям, инвазия у пернатых хищников восточно-европейского региона достигает 20% (Касимов и Самедов, 1975).
Клинические признаки гельминтозов
Клинически болезнь практически не проявляется. Лишь в тяжелых случаях отмечают диарею и потерю веса.
Диагностика
Яйца паразитов с личинками обнаруживают при микроскопии фекалий (фото 2f). Гельминтоовоскопию проводят по методу последовательных смывов или путем использования флотационного способа с применением насыщенных растворов солей (по Фюллеборну). Посмертную диагностику осуществляют путем вскрытия кишечника и обнаружения возбудителя.
Лечение
Терапевтические дозы препаратов для хищных птиц не отработаны.
При лечении птиц, относящихся к другим видам, с успехом используют Fenbendazole в дозе 20 мг/кг 1 раз в день в течение 5 дней или 40 мг/кг 3 раза в день в течение 3 дней.
Заключение
Несмотря на многообразие гельминтов и признаков их персистенции в организме птицы, в борьбе с гельминтозами необходимы прежде всего строгое соблюдение профилактических мероприятий и своевременная диагностика с целью недопущения развития высокой степени инвазии или инфестации, при которых оказываемые методы лечения становятся неэффективными.
Учитывая, что различные паразитозы у птиц протекают, как правило, параллельно, необходимо уделять должное внимание вопросу их дифференциальной диагностики с использованием специальных методов лабораторного и клинического обследования.
Библиография:
1. Акбаев М.Ш.: Практикум по диагностике инвазионных болезней животных. М., Колос, 1994.
1. Дубинина М.Н.: Паразитологическое исследование птиц. Л., Наука, 1971.
2. Beynon PH, Forbes NA, Harcourt-Brown NH: Manual of Raptors, Pigeons and Waterfowl. BSAVA Ltd., Kingsley House, 1996. Pp. 142, 204.
3. Bougerol C. (1967) in: Cooper JE: Veterinary aspects of captive birds of prey. Standfast Press, Saul, Gloustershire, England, 1978.
4. Heidenreich M.: Birds of Prey: Medicine and management. UK, Blackwell Science, 1997. P. 131.
5. Kocan A.A., Gordon L.R.: Fatal air sac infection with Serratospiculum amaculata in a prairie falcon. Journal of the American Veterinary Association. 1976.
6. Morgan D.O. and Clapham PA: Some observations on gapeworm in poultry and game birds. Journal of Helminthology, №12, 1934. P. 267.
7. Murrey E. Fowler et. al.: Zoo and Wild Animal Medicine: Current Therapy 3. W.B. Sounders Company, 1993. Pp. 27-33, 164-171.
8. Redig PT et al., Raptor Biomedicine, Chiron Pub. Ltd. Keighley, West Yorkshire, England, 1993.
9. Samour J.H. Avian Medicine. Mosby-Harcourt Publishers Ltd., 2000. Pp. 231-244.
10. Samour J.H.: Parasites in Lanner Falcon. Falco. The Newsletter of the Middle East Falcon Research Group. Issue № 6, 2000. P. 19.
11. Samour J.H.: The Fahad bin Sultan Falcon Centre. ёFalco. The Newsletter of the Middle East Falcon Research Group. Issue № 14, 1999. p 4.
12. Simpson V.R. and Harris E.A.: Cyathostoma lavi (nematode) infection in birds of prey. Journal of Zoology. London, 1992. Pp 227, 655.
13. Shivaprasad H.L.: An Overview of Avian Pathology. California Veterinary Diagnostic Laboratory System, Fresno Branch, University of California, Davis 2789 South Orange AvenueFresno, CA, 1998.
14. Smith S.A.: Diagnosis and treatment of helminths in birds of prey. In: Redig PT et al., Raptor Biomedicine, Chiron Pub. Ltd. Keighley, West Yorkshire, England, 1993. Pp. 21-27.
СВМ № 1/2003