С. В. Коняев1, 2, 3, к. б. н.
Иллюстратор: В. А. Штурбабин
1 Ветеринарная лаборатория VetUnion, г. Москва.
2 Институт систематики и экологии животных СО РАН, г. Новосибирск.
3 Ветеринарная клиника «АС Вет», г. Новосибирск.
Гепатозооноз кошек — инвазия представителей семейства кошачьих, вызываемая простейшими рода гепатозоон, протекающая чаще всего бессимптомно.
Возбудители и их таксономия
Всего в мире описано более 340 видов гепатозоонов, из которых у кошек выявлено три вида, их систематическое положение и названия приводятся ниже.
Царство: Eukaryota.
Тип: Apicomplexa.
Класс: Conoidasida.
Отряд: Eucoccidiorida.
Подотряд: Adeleorina.
Семейство: Hepatozoidae.
Hepatozoon Miller, 1908.
Hepatozoon felis Patton, 1908.
Hepatozoon silvestris Hodziz et al., 2017.
Hepatozoon canis (James, 1905) Wenyon, 1926.
Представители семейства Hepatozoidae являются в большинстве своём паразитами рептилий и амфибий, обладающими двуххозяинным жизненным циклом, где окончательный хозяин — кровососущее членистоногое (комары, клещи и другие) либо пиявки, а промежуточный — позвоночное животное. Систематическое положение многих видов рода ещё не устоялось. Ревизия с применением молекулярно-генетических методов свидетельствует, что внутри рода всё ещё остаются неродственные между собой группы видов, каждая из которых может рассматриваться как самостоятельный род. Также не исключено, что и список видов, способных заражать кошек, будет пересмотрен. Предполагается, что такие виды, как Hepatozoon procyonis, описанные от енотов-полоскунов, и неопределённые до вида Hepatozoon sp. от рыжей рыси (Lynx rufus), могут являться причиной инвазии кошек в США [8].
Этимология и синонимия названий
Названия возбудителей гепатозооноза происходит от латинских слов hepato — печень, zoon — животное, felis — кошачий, silvestris — лесной (отсылка к латинскому названию хозяина Felis silvestris).
В части публикаций вид H. felis мог быть определён как Hepatozoon canis [8]. В ряде источников может упоминаться как: Haemogregarin felis-domesticae Patton, 1908; Hepatozoon felisdomesticae (Patton, 1908) Weyon, 1926; Leucocytozoon felis-domestici (Patton, 1908) Patton, 1908. Ещё сложнее определить синонимию для H. silvestris, однако авторы, описавшие этот вид, предполагают, что к нему может относиться часть находок, определённых как H. felis и H. canis у кошек.
История
Типовой вид рода Hepatozoon muris (Balfour, 1905) был описан от лабораторной крысы (Rattus norvegicus), а тремя годами позже был описан и Hepatozoon felis от домашней кошки в Индии. Второй вид этого рода, специализированный паразит кошек, описан в 2017 году в Боснии и Герцеговине от дикой европейской кошки [12]. Шизонты были впервые описаны в капиллярах в 1973 году У. Клопфером с соавторами (1973) при изучении миокарда кошек. Позднее вид был выявлен в Нигерии, Израиле, на Гаваях, Южной Африке [15; 14; 10; 20]. Молекулярно-генетические данные свидетельствуют о том, что в составе H. felis есть ещё один скрытый вид-двойник. Анализ последовательностей гена 18S демонстрирует наличие внутри вида трёх групп: от крупных кошачьих из Индии (леопард, азиатский лев, бенгальский тигр), от домашних кошек (Испания, Израиль) и диких лесных кошек (Босния и Герцеговина). Последние были выделены в отдельный вид — H. silvestris [12]. Таким образом, систематика этих видов может измениться в ближайшие годы. Выявленные в клещах H. felis из России были наиболее близки к последовательностям Hepatozoon sp. от азиатского льва [19]. Вместе с тем именно изоляты из Индии (типовой территории), скорее всего, являются истинным Hepatozoon felis sensu stricto, чем использованные для переописания вида образцы из Израиля [6].
 |
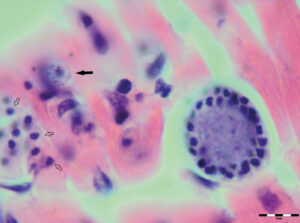 |
| Фото 1. Гамонт Hepatozoon felis в моноците ко-инфекция с гематропным микоплазмозом, окраска по Май-Грюнвальду — Гимзе. Масштаб — 10 мкм (по Beneth et al., 2013) | Фото 2. Микро- и макрошизонты Hepatozoon silvestris. Окраска гематоксилин-эозином. Масштаб — 10 мкм (по Hodžić et al., 2017)
|
Морфология
У кошек гепатозооны обнаруживаются в нейтрофилах в виде вытянутых овальных телец с округлыми полюсами, размером около 10×5 мкм. При окраске по Романовскому — Гимзе ядро тёмно окрашено, цитоплазма голубоватого цвета (рис. 1). На гистологических срезах миокарда могут быть обнаружены шизонты двух типов — с отдельно расположенными мерозоитами и с мерозоитами, расположенными по периферии (фото 1).
Меронт H. felis — размером больше чем у H. canis — 30,6×28,9 μm [4], обнаруживается в мышечных тканях (миокард, скелетная мускулатура), тогда как у собак меронты H. canis выявляются в костном мозге, лимфоузлах, паренхиматозных органах, но не в мышцах. Кроме того, меронты H. felis не образуют типичной для H. canis формы колеса. Гамонты H. felis в мазках крови встречаются в нейтрофилах и моноцитах, иногда сдавливая ядро клетки хозяина. Гамонты вытянутые, с видимой мембраной и ацентрично расположенным ядром. Некоторые из гамонтов содержат базофильно окрашенные гранулы. У H. felis ядро в основном округлое, тогда как у H. canis чаще подковообразное. В среднем гамонты H. felis короче (10,5 μm), чем H. canis (11 μm). H. felis менее заметен в лейкоцитах и часто укрыт материалом ядра клеток хозяина [6]. H. silvestris отличается от H. felis тем, что меронты имеют более тонкую капсулу, колёсообразные меронты содержат 20–30 мелких округлых микромерозоитов, тогда как у H. felis они прямо- и треугольные, крупные, перпендикулярно расположенные к стенке, в количестве 10–15 [12].
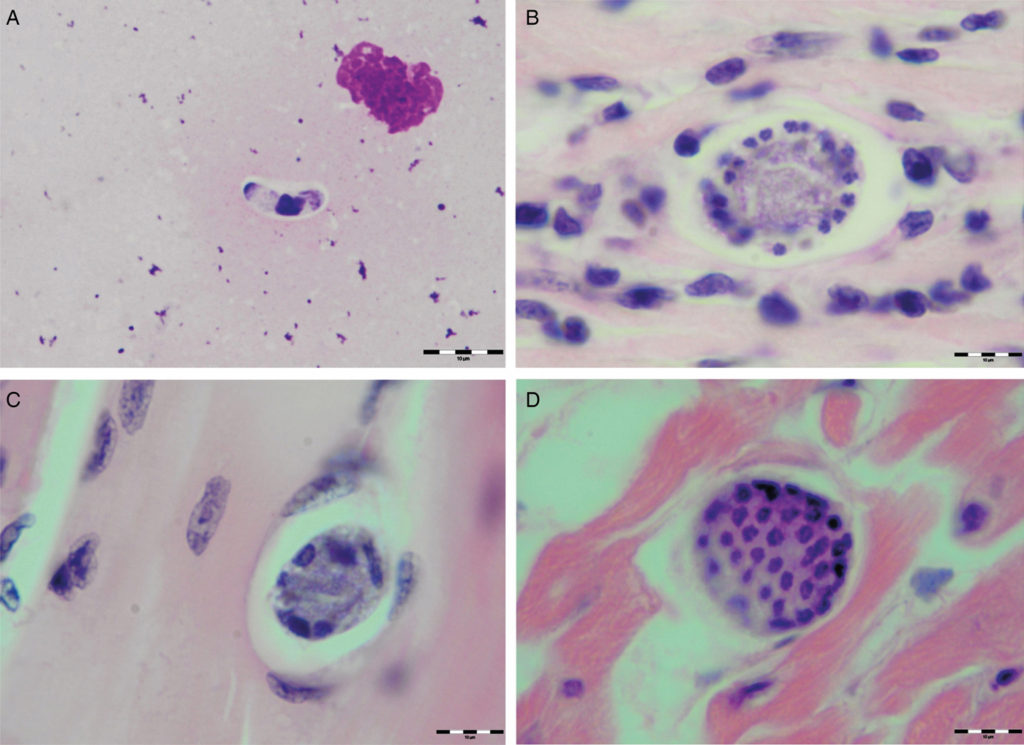 |
| Фото 3. Стадии развития Hepatozoon silvestris в миокарде и скелетной мускулатуре лесной кошки. (A) Внеклеточная стадия в мазке-отпечатке сердца, окраска по Май-Грюнвальду — Гимзе. Масштаб — 10 мкм. (B) Колесообразный меронот с микромерозоитами, окружающими центральную базально окрашенную массу, а также клеточный инфильтрат, окружающий меронт. Масштаб — 10 мкм. (C) Развивающийся меронт с расположенными по кругу макромерозоитами в скелетной мускулатуре. Масштаб — 20 мкм. (D) Зрелый меронт, заполненный множеством мерозоитов. (B–D) Окраска гематоксилин-эозином (по Hodžić et al., 2017) |
 |
|
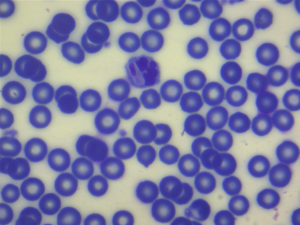
Фото 4. Гамонт Hepatozoon canis |
Жизненный цикл
Хозяевами H. felis являются домашние (Felis silvestris domestica) и дикие кошки (Felis silvestris silvestris), а также бенгальские кошки, львы, леопарды, тигры. H. silvestris на данный момент описан только у лесных и домашних кошек, а H. canis имеет более широкий спектр хозяев, включая представителей семейства собачьих, гиеновых. Далеко не во всех случаях видовая принадлежность гепатозоонов может быть установлена, поэтому мы приводим дополнительный список хозяев гепатозоон из семейства кошачьих, у которых они были выявлены, без указания вида паразитов: гепард, манул, ириомотская кошка, оцелот, онцилла, суматранская кошка, тигр, бенгальская кошка. В качестве окончательного хозяина выступают иксодовые клещи. Предполагается, что для H. silvestris окончательным хозяином служит Ixodes ricinus [12]. Rhipicephalus sanguneus описан как основной хозяин для Hepatozoon canis.
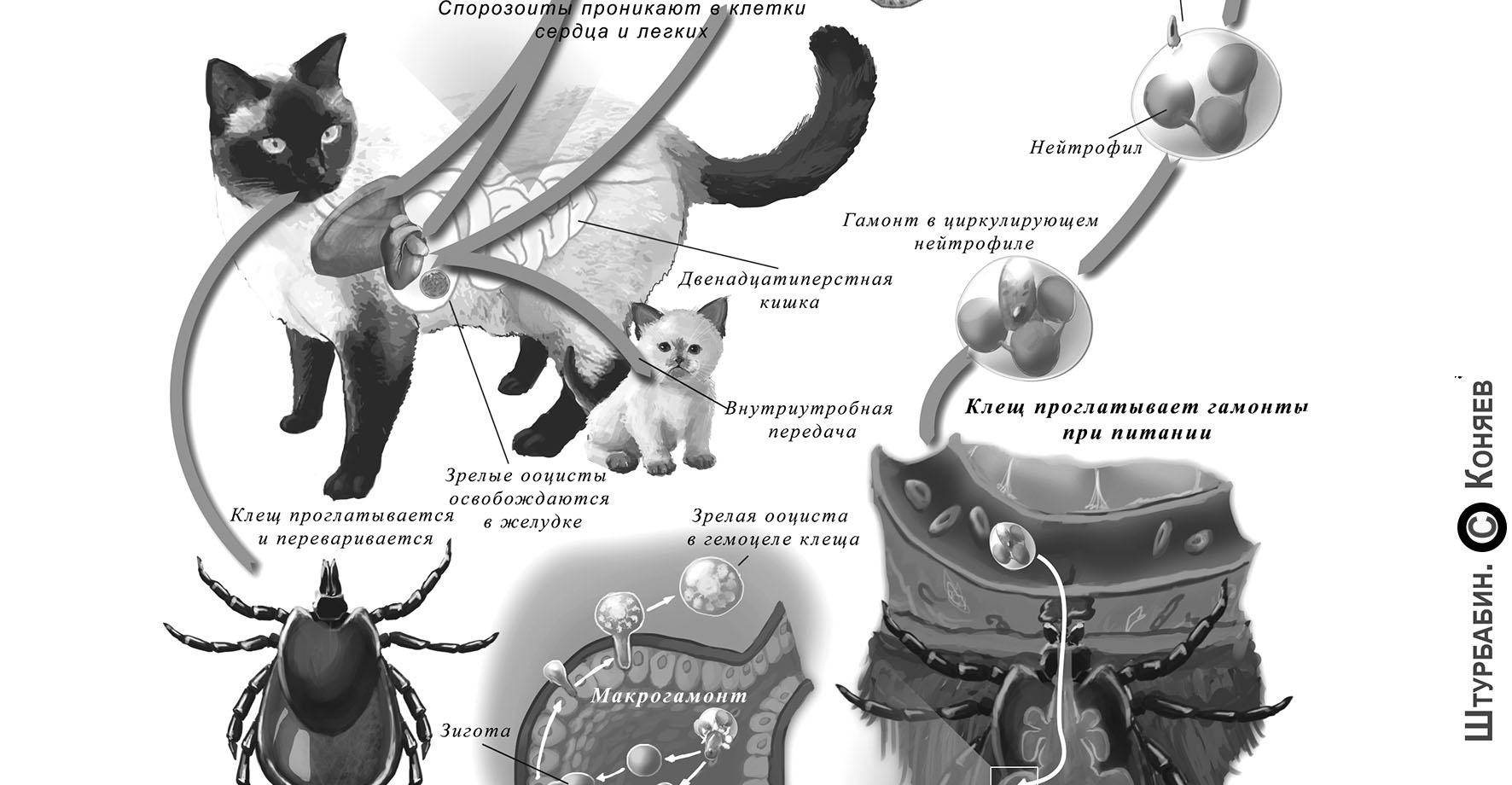
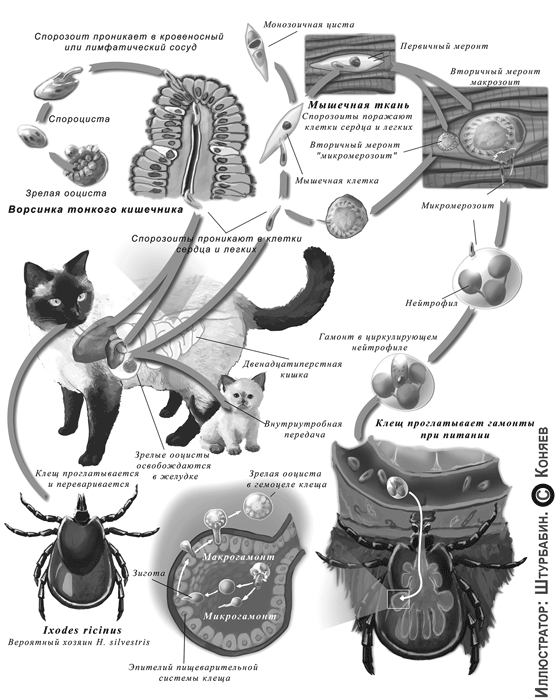
Жизненный цикл Hepatozoon felis и H. silvestris до сих пор детально не изучены, но предполагается, что он мало отличается от H. canis (рис. 1). Клещ заглатывает вместе с кровью гамонтов Hepatozoon, заключённых внутри моноцитов и нейтрофилов. В кишечнике клеща гамонты соединяются в сизигий. Сформировавшаяся ооциста проходит через стенку кишки клеща и выходит в полость тела или гемоцель. В результате споруляции образуется 30–50 спороцист, в каждой по 12–24 спорозоита. Спороцисты в клеще не изменяются, и спорозоиты из них не выходят. При поедании клеща спорозоиты высвобождаются из спороцист, проходят через стенку кишки нового хозяина и попадают через кровь или лимфу в организм животного. Развитие совершается в фагоцитах или в клетках эндотелия внутренних органов. В зависимости от размеров внутри клеток различают макро- и микромеронты (шизонты) (фото 2). Макромеронты продуцируют небольшое число мерозоитов и способны к новым раундам мерогонии. Микромеронты же, напротив, распадаются на множество мелких мерозоитов, которые в дальнейшем развиваются в гамонтов внутри лейкоцитов (фото 1). Меронты локализуются в клетках селезёнки, миокарда, лёгких и скелетных мышц (фото 3), а также в лимфатических узлах, костном мозгу [2]. В естественных условиях передача происходит при питании клеща, но также возможно инфицирование при инъекционном введении заражённого материала от собаки к собаке [9]. При исследовании плодов, полученных в ходе стерилизации, ДНК H. felis было выделено из образцов лёгких, амниотической жидкости и внутренних органов брюшной полости котят [6], что свидетельствует о возможности внутриутробной передачи возбудителя гепатозооноза. Кроме того, известно заражение через плаценту у H. felis [6] и H. canis, а также при поедании мяса заражённых животных у H. americanum.
Рисунок 1. Жизненный цикл Hepatozoon silvestris и H. felis
Эпизоотология
Гепатозооноз кошачьих, вызываемый предположительно H. felis, зарегистрирован в Индии, Таиланде, Корее, Японии, Испании, Италии, Франции, Израиле, Португалии, Танзании, Нигерии, США, Бразилии, Аргентине, зарегистрирован с 2016 года и в России. Вместе с тем, учитывая более широкое распространение Hepatozoon canis и способность этого вида заражать кошек, следует ожидать, что инвазия этим видом кошек может быть отмечена во многих других регионах. Hepatozoon canis в России зарегистрирован в Новороссийске, Саратовской области, Уфе, Грозном, Москве [1].
При исследовании кошек, поступивших для стерилизации в клиники Израиля, 36,2% (n=152) были позитивны в ПЦР по Hepatozoon spp., наибольшая корреляция заражённости наблюдалась с возрастом кошек, так большинство из них были в возрасте от 4 до 18 лет, в большинстве случаев выявлены H. Felis [6]. В подобном исследовании в Бангкоке (Таиланд) из 300 исследованных кошек 32% были заражены гепатозоонозом, вызванным H. canis [13]. В Бразилии при исследовании 200 образцов крови кошек только одна кошка была заражена Hepatozoon sp., наиболее близко кластеризующейся в филогенетическом анализе с Hepatozoon felis. A. Giannelli с соавторами описали случаи заражения кошек в Италии всеми тремя видами гепатозоон и описали первый случай заражения H. silvestris домашних кошек [11].
Клинические признаки и патогенез
Клинические проявления гепатозооноза встречаются по всей видимости крайне редко. Шизонты чаще всего обнаруживаются в тканях домашних кошек при вскрытии и гистологическом исследовании при других заболеваниях. Сообщалось о прогрессирующей потере веса, язвенном глоссите с гиперсаливацией, прерывистой анорексией и пирексией, прогрессирующей анемии и выделениях из носа и глаз [3].
Описан случай лимфоаденопатии и желтухи у кошки. Повышенное количество моноцитов с увеличением числа циркулирующих монобластов в периферической крови может привести к ошибочному диагнозу моноцитарного лейкоза, как произошло в одном из описанных случаев. У животного были обнаружены H. felis в печени. Тщательный поиск в мазках крови и костного мозга, исследование других тканей не выявили каких-либо других патогенов, что подтверждает возможное участие данного вида паразитов в развитии клинической картины [10].
Семь описанных случаев клинических проявлений гепатозооноза сочетались с вирусным иммунодефицитом и лейкозом кошек, гематотропными микоплазмозами [14]. У животных с меронтами Hepatozoon sp. в поперечно-полосатой мускулатуре отмечена повышенная активность креатинкиназы и лактодегидрогеназы в сыворотке [5; 17]. Меронты обнаруживаются в лёгких, поджелудочной железе, селезёнке, печени и лимфатических узлах. Вместе с тем гистологического подтверждения воспалительной реакции вокруг меронтов не было выявлено [5]. Напротив, при исследовании миокарда, селезёнки, лёгких кошек, заражённых H. silvestris, была обнаружена умеренная инфильтрация тканей лифоцитами, макрофагами и реже нейтрофилами и эозинофилами (фото 3).
Диагностика
При гепатозоонозе, вызываемом H. canis, у кошек паразитемия не выражена. Так, при исследовании 300 кошек только у 0,7% из них были выявлены гамонты в нейтрофилах и моноцитах, тогда как по ПЦР были положительны 32% этих животных [13]. При аналогичном исследовании в Израиле гамонты не были выявлены ни у одной из 100 исследованных кошек, при этом у 36% из них меронты были выявлены в миокарде.
В условиях клиники диагностика может быть осуществлена путём обнаружения гамонтов в крови (окрашенный мазок любым доступным красителем по Май-Грюнвальду, Романовскому — Гимзе и т. д.) (фото 1, 4). Однако чувствительность такого исследования крайне низка. Повысить чувствительность исследования можно путём получения концентрата белых клеток крови с помощью седиментации в гематокритном капилляре с последующей окраской выделенного слоя лейкоцитов (см. вставку 1). Данный метод полезен для диагностики многих трансмиссивных заболеваний кошек и собак. Полимеразная цепная реакция (ПЦР), направленная на поиск ДНК возбудителя, может быть значительно более чувствительна, однако праймеры должны быть рассчитаны на весь спектр видов заражающих кошек. Обнаружение гамонтов является достаточно показательным при исследовании крови, их сложно перепутать с другими объектами в силу их размеров. Однако отрицательные результаты микроскопии не позволяют исключать диагноз «гепатозооноз» из-за её низкой чувствительности.
Лечение
Нет опубликованных контролируемых исследований эффективности препаратов при гепатозоонозе кошек. Ожидается, что могут быть эффективны — доксициклин, имидокарб. Имеется только одно исследование, в котором применялся окситетрациклин 50 мг на 1 кг, 7 дней подряд, дважды в день, после единственного введения 2 мг на 1 кг примаквина, перорально. Данное лечение не было проверено в плане способности полностью элиминировать инвазию из организма кошки [20]. Данные о низкой эффективности лечения у собак позволяют предположить подобную ситуацию и у кошек. Применение большинства препаратов у собак приводит к медленному исчезновению гамонтов из периферической крови, улучшению состояния животных, но не избавляет полностью от паразитов. Вероятно, эффективными могут быть: клиндамицин, триметоприм/сульфадиазин, пириметамин и ряд современных противококцидийных препаратов при длительном применении (не менее 14 дней). Поддерживающее лечение может включать нестероидные противовоспалительные средства.
Профилактика
Сложно предложить эффективные меры профилактики гепатозооноза у домашних кошек, так как нет достаточной изученности жизненного цикла этих паразитов. Возможно, эффективным будет использование противоклещевых препаратов, прежде всего профилактирующих длительное нахождение клещей на кошках. Вместе с тем проглатывание клещей при вылизывании шерсти, транспланцентарное заражение, а также предполагаемое заражение при питании мясом инвазированных жертв, делают неэффективной такую профилактику у свободно живущих кошек.
Литература
- Коняев С.В., Акимов И.А., Фоменко Н.В., Иванов М.К. Случаи заражения собак Hepatozoon canis и Babesia gibsoni в России // Материалы II международного паразитологического симпозиума «Современные проблемы общей и частной паразитологии»
6–8 декабря 2017/ СПб., 2017. — Из-во ФГБУ ВО СПбГАВМ — С. 136–138. - Бейер Т.В. Протисты. Руководство по зоологии. Часть 2. Под ред. Алимова А.Ф., СПб., 2007. — 1144 с.
- Baneth G. Part 3. Feline babesiosis and hapatozoonosis // Parasitoses and vector borne diseases of cats. — France, 2015. — Imprimerie Ferreol. Ed.: F. Beugnet, L. Halos. — P. 234–241.
- Baneth G., Samish M., Shkap V. Life cycle of Hepatozoon canis (Apicomplexa: Adeleorina: hepatozoidae) in the tick Rhipicephalus sanguineus and domestic dog (Canis familiaris) // Journal of Parasitology, 2007. — Vol. 93. — P. 283–299.
- Baneth G., Aroch I., Tal N., Harrus S. Hepatozoon species infection in domestic cats: a retrospective study // Veterinary Parasitology, 1998. — № 79. — P. 123–133.
- Baneth G., Sheiner A., Eyal O., Hahn S., Beaufils J.P., Anug Y., Talmi-Frank D. Redescription of Hepatozoon felis (Apicomplexa: Hepatozoidae) based on phylogenetic analysis, tissue and blood form morphology, and possible transplacental transmission // Parasite and Vectors, 2013. — № 6. — P. 102.
- Beaufils J.P., Martin-Granel J., Jumelle P. Hepatozoon spp. parasitemia and feline leukemia virus infection in two cats // Feline Practice, 1998. — Vol. 26. — P. 10–13.
- Bowman D.D., Hendrix C.M., Lindsay D.S., Barr S.C. (Eds.) Feline Clinical Parasitology: 1st edition, Iowa State University Press, Blackwell Science Company, 2002, 469 p.
- Craig T.M., Smallwood J.E., Knauer K.W., McGrath J.P. Hepatozoon canis infection in dogs: clinical, radiographic, and hematologic findings. // J Am Vet Med Assoc., 1978. Oct 15;173(8):967–972.
- Ewing G.O. Granulematous cholangiohepatitis in a cat due to a protozoan parasite resembling Hepatozoon canis // Feline Practice, 1977. — № 7. — P. 37–40.
- Giannelli A., Latrofa M.S., Nachum-Biala Y., Hodi A., Greco G., Attanasi A., Annoscia G., Otranto D., Baneth G. Three different Hepatozoon species in domestic cats from southern Italy // Ticks and Tick Borne Diseases, 2017. — № 8(5). — P. 721–724.
- Hodi A., Ali A., Praovi S., Otranto D., Baneth G., Duscher G.G. Hepatozoon silvestris sp. nov.: morphological and molecular characterization of a new species of Hepatozoon (Adeleorina: Hepatozoidae) from the European wild cat (Felis silvestris silvestris) // Parasitology, 2017. — № 144(5). — P. 650–661.
- Jittapalapong S., Rungphisutthipongse O., Maruyama S., Schaefer J.J., Stich R.W. Detection of Hepatozoon canis in stray dogs and cats in Bangkok, Thailand // Ann NY Acad Sci, 2006. – № 1081. — P. 479–488.
- Klopfer U., Nobel T.A., Neuman F. Hepatozoon-like parasite (schizonts) in the myocardium of the domestic cat. Veterinary Pathology, 1973. — Vol. 10 — P. 185–190.
- Leeflang P., Ilemobade A.A. TIck-borne disease of domestic animals in northern Nigeria. Trop An Prod, 1977. — № 9. — P. 211–218.
- Patton W.S. The haemogregarines of mammals and reptiles // Parasitology, 1908. — Vol. 1. — P. 318–321.
- Perez R. R., Rubini A. S. and O'Dwyer L. H. The first report of Hepatozoon spp. (Apicomplexa, Hepatozoidae) in domestic cats from So Paulo state, Brazil // Parasitology Research, 2004 — Vol. 94. — P. 83–85.
- Tabar M.D., Altet L., Francino O., Sánchez A., Ferrer L., Roura X. Vector-borne infections in cats: Molecular study in Barcelona area (Spain) // Veterinary Parasitology, 2008. — № 151. — P. 332–336.
- Thomas L.H., Seryodkin I.V., Goodrich J.M., Miquelle D.G., Birtles R.J., Lewis J.C. Detection of Hepatozoon felis in Ticks Collected from Free-Ranging Amur Tigers (Panthera tigris altaica), Russian Far East, 2002–12 // Journal of Wildlife Diseases, 2016. — № 52(3). — P. 674–676.
- Van Amstel S. Hepatozoonose in n’ Kat. // Journal of South Africa Veterinary Medicine Association, 1979. — № 50. — P. 215–216.
- Vilhena H., Martnez-Daz V.L., Cardoso L., Vieira L., Altet L., Francino O., et al. Feline vector-borne pathogens in the north and centre of Portugal // Parasite and Vectors, 2013. — Vol. 6. — P. 99.
СВМ № 1/2018