С. Бюро, Жан-Гийом Гранд
Прогресс в развитии визуальной диагностики и хирургических методов позволяет предложить альтернативу консервативному лечению гиперкортицизма (синдрома Кушинга) у собак.
Гиперкортицизм, или синдром Кушинга — довольно частое явление у собак. Он характеризуется большим количеством вторичных клинических признаков, связанных с избыточной продукцией кортизола (J.M. Nanson, M.M. Van’t Hoofd, G. Voorhout et coll., 2005). Опухоль, ответственная за нарушения в 90% случаев, может иметь два происхождения:
– центральное, или гипофизарное (80–85% случаев), с избыточной секрецией адренокортикотропного гормона (АКТГ) гипофизом;
– периферическое, или надпочечниковое (15–20% случаев), с опухолью функционирующей в кортикальном слое (T.V. Axlund, E.N. Behrend, 2003; C.H. Brown, 2007).
Консервативное лечение гиперкортицизма требует пожизненного назначения препаратов под постоянным контролем. Оно может сопровождаться вторичными эффектами, рецидивами и не упреждает появления метастазов (таблица). Развитие методов визуальной диагностики и прогрессивные достижения в области ветеринарной хирургии за последние годы позволяют предложить метод хирургического вмешательства с достаточно благоприятным прогнозом в отличие от консервативной терапии.
Первый необходимый этап заключается в выявлении центральной или периферической природы данного заболевания. Такой подход определяет лечение и прогноз. Этот этап основан на гормональных тестах и методах визуальной диагностики.
Определение уровня поражения
Гормональный тест
Тест на торможение дексаметазоном
Дексаметазоновый тест основывается на отрицательной обратной связи в гипофизе, который в ответ на повышение глюкокортикостероидов в крови снижает секрецию АКТГ (T.V. Axlund, E.N. Behrend, 2003). В связи со снижением концентрации АКТГ, стимуляция коры надпочечников ослабевает, и кортизолемия снижается. Таким образом, через 4–8 часов после назначения дексаметазона содержание кортизола в крови достигает низкого уровня.
В случае гиперкортицизма центрального происхождения гипофиз резистентен к обратной связи. При низкой дозе дексаметазона секреция АКТГ продолжается и кортизолемия поддерживается. Назначение высокой дозы может преодолеть резистентность гипофиза, и выработка АКТГ уменьшится.
Когда мы имеем дело с периферическим нарушением, эндогенный АКТГ уже снижен из-за работающей обратной связи, так как уровень кортизола в крови высок. В этом случае назначение глюкокортикостероидов не оказывает эффекта на кортизолемию.
При проведении теста торможения высокой дозой дексаметазона, падение кортизола в крови ниже 30 нмоль/л или на 50% от исходной свидетельствует о центральном нарушении. Приблизительно в 30% случаев кортизолемия не снижается в связи с резистентностью гипофиза. Следовательно, в случае отсутствия снижения кортизола в крови невозможно прийти к заключению о центральной или периферической природе гиперкортицизма.
Количественное определение эндогенного АКТГ
Количественное определение эндогенного АКТГ не позволяет установить диагноз на гиперкортизолемию, потому что его содержание может соответствовать норме даже в случае гиперкортицизма (T.V. Axlund, E.N. Behrend, 2003). Когда мы имеем дело с центральным нарушением, концентрация АКТГ превышает норму в результате секреции его опухолью гипофиза.
Когда нарушение носит периферический характер, то эндогенная концентрация низкая из-за отрицательной обратной связи, влияющей на гипофиз. Однако при получении нормальных показателей содержания АКТГ в крови очень трудно прийти к заключению. Следует заметить, что этот количественный показатель определяется в 82–95% случаев (T.V. Axlund, E.N. Behrend, 2003).
Тест на стимуляцию АКТГ
Чувствительность теста на стимуляцию АКТГ при центральном гиперкортицизме составляет 87%, при периферическом — 61%. Кроме того, периферический гиперкортицизм, в 40% случаев невозможно диагностировать, используя лишь один тест на стимуляцию АКТГ.
Таблица. Основные лекарственные препараты, используемые для лечения гиперкортицизма
Визуальная диагностика
Рентгенографическое исследование
В ретроспективном исследовании из 94 случаев опухоли надпочечников по рентгенограмме были идентифицированы 50% по обнаружению кальцификации или за счёт непосредственной визуализации их в брюшной полости. Однако следует иметь в виду, что дискретная минерализация может развиваться у здоровых особей и что она также может быть связана с гиперкортицизмом центрального происхождения (T.V. Axlund, E.N. Be-hrend, 2003).
Эхографическое исследование
В случае центральной природы заболевания гипертрофия надпочечников на УЗИ брюшной полости носит билатеральный характер с однородной структурой. Иногда можно наблюдать лишь простое увеличение эхогенности (T.V. Axlund, E.N. Behrend, 2003). Надпочечник, размер которого превышает 1,0 см по его короткой и 2,4 см по длинной осям, рассматривают как гипертрофированный. Эхография более информативно для диагностики опухоли надпочечника, чем рентгенография. Но интерпретировать результаты исследования правого надпочечника сложнее, потому что асимметрия может иметь место и в норме. В исследовании, включающем 79 новообразований надпочечников, 86% из них идентифицированы с помощью эхографа.
Надпочечник может быть гипо-, изо- и гиперэхогенным с элементами минерализации, геморрагии или просто гипертрофированным. Обнаружение билатерального образования может вызвать затруднение в предположении центральной природы заболевания.
Провести дифференциацию между аденомой и аденокарциномой при использовании эхографического исследования невозможно, даже несмотря на то что основным признаком, позволяющим установить карциному, является инвазирование новообразования в каудальную полую вену (T.V. Axlund, E.N. Behrend, 2003). Чувствительность и специфичность предлагаемого метода с целью выявления тромбов в каудальной полой вене, согласно ретроспективным исследованиям, составили 80% и 90% соответственно (A.E. Kiles, E.C. Feldman, H.E.V. De Cock et coll., 2003).
Компьютерное томоденситометрическое (КТ) исследование
Томоденситометрия — это чувствительный метод, который позволяет достаточно легко сравнить надпочечники (T.V. Axlund, E.N. Behrend, 2003). Тем не менее, гипертрофия не всегда очевидна. Доброкачественную опухоль надпочечника невозможно отличить от злокачественной, и инвазия сосудами идентифицируется с трудом. Основное применение КТ заключается в оценке области гипофиза. Детализация визуальной картины, необходимая перед хирургическим вмешательством, позволяет окончательно установить локализацию железы.
Обычное томоденситометрическое исследование позволяет получить визуальное изображение через двухмиллиметровую толщину с прохождением питуитарной (гипофизарной) зоны до и после инъекции йод-содержащего контрастного вещества (R.H. Van der Vlugt-Meijer, B.P. Meij, T.S. Van den Ingh et coll., 2003). Опухоль располагается в турецком седле и вытягивается дорсально. Выявление минерализации можно рассматривать как признак опухоли. Макроаденому в основном хорошо определяют по умеренной фиксации контрастного вещества (фото 10). Маленькие опухоли или микроаденомы не визуализируются. Отсутствие новообразования не говорит о том, что нарушение носит не центральный характер. Чувст-вительность сканера КТ составляет 5,0–6,0 мм, а разрешающая способность магнито-резонансного томографа (МРТ) равна 3,0 мм (G.W. Niebauer, 2002).
Динамичное томоденситометрическое исследование позволяет получить серию поперечных срезов на одном и том же участке (центральная часть железы) во время и после введения контрастного продукта. После усиления контрастирования внутренних сонных артерий и артериальной дуги на периферии железы в первую очередь происходит усиление контрастности центральной части гипофиза (или нейрогипофизе) с последующим её усилением в периферийной части (или аденогипофизе) и одновременным снижением при этом контрастности нейрогипофиза.
Общее смещение, искажение или изменение этой последовательности способствуют выявлению места локализации повреждения типа микроаденомы (G.W. Niebauer, 2002; R.H. Van der Vlugt-Meijer, B.P. Meij, T.S. Van den Ingh et coll., 2003). Повреждения гипофиза выявляются при динамическом исследовании в 82% случаев (R.H. Van der Vlugt-Meijer, B.P. Meij, T.S. Van den Ingh et coll., 2003).
 |
|
| Фото 1. Томоденситометрическое исследование гипофиза у американского стаффордширского терьера в возрасте 7 лет, который имеет гипофизарную макроаденому. Образование (стрелка), располагающееся в центре турецкого седла, умеренно фиксированное контрастным веществом | Фото 2. Вид во время операции у собаки. Правый надпочечник (А) близок к каудальной полой вене (В), его капсула иногда соединяется со стенкой вены. Правая почка отмечена буквой С |
 |
|
| Фото 3. Во время операции, проводимой у собаки, следует обратить внимание на аденому левого надпочечника (стрелки) | |
 |
 |
| Фото 4. Вид во время операции у собаки. Диафрагмально-брюшная вена (D), наличие поверхности левого надпочечника (Е) | Фото 5. Вид во время операции у собаки. Левый надпочечник извлечен (стрелка). Наложение сосудистых клипс оказывает точную услугу для обеспечения гемостаза множества дорсальных сосудов |
Удаление надпочечника
Унилатеральная функционирующая опухоль надпочечника может быть удалена хирургически с надеждой на выздоровление.
Предоперационный период
В предоперационный период назначают кортикостероиды (дексаметазон 0,1–0,2 мг/кг или преднизолон 1–2 мг/кг в/в для создания индукции в постоперационной фазе), что позволяет упредить фатальный гипокортицизм через 12–18 часов после проведения операции. Противоположная железа атрофирована, и требуется несколько недель, чтобы она восстановилась. Преднизолон (Megasolone) назначают в физиологической дозе или 0,25 мг/кг перорально один раз в день в течение 1–2 недель. Затем дозу постепенно снижают до состояния, при котором тест на стимуляцию АКТГ показывает адекватную секрецию кортизола. Нормальное образование гормона наблюдают в основном через 3–9 недель после проведения операции (C.G. Brown, T.K. Graves, 2007).
Для упреждения выраженного риска инфицирования в состоянии гиперкортицизма также назначают антибиотик широкого спектра (например, цефалексин).
Метод хирургического вмешательства
При выборе доступа вентральный предпочтительнее паралюмбального, потому что он позволяет осуществить полную ревизию брюшной полости. Надпочечники располагаются ретроперитонеально и краниомедиально по отношению к краниальному полюсу почек. Каждый из них укрыт тонкой капсулой и жиром. Правый надпочечник ближе к каудальной полой вене, и его капсула иногда сращена с венозной стенкой (фото 2). У некоторых собак для визуализации надпочечника, нужно отвести правую полую вену. Это необходимо осуществлять с осторожностью в связи с риском вторичной редукции (уменьшения диаметра) возвратной вены. Левая железа более объёмная и незначительно смещена каудально. Диафрагмально-абдоминальную вену, располагающуюся на вентральной поверхности железы, изолируют, лигируют и удаляют (фото 3 и 4). Железу иссекают постепенно. Облегчению манипуляции может способствовать наложение на нее лигатуры. Надпочечник имеет выраженную васкуляризацию в его дорсальной поверхности, начиная от ветвей аорты и диафрагмы, от почечной артерии и дополнительных её ответвлений, поясницы и диафрагмально-обдоминального отделов, что вызывает не-обходимость применения электрического скальпеля и клипс для сосудов (фото 5). Вена правого надпочечника соединяется с полой, в то время как левого — с левой веной надпочечника. Вены надпочечников могут также соединяться с диафрагмально-брюшными венами. В случае инвазии почки практикуется нефрэктомия. Примерно в 11–20% случаев в полой вене обнаруживают тромб (T.V. Axlund, E.N. Behrend, 2003; A.E. Kiles, E.C. Feldman, H.E.V. De Cock et coll., 2003). Это не является противопоказанием к проведению хирургической операции и, согласно исследованиям, не ведет к увеличению смертности при хирургическом вмешательстве в области сосудов. В большинстве случаев тромбы образуются в диафрагмально-брюшной вене, а затем попадают в каудальную. В этом случае венотомию осуществляют в месте обтурации диафрагмально-брюшной вены с временной окклюзией каудальной полой. Также на каудальную полую вену тангенциально можно поместить зажим Сатинского и резецировать захваченную часть, накладывая сразу же шов из полипропиленовой нити (диаметр 5/0). Окклюзия полой вены должна быть как можно короче в связи с выраженным снижением венозного оттока.
Осложнения
К потенциальным осложнениям относятся кровотечения, гипоадренокорти-цизм, тромбоэмболия, панкреатит, медленное рубцевание и сепсис (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001; A.E. Kyles, E.C. Feldman, H.E.V. De Cock et coll., 2003). В ранних работах сообщается о том, что смертность составляет 60%. В последних исследованиях, включавших 21 и 40 случаев, согласно ретроспективным данным, общая смертность во время операции составила 19% и 21% соответственно (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001; A.E. Kyles, E.C. Feldman, H.E.V. De Cock et coll., 2003). Две собаки, которые были подвержены частичной резекции, имели хорошую выживаемость в течение длительного времени под врачебным контролем. Опухоль, которая не может быть извлечена в связи со сложностью и наличием метастазов, не должна быть поводом для эвтаназии (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001).
Прогноз
Рецидивы возникают редко. Несмотря на хирургическое вмешательство, прогноз очень хороший (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001). Проведенная операция уменьшает риск развития вторичного диабета, связанного с гиперкортицизмом, и улучшает его контроль. Медиана выживаемости 18 собак, страдавших карциномой надпочечников, составила 778 дней. Общее число метастазов составило 5% с момента операции и 14% — на более длительный период времени (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001). Возраст животного, размер и природа новообразования не влияют на выживаемость (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001). Дополнительная консервативная терапия (митотан или трилостан) необходимы, когда опухоль не может быть извлечена полностью или когда имеются метастазы, сопровождающиеся клиническими симптомами (C.A. Anderson, S.J. Brichard, B.E. Powers et coll., 2001).
Гипофизэктомия
Роль хирурга в коррекции гиперкортицизма центрального происхождения в гуманитарной медицине определена чётко. В 1914 году нейрохирург Харви Кушинг разработал удобный в техническом отношении транссфеноидальный доступ к гипофизу (T.W. Axlund, E.N. Bechrend, 2003). У человека чаще рекомендуют проводить селективное удаление опухоли гипофиза. Первую гипофизэктомию у собаки с целью дальнейшего лечения провели в 1968 году в университете Утрехта (G.W. Niebauer, 2002). В следующее десятилетие было прооперировано 28 собак, что говорит об оптимально допустимом методе лечения. Тем не менее технические сложности возникают в основном у брахи- и долихоцефальных пород собак. Железа у собак в зависимости от формы головы имеет разную позицию в турецком седле клиновидной кости. Для того чтобы её выделить, костных реперов недостаточно. Тем не менее, точную локализацию железы знать крайне необходимо, потому что она охвачена кавернозными венозными синусами, окружной артерией головного мозга, глазодвигательными, трохлеарными и отводящими нервами, а также офтальмической ветвью тройничного нерва (рисунок). Методы визуальной диагностики (КТ и МРТ) позволяют точно определить локализацию гипофиза и, следовательно, объективно определить хирургический доступ (C.G. Brown, T.K. Graves, 2007; G.W. Niebauer, 2002). В большинстве публикаций фигурируют методы начального транссфеноидального доступа с более или менее слабыми вариациями (T.W. Axlund, E.N. Bechrend, 2003). Другие методы хирургического вмешательства основаны на промежуточном ростральном, парамедианном вентральном и внутричерепном транстемпоральном доступах, которые уже описаны (G.W. Niebauer, 2002).

Показания
Аденомы чаще встречаются в дистальной и промежуточной частях гипофиза. Аденокарциномы выявляются менее чем в 3% случаев. В 80–90% случаев появление нарушений провоцируется микроаденомой (до 1,0 см). Однако большая часть терапевтического воздействия направлена на надпочечники, а не опухоль. Большинство повреждений эволюционирует вторично в микроаденомы, что вызывает компрессию прилегающих неврогенных структур (10–30%) (C.G. Brown, T.K. Graves, 2007; G.W. Niebauer, 2002). Неврологические симптомы появляются в зависимости от скорости роста новообразования и его размера (наиболее часто диаметром 8–10 мм) и носят слабо выраженный специфический характер: слабость, дезориентация, нарушение зрительной способности.
В связи с вышесказанным могут быть следующие показания:
– гипофиз нормального размера (гиперкортицизм центрального генеза составляет 25%) — благоприятное условие к проведению операции;
– новообразования в гипофизе, локализующиеся в турецком седле (50%), имеют благоприятный прогноз после проведения операции;
– новообразование гипофиза, вытягивающееся дорсально, упираясь в нервные структуры и проявляющееся наличием или отсутствием неврологических симптомов (25%), считают крайне неблагоприятным условием к проведению операции. При таких нарушениях прогноз слабый (T.W. Axlund, E.N. Bechrend, 2003; J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005; G.W. Niebauer, 2002).
 |
Фото 6. Для проведения гипофизэктомии через трансфеноидальный доступ. Собака помещена в грудное положение. Пасть максимально открыта |
 |
Фото 7. Вид проведения операции по гипофизэктомии у собаки. Первый этап хирургического вмешательства основан на продольном разрезе мягкого неба. Его каудальная часть предохраняется, чтобы облегчить её ушивание и ограничить риск постоперационного разрыва |
 |
Фото 8. Томоденситометрическое исследование гипофиза, проведенное в постоперационный период после гипофизэктомии. Отмечается остеотомия клиновидной кости (стрелка), центрированная и открытая, размером от 5 до 6 мм |
 |
|
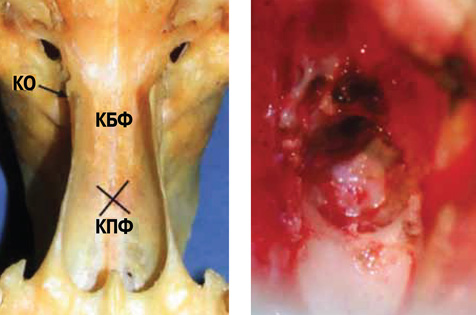
| Фото 9. Костные реперы для проведения остеотомии. КО: крючковидный отросток; КБФ: кость базисфеноид; КПФ: кость пресфеноид; Крест: участок приблизительного проведения остеотомии | Фото 10. Вид во время операции гипофизэктомии у собаки. Гипофиз располагается рострально и окружен кавернозным синусом в форме подковы, открытой спереди |
Метод хирургической операции
Собаку помещают в грудное положение, голову поднимают с максимально открытой пастью (фото 6) (B.P. Mej, 1998). Турецкое седло — это впадина на дорсальной части тела клиновидной кости, формирующей основание черепа. Чтобы получить к нему доступ, осуществляют продольный разрез мягкого неба, а затем отводят мукопериост. Остеотомия клиновидной кости разной толщины должна быть чётко центрированной и обеспечивающей открытие в ней отверстия на 5–6 мм (фото 8). Она осуществляют с помощью пневматического мотора, оснащенного фрезой (вибрационной пилой). Основным техническим препятствием для определения участка остеотомии является вариабельность костных реперов:
– крючковидные отростки, каудальная часть крыловидной кости более или менее пальпируются, так как покрыты мышцами, напрягающими мягкое небо, и мукопериостом. Линия, которая соединяет их каудальную вершину, определяет точку медианной линии клиновидной кости, соответствующую участку остеотомии около 5 мм;
– соединение между телом основной клиновидной кости (базисфеноидом) и телом предклиновидной кости (пресфеноидом) соответствует центру турец-кого седла в основном в мезенцефальной (средней) части, но оно не всегда идентифицируется, и тогда можно прощупать лишь один костный гребень;
– эмиссарная (отводная) вена в случае её присутствия также может служить репером. Следуя за ней, проходя через клиновидную кость, можно достичь центра гипофиза (фото 9) (G.W. Niebauer, 2002).
Применение метода томоденситометрии в срезе и в объёмном измерении (3D) позволяет провести точный замер расстояния от реперов, что помогает локализовать зону остеотомии. После проведения остеотомии кавернозные синусы в форме подковы визуализируются вокруг гипофиза, который имеет розоватый цвет (фото 10). Эти синусы не должны быть повреждены, так как имеется риск фатального кровотечения, потому что они не коллабируются (не спадаются). Внутренние сонные артерии располагаются латерально. Ростральный внутрикавернозный синус локализуется каудально по отношению к гипофизу, то есть между железой и дорсальной частью турецкого седла. Таким образом, неполный сосудистый круг и составляет ростральную часть между железой и зрительным перекрестом. В дальнейшем на протяжении вмешательства расширение участка в этом направлении невозможно. Кровотечение в процессе гипофизэктомии минимально и может исходить от сосудов гипофиза. Железа с её вентральной поверхности укрыта твердой оболоч-кой, и субдуральное пространство содержит спинномозговую жидкость, которая вытекает при рассечении твердой оболочки. При этом гипофиз имеет тенденцию к частичной протрузии. Его извлекают постепенно с помощью атравматического пинцета (T.W. Axlund, E.N. Bechrend, 2003; G.W. Niebauer, 2002). Из-за размера этой железы удаление лишь одной аденомы весьма иллюзорно, поэтому приходится проводить резекцию всего участка. Остеотомированную щель закрывают кусочком мышечной ткани, взятой от твердого неба, и фиксируют подшиванием её к периосту или посредством наложения костного воска.
Послеоперационный период
В этом периоде назначают антибиотики широкого спектра действия (например, цефалексин), потому что такое вмешательство не позволяет избежать контаминации.
Поддержание здоровья собаки осуществляют за счёт:
– гормонов щитовидной железы (из расчёта 0,02 мг/кг/сутки перорально) в связи с супрессией соматотропного гормона (СТГ), стимулируя таким образом щитовидную железу на протяжении всей жизни животного (T.W. Axlund, E.N. Bechrend, 2003; G.W. Niebauer, 2002);
– синтетического антидиуретического гормона, такого как десмопрессин (1 капля в конъюнктивальный мешок 2–3 раза в сутки), потому что удалена задняя часть гипофиза и выделение антидиуретического гормона прекращается. Транзиторная гипернатриемия часто имеет место при лечении и объясняется резистентностью к десмопрессину. В связи с этим в послеоперационнном периоде рекомендуется осуществлять инфузию раствором, обедненным натрием (NaCl 0,45% с декстрозой 2,5%) (J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005). Вазопрессин синтезируется в гипоталамусе и перетекает в нейрогипофиз, таким образом, функция антидиуретического гормона восстанавливается за счёт центральной части гипоталамуса, и, следовательно, дополнительного назначения его на длительный период не требуется. В 80% случаев концентрация вазопрессина нормализуется в течение двух недель после проведения операции (T.W. Axlund, E.N. Bechrend, 2003; J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005; G.W. Niebauer, 2002);
– кортикостероидов (преднизолон перорально из расчёта 0,2 мг/кг/сутки), которые чаще всего применяют на протяжении всей жизни животного.
Тем не менее полностью удалить железу очень трудно, поэтому остаются все типы клеток, но функционируют только те, которые продуцируют АКТГ (B.P. Meij, J.A. Mol, M.M. Bevers et coll., 1997). Иногда оставшиеся клетки приводят к рецидиву заболевания, но именно они позволяют избежать длительного (пожизненного) назначения глюкокортикостероидов (G.W. Niebauer, 2002).
Поддержание концентрации гормона роста, или соматотропного гормона (СТГ), для взрослой особи необязательно. Собака становится стерильной в связи с прекращением образования лютеинизирующего (ЛГ) и фолликуло-стимулирующего (ФСГ) гормонов (T.W. Axlund, E.N. Bechrend, 2003; G.W. Niebauer, 2002). Гистоморфологический анализ гипофиза позволяет сделать наиболее точный прогноз. Что касается прогноза в отношении редко встречающихся аденокарцином, которые изначально можно спутать с микроаденомой, то он неблагоприятный.
Осложнения
В течение гипофизэктомии и в послеоперационном периоде можно наблюдать некоторые осложнения (G.W. Niebauer, 2002).
Возможно развитие сухого кератоконъюнктивита (СКК). Его диагностируют с помощью теста Ширмера в послеоперационном периоде, и в большинстве случаев СКК рассасывается. Чаще всего снижение продукции слезы наблюдают в левом глазу. Возможно, это связано с тем, что хирург-правша имеет тенденцию отклонять свою фрезу влево по отношению к голове собаки. Предлагается несколько объяснений этого осложнения (J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005):
– травматическое или ишемическое повреждение нервов слезной железы;
– повреждение крыловидно-небного ганглия в связи с длительной компрессией нижнечелюстных венечных отростков в ретробульбарной области при трансоральном доступе. Степень открытия пасти и вероятность возникновения сухого кератоконъюнктивита по мере приобретения хирургом опыта снижаются;
– повреждение крыловидно-небного нерва, который располагается каудо-рострально по отношению к клиновидной кости, при удалении мукопе-риоста в каудальной части крючковидного отростка;
Ещё одним осложнением может быть миозит жевательной мышцы вследст-вие длительного открытия пасти во время операции.
На второй и четвертый день может возникнуть расхождение краев постоперационной раны мягкого неба. В связи с этим шов должен быть выполнен в два этажа.
При повреждении сосудистых структур возникают кровотечения.
Прогноз
Признаки гиперкортицизма исчезают через несколько недель (G.W. Niebauer, 2002). Самое крупное исследование, проведенное на собаках, включает 150 случаев. По его результатам:
– 8% смертности во время операции и в течение месяца после её проведения по причине кровотечения, эмболии, гипернатриемии, кислотно-кетонового диабета или пневмонии;
– 9% особей остаются в состоянии гиперкортицизма;
– ремиссия достигнута в 84,6% случаев, при этом три четверти пациентов не дали рецидивов; медиана выживаемости составила 28 месяцев; у 4 пациентов отмечался рецидив с медианой выживаемости 18,3 месяца (J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005).
Сравнение с консервативной терапией
Из большинства факторов, которые влияют на выбор лечения, главными считают следующие: стоимость, предпочтение владельцев и простота выполнения. С экономической точки зрения хирургическое вмешательство более дорогостоящее за короткий период времени по отношению к консервативной терапии, но дешевле в средней и длительной перспективе. Что касается длительности курса лечения, то митотан назначают только два или три раза в неделю, в то время как трилостан как дополнительное средство после гипофизэктомии — ежедневно. Безопасность лечения также учитывается.
Применение трилостана может привести к внезапной смерти, так же как и хирургическое вмешательство, во время которого собака может умереть. Кетоконазол очень эффективен в связи с его множественной ферментативной ингибирующей функцией и способностью устранять секрецию АКТГ, тем не менее его действие на собаку никогда по-настоящему не изучали (C.H. Brown, 2007).
В двух исследованиях, проведенных на 11 и 78 собаках, леченых трилостаном, ремиссия полиурополидипсии была достигнута соответственно в 100% и 70% случаев с изолированным нарушением кож-ного покрова в 82% и 62% случаев. В другом исследовании, проведенном в 78 клинических случаях, было показано, что медиана выживаемости у 26 собак составила 549 дней.
Тем не менее, на сегодняшний день не имеется достаточных данных ретро-спективного исследования, чтобы провести объективное сравнение между трилостаном и гипофизэктомией.
Эффективность митотана со временем снижается, и неудач достаточно много (C.H. Brown, 2007). Исследования, проведенные на 129 собаках, показали ремиссию в 86% случаях, но у 39% наблюдали рецидивы. В исследованиях 54 клинических случаев синдрома Кушинга у собак, леченных митотаном, трехлетняя выживаемость составила 45%.
В другом исследовании, проведенном на 200 особях с гиперкортицизмом центрального генеза, трехлетняя выживаемость составила 30%.
Надо отметить, что успешные исходы гипофизэктомии составили 65% про-тив 61% животных, леченых митотаном (J.M. Hanson, M.M. Van't Hoofd, G. Voorhout et coll., 2005). Однако долгосрочный прогноз после проведения гипофизэктомии значительно лучше:
– через 1 год 90% прооперированных животных чувствуют себя нормально;
– через 2 года более 80% прооперированных собак остаются живыми;
– через 3 года 61% собак, леченных митотаном, остается в живых против 72% перенесших гипофизэктомию, 44% собак, леченых консервативно, не имеют клинических признаков в сравнении с 66% прооперированных животных.
Что касается опухолей надпочечников, то принятие решения о хирургиче-ском вмешательстве, в связи с деликатностью самой процедуры, часто остается сдержанным. Развитие метода гипофизэктомии при гиперкортицизме центрального генеза происходит медленными темпами в связи с необходимостью использования специальной визуализации и сложностями по уточнению анатомической локализации железы. Однако после успешного преодоления этих сложностей, гипофизэктомия пред-ставляется наиболее логичный подход к решению проблемы. Послеоперационный период протекает нетяжело, и прогноз на длительный период времени благоприятный.
Основные положения
— Более чем в 80% случаев гиперкортицизм имеет гипофизарную природу.
— Томоденситометрическое исследование является необходимым мето-дом для того, чтобы определить более точно локализацию и размер новообразования.
— Правый надпочечник располагается ближе к каудальной полой вене.
— После проведения гипофизэктомии собака на протяжении всей жизни получает гормоны щитовидной железы и кортикостероиды.
СВМ № 5/2010