Екатерина Андреева, врач-терапевт, Ветеринарная клиника неврологии, травматологии и интенсивной терапии, Санкт-Петербург
Список сокращений: АД — артериальное давление; АКТГ — адренокортикотропный гормон; АЛТ — аланинаминотрансфераза; в/в — внутривенно; ЖКТ — желудочно-кишечный тракт; ЛП — левая почка; ОПП — острое повреждение почек; ОРИТ — отделение реанимации и интенсивной терапии; ОЦК — объём циркулирующей крови; ПП — правая почка; ПЦР — полимеразная цепная реакция; РААС — ренин-ангиотензин-альдостероновая система; РМА — реакция микроагглютинации; УЗИ — ультразвуковое исследование; УЗ — ультразвуковой; ЦНС — центральная нервная система; ЩФ — щелочная фосфатаза; ЭГ — этиленгликоль.
Вступление
Острое поражение почек — проблема, с которой регулярно сталкивается ветеринарный врач общей практики. Эта патология нередко становится дилеммой для клинициста, так как далеко не всегда удаётся установить первопричину заболевания. Тяжесть заболевания и отсутствие чёткого понимания развития патологического процесса нередко приводят к неудачам в лечении пациентов с острым повреждением почек. В данной статье описана одна из относительно нередко встречающихся патологий эндокринной системы, способная маскироваться под многие болезни, в том числе под острое поражение почек.
Описание случая
Вид животного: собака.
Пол: самец.
Порода: немецкая овчарка.
Возраст: 2 года.
Вес: 22 кг.
Условия содержания: свободный выгул, собака живёт на базе по ремонту авиатехники.
Кормление: натуральное кормление (овёс, говядина, курица).
Вакцинальный статус: вакцинирован около 1,5 года назад.
Обработки от эктопаразитов: нет.
Ранее перенесённые заболевания: нет.
Ранее перенесённые травмы: нет.
Ранее перенесённые операции: нет.
Анамнез
На приём поступила собака с резким ухудшением состояния в течение последних двух дней (выраженная вялость, снижение аппетита). Четыре дня назад появилась перемежающаяся диарея, была однократная рвота. День назад владельцы обратились в другую клинику, где была проведена внутривенная инфузия раствора NaCl 0,9% и 5% глюкозы в объёме 500 мл. Последнее мочеиспускание — около 20 часов назад.
Собака живёт на открытой территории. На участке могла подобрать всё что угодно. Есть доступ к машинному маслу. Доступ к этиленгликолю владельцы считают маловероятным. Есть доступ к открытым водоёмам. Возможен укус змеи, клеща. Со слов работников, недалеко от базы травили собак.
За 6 часов до приёма были сданы анализы крови.
| Показатель | Результат | Референсные значения |
| АЛТ | 206 МЕ/л | до 80 МЕ/л |
| АСТ | 443 МЕ/л | до 60 МЕ/л |
| Креатинин | 626 мкмоль/л | до 120 мкмоль/л |
| Мочевина | 48 мкмоль/л | до 8 мкмоль/л |
| Креатинкиназа | 14729 МЕ/л | до 500 МЕ/л |
| Натрий | 129 ммоль/л | от 144 ммоль/л |
| Калий | 10 ммоль/л | до 5,3 ммоль/л |
| Хлор | 100 ммоль/л | от 109 ммоль/л |
| Фосфор | 4,7 ммоль/л | до 2,0 ммоль/л |
| Гематокрит | 56% | до 54% |
| Лейкоциты | 26×109/л | до 17×109/л |
Данные первичного осмотра
Температура 37,0°. Положение тела — вынужденное лежачее. Упитанность — ниже среднего. Видимые слизистые оболочки — розовые, сухие. Скорость наполнения капилляров — более 2 сек. Подкожные лимфоузлы не увеличены. При пальпации брюшная стенка была мягкая, безболезненная. Аускультация: тоны сердца ясные, патологических шумов не выявлено. Тургор кожи сохранён. Ротовая полость: без особенностей. На градуснике — тёмный кал, который не оставляет на бумаге следов крови.
На первичном приёме было проведено УЗИ брюшной полости, которое продемонстрировало признаки острого поражения почек, острого гепатита (рис. 1).
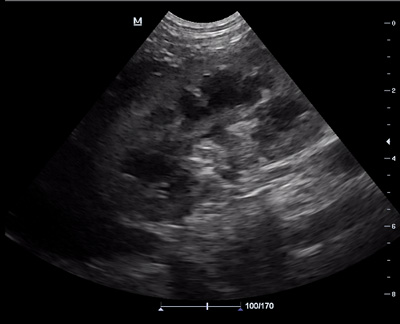 |
| Рис. 1. УЗ-картина правой почки |
Заключение УЗИ брюшной полости:
— УЗ-картина почек: размеры почек не изменены, правая: 55×35×31 мм, левая: 57×37×32 мм. Контуры почек ровные, чёткие. Кортико-медуллярная граница сохранена. Эхогенность коркового слоя повышена. Полостные системы обеих почек не расширены, мочеточники не визуализируются. Такая картина может соответствовать острому нефриту.
— УЗ-картина печени: размеры печени не изменены, печень не выходит за край рёберной дуги. Контуры печени ровные, чёткие. Паренхима мелкозернистая, однородная, не содержит очаговых образований. Эхогенность паренхимы снижена. Сосудистый рисунок печени не изменён, не обеднён, портальная вена — 8,9 мм. Желчные протоки не уплотнены, не расширены. Такая картина может соответствовать острому гепатиту.
— УЗИ желчного пузыря патологии не выявило. Пузырь среднего наполнения. Стенки не утолщены (1,0 мм), не уплотнены. В полости пузыря — анэхогенное содержимое. Пузырный проток не расширен.
Исходя из данных анамнеза, клинических признаков, результатов анализов крови и УЗИ был поставлен предположительный диагноз: острое повреждение почек (ОПП), сопровождающееся олигоанурией.
Рассматривались следующие возможные диагнозы:
— отравление нефротоксичными препаратами;
— лептоспироз;
— векторные инфекции (менее вероятны, так как отсутствовали данные о поражении соответствующих органов, помимо почек, а также для них не характерно такое резкое появление клинических признаков).
Для дифференциации была проведена дополнительная диагностика:
- Уровень глюкозы крови: 2,0 ммоль/л.
- АД (левая грудная конечность): ср. 80/45 мм рт. ст.
- Общий анализ мочи (моча взята цистоцентезом): плотность мочи 0,016, рН 5,5. Осадок: конгломераты кристаллов оксалата кальция моногидрата в умеренном количестве, единичные кристаллы оксалата кальция дигидрата, восковидные цилиндры от 0 до 1 в поле зрения. Элементы мочевого осадка окрашены желчными пигментами.
- Определение соотношения концентраций белка и креатинина в моче — 0,73 (моча взята цистоцентезом).
- Определение концентрации С-реактивного белка (в пределах нормы).
Диагностика лептоспироза включала:
- ПЦР мочи — отрицательная.
- ПЦР крови — отрицательная.
- РМА — отрицательная.
По причине наличия олигоанурии было принято решение оправить пациента в специализированную клинику для проведения гемодиализа.
Предварительно была проведена стабилизация уровня давления и глюкозы. Для этого были применены:
— Глюкоза 20% в/в болюсно 20 мл.
— Стерофундин изотонический в/в инфузия с постоянной скоростью 500 мл.
— Допамин в/в инфузия с постоянной скоростью 5 мкг/кг/мин.
После стабилизации уровень АД составлял в среднем 120/80 мм рт. ст., уровень глюкозы крови 4,0 ммоль/л. После 6 часов пребывания в клинике объём мочи в мочевом пузыре, согласно контрольному УЗИ, не изменился, что свидетельствовало об олигоанурии.
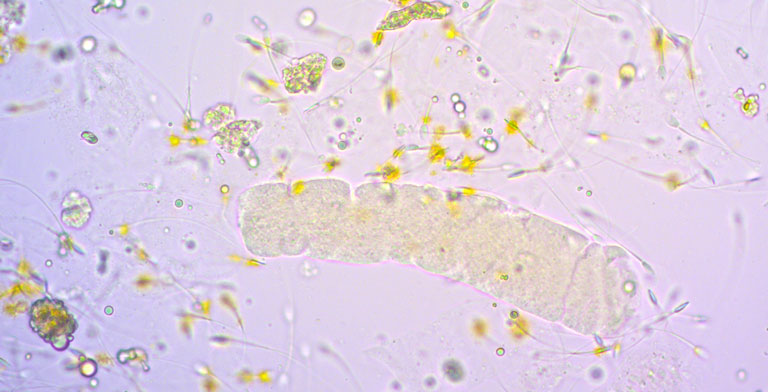
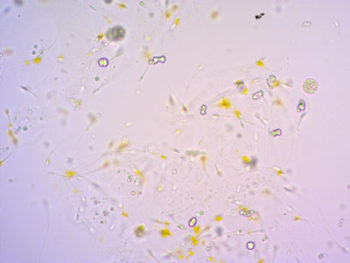
По результатам дополнительных анализов, взятых на первичном приёме, были выявлены признаки острого поражения почек: плотность мочи 0,016 (референсные значения 1,030–1,050), рН 5,5 (референсные значения 6,0–7,5), умеренная протеинурия (соотношение концентраций белка и креатинина в моче — 0,73). В осадке мочи были обнаружены конгломераты кристаллов оксалата кальция моногидрата в умеренном количестве (рис. 2), единичные кристаллы оксалата кальция дигидрата, восковидные цилиндры от 0 до 1 в поле зрения (рис. 3). Элементы мочевого осадка были окрашены желчными пигментами. Концентрация С-реактивного белка находилась в пределах нормы, а также не было получено лабораторных данных в пользу лептоспироза.
 |
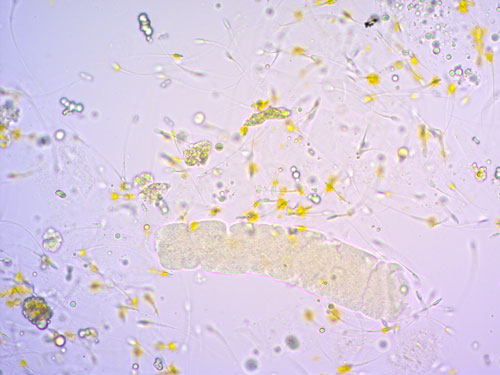 |
| Рис. 2. Кристаллы оксалата кальция моногидрата | Рис. 3. Восковидный цилиндр в осадке мочи |
В сторонней клинике пациент находился в ОРИТ под постоянной инфузией кристаллоидных растворов с применением дополнительных препаратов (в т. ч. преднизолона). Собаку удалось стабилизировать в течение нескольких суток без проведения процедуры гемодиализа. В первые сутки уровень глюкозы был не стабилен, что потребовало дополнительного введения растворов глюкозы внутривенно. На момент выписки пациента из стационара сторонней клиники уровень маркеров азотемии и глюкозы пришёл в норму, общее состояние стабилизировалось.
Через 10 дней после выписки из стационара владельцы повторно обратились на приём с ухудшением состояния собаки (снижение аппетита, активности). Мочеиспускание, дефекация были в норме. Жажда усиливалась на фоне приёма преднизолона, после его отмены пришла в норму.
При осмотре патологий выявлено не было, УЗ-картина внутренних органов соответствовала норме, УГК — 6,5 ммоль/л, АД (левая грудная конечность) — ср. 130/90.
Был произведён забор крови на клинический и биохимический анализы:
| Показатель | Результат | Референсные значения |
| АЛТ | 132 МЕ/л | до 80 МЕ/л |
| Щелочная фосфатаза | 203 МЕ/л | до 150 МЕ/л |
| Креатинин | 267 мкмоль/л | до 120 мкмоль/л |
| Мочевина | 42 мкмоль/л | до 8 мкмоль/л |
| Креатинкиназа | 731 МЕ/л | до 500 МЕ/л) |
| Натрий | 128 ммоль/л | от 144 ммоль/л |
| Калий | 7,9 ммоль/л | до 5,8 ммоль/л) |
| Хлор | 101 ммоль/л | от 109 ммоль/л |
| Фосфор | 2,3 ммоль/л | до 2,0 ммоль/л |
С учётом соответствующих изменений уровня электролитов при отсутствии данных об олигоанурии и обструкции мочевыводящих путей наиболее вероятным диагнозом являлся гипоадренокортицизм (болезнь Аддисона).
Для подтверждения диагноза была проведена стимуляционная проба с АКТГ (таблица 1).
Таблица 1. Результаты стимуляционной пробы с АКТГ
| Показатель | Результат исследования, нмоль/л | Референсное значение, нмоль/л |
| Базовый кортизол | 6,35 | 25–250 |
| Кортизол через час после введения АКТГ | 7,72 | 200–450 |
Через неделю после начала заместительной терапии (флудрокортизон 40 мкг/кг/сутки) болезни Аддисона общее состояние собаки нормализовалось, уровни маркеров азотемии пришли в норму.
Хочется сделать небольшое отступление по поводу непродолжительного периода достигнутой стабильности у пациента после выписки из стационара другой клиники — в данном случае сработала частичная заместительная терапия применёнными ГКС, после отмены которой симптомы гормональной недостаточности вернулись, позволив обратить пристальное внимание на выраженные электролитные нарушения у клинически стабильной собаки.
На сегодняшний день период наблюдения за собакой составляет 5 месяцев. На фоне применения заместительной терапии (флудрокортизон в подобранной дозировке 40 мкг/кг/сутки) была достигнута стабилизация состояния пациента (клинические признаки не рецидивировали, электролитных и других нарушений в результатах контрольных лабораторных тестов не было выявлено).
Обсуждение
Этот клинический случай приведён в пример для того, чтобы обратить внимание на необходимость критической оценки каждого пациента. Ещё на первичном приёме животному мог быть поставлен верный диагноз.
На что стоит обратить внимание при оценке данных, полученных на первичном приёме:
- Наиболее ярким маркером наличия у животного гипоадренокортицизма является нарушение электролитного состава плазмы крови: гиперкалиемия сопровождающаяся гипонатриемией и гипохлоремией. Однако необходимо помнить, что как гиперкалиемия, так и гипонатриемия могут развиваться по причине острого поражения почек, сопровождающегося олигоанурией.
- Олигоанурия является редким, но тяжёлым осложнением острого поражения почек. При этом подобное состояние может быть следствием как тяжёлого повреждения почек, так и снижения ОЦК, развивающегося в том числе при выраженной дегидратации (например, на фоне гипоадренокортицизма).
- Ещё одним важным аспектом является оценка гидратационного статуса. Наиболее привычный в практике метод оценки тургора кожи может давать ложные результаты в определённых ситуациях. Например, при остро развившейся дегидратации тургор кожи может какое-то время оставаться в норме. Это связано с тем, что в первую очередь теряется внутрисосудистая жидкость, после чего жидкость в сосуды начинает перемещаться из межклеточного пространства. Поэтому у пациентов с острым заболеванием более ранними маркерами дегидратации будут сухость слизистых оболочек, снижение СНК, эндофтальм. Клинический анализ крови (в частности, гематокрит) также будет говорить о гидратационном статусе. При анурии гематокрит может снижаться по причине гиперволемии или может быть повышен при наличии других источников потери жидкости, таких как рвота и диарея.
- Снижение УГК может развиваться при остром поражении почек, сопровождающемся панкреатитом или поражением печени. Однако в совокупности с нарушением электролитного состава плазмы крови является ещё одним маркёром болезни Аддисона.
Рассматривались другие возможные диагнозы:
- Лептоспироз: за него говорит анамнез (доступ к стоячей воде), признаки поражения печени и почек, лейкоцитоз.
- Отравление этиленгликолем, при котором часто выявляются признаки общей интоксикации (рвота, диарея), ацидоз (рН мочи 5,5) и кристаллы оксалата кальция моногидрата в осадке мочи, признаки острого поражения почек (цилиндры в осадке мочи).
- Векторные инфекции и кровепаразиты как причина острого гломерулонефрита.
- Обструктивная уропатия с большой долей вероятности может быть причиной подобных симптомов и лабораторных отклонений. Так, отсутствие мочеиспускания может быть как результатом обструкции уретры (тогда владелец будет отмечать безуспешные попытки к мочеиспусканию, а на осмотре выявится переполненный мочевой пузырь), так и следствием билатерального уретеролитиаза (тогда мочевой пузырь не будет наполнен). Однако данная патология не требует отдельного обсуждения, так как легко диагностируется при помощи УЗИ органов мочевыводящей системы.
Что же касается болезни Аддисона — это «великий симулятор», как любят называть её врачи-эндокринологи. Такое название неслучайно, ведь для этого заболевания не существует патогномоничных симптомов. Распространёнными клиническими признаками являются перемежающиеся рвота и диарея, снижение аппетита, вялость, дефицит массы тела, полиурия и дегидратация. Наиболее очевидной болезнь становится в период так называемого криза Аддисона, когда развивается гиповолемический шок. При длительной гипоперфузии почек данное состояние может привести к их острому повреждению, с чем мы и столкнулись в данном случае.
При гипоадренокортицизме могут встречаться следующие лабораторные отклонения: эозинофилия и лимфоцитоз, умеренная нерегенераторная анемия, умеренная преренальная азотемия, гиперкалиемия, гипонатриемия и гиперкальциемия, снижение относительной плотности мочи (таблица 2).
Таблица 2. Распространённые клинико-патологические изменения, регистрируемые при гипоадренокортицизме собак (взято из Ettinger SJ, Feldman ЕС: Textbook of veterinary internal medicine, ed 7, St Louis, 2010, Saunders/Elsevier)
| Клинико-патологические изменения | Встречаемость, % |
| Клинический анализ крови | |
| Эозинофилия | 20 |
| Отсутствие стрессовой лейкограммы | 92 |
| Лимфоцитоз | 10 |
| Нейтрофилия | 32 |
| Нерегенераторная анемия | 27 |
| Биохимический анализ крови | |
| Азотемия | 88 |
| Гиперкальциемия | 31 |
| Гиперкалиемия | 95 |
| Гиперфосфатемия | 68 |
| Гипоальбуминемия | 6–39 |
| Гипохлоремия | 42 |
| Гипохолестеролемия | 7 |
| Гипогликемия | 17 |
| Гипотариемия | 81 |
| Повышение печеночных ферментов | 30–50 |
| Метаболический ацидоз | 40 |
| Плотность мочи < 1,030 | 60 |
Гипоадренокортицизм в своём классическом проявлении приводит к снижению секреции двух классов гормонов: глюкокортикоидов и минералокортикоидов.
Именно дефицит минералокортикоидов в итоге приводит к манифестации болезни Аддисона за счёт выраженной дегидратации и, как следствие, к поражению почек. Механизм поражения почек заключается в снижении почечного кровотока. Чтобы разобраться в этом процессе, необходимо вспомнить строение структурной единицы почки — нефрона. Нефрон состоит из гломерулы и отходящих от неё почечных канальцев. В капиллярах гломерулы за счёт высокого внутрипросветного давления происходит ультрафильтрация и образование первичной мочи. Физиология этого процесса основана на разнице в диаметре приносящей (афферентной) и выносящей (эфферентной) артериол. При незначительном падении давления в афферентной артериоле, например, при снижении ОЦК, активируется система РААС и происходит вазоконстрикция эфферентной артериолы. Этот механизм стабилизирует давление внутри капсулы и позволяет продолжить выделение токсических продуктов обмена веществ из организма. При выраженном снижении ОЦК даже активация РААС не способна поддерживать достаточное для обеспечения фильтрации давление в капиллярах клубочков, что приводит к развитию анурии. Важным фактором поражения почек является то, что эфферентная артериола даёт начало так называемой чудесной сети капилляров, оплетающих почечные канальцы. Если приток крови к канальцам снижается на непродолжительный период времени, это практически не оказывает влияния на клетки канальцев. Однако при продолжительном нарушении оксигенации и питания клеток развивается острое повреждение эпителия канальцев. В дальнейшем некротизированный эпителий начинает слущиваться и может приводить к обструкции канальцев и полному выпадению функции поражённого нефрона. Частым признаком острого повреждения почечных канальцев является появление различных цилиндров в моче, что и было выявлено при исследовании осадка мочи у данного пациента.
Дефицит минералокортикоидов также ответственен за нарушение электролитного состава крови. В норме альдостерон обеспечивает задержку натрия и хлора и экскрецию калия и гидроксид-иона в почечных канальцах. Соответственно, дефицит альдостерона приводит к обратному эффекту: задержке калия и гидроксид-иона и повышенной экскреции натрия и хлора. Ионы натрия и хлора, находясь в высоких концентрациях в просвете почечных канальцев, утягивают за собой воду, что приводит к полиурии и развитию дегидратации. Следствием задержки гидроксид-ионов является умеренный ацидоз. С прогрессированием болезни Аддисона усиливается и гиперкалиемия — помимо снижения экскреции калия в почечные канальцы, происходит его задержка по причине снижения СКФ, развивающийся ацидоз способствует выходу калия из клетки в межклеточное пространство.
Нужно отметить, что подобные электролитные и кислотно-щелочные изменения могут развиваться и при остром поражении почек, сопровождающемся олигоанурией. Задержка калия у пациентов с олигоанурией в первую очередь происходит за счёт снижения СКФ или полного прекращения образования первичной мочи. Уменьшение доставки натрия к дистальным почечным канальцам, в свою очередь, приводит к снижению экскреции калия в мочу. За счёт задержки жидкости в кровеносном русле может развиваться так называемая гиперволемическая гипонатриемия. Повреждение почечных канальцев приводит к снижению экскреции гидроксид-ионов и реабсорбции бикарбонат-ионов — развивается ацидоз, усугубляющий гиперкалиемию.
Гипогликемия развивается в результате снижения секреции ГКС, стимулирующих глюконеогенез.
Если говорить о дифференциальной диагностике, то наиболее вероятной причиной поражения почек у описанного пациента, исходя из анамнеза и данных лабораторных исследований, являлся лептоспироз. Несмотря на наличие вакцинации в анамнезе, остаётся вероятность заражения штаммами, не входящими в состав стандартной вакцины (Australis, Grippotyphosa, Pomona и др.). Кроме того, в высокоэндемичной зоне, какой является Ленинградская область, рекомендуется вакцинация от лептоспироза не реже, чем раз в 12 месяцев. Напомню, что собака вакцинировалась последний раз около 1,5 года назад. Колонизация почек лептоспирами происходит практически у всех заражённых животных. Основным местом размножения лептоспир является эпителий почечных канальцев. Однако, помимо канальцев, развивается и поражение интерстиция. За счёт определённых белков, находящихся на поверхности мембран лептоспир, происходит активация воспалительных медиаторов и провоспалительных цитокинов, привлечение клеток воспаления. Место нахождения лептоспир становится очагом воспаления, где происходит активное повреждение тканей. Таким образом, развивается тубулоинтерстициальный нефрит. Воспалительный отёк почечной паренхимы способствует снижению СКФ за счёт сдавливания кровеносных сосудов. Результатом повреждения эндотелия мелких сосудов становятся ишемические поражения почечной паренхимы. Сами по себе лептоспиры не поражают гломерулы. Однако гломерулонефрит нередко развивается как реакция на присутствие лептоспир. Ведущими факторами при этом являются васкулит и активное образование антител. Поражение печени при лептоспирозе развивается в первую очередь за счёт бактериальных токсинов. Возможно развитие иммуноопосредованного миозита.
Лабораторные изменения при лептоспирозе могут быть весьма обширными. Клинический анализ крови может выявить лейкоцитоз и тромбоцитопению. Биохимический профиль может включать азотемию, повышение печёночных трансаминаз, повышение КФК и С-реактивного белка, гипонатриемию, гипохлоремию, гипокалиемию или гиперкалиемию. Анализ мочи часто выявляет гипостенурию, глюкозурию и появление цилиндров в осадке мочи.
Похожую с кризом Аддисона картину может давать и отравление этиленгликолем (далее — ЭГ). ЭГ широко используется в промышленности при производстве пластика и красок, является распространённым компонентом, входящим в состав тормозной жидкости, моторного масла, антикоррозийных соединений, растворителей, жидкостей для мытья стёкол и многих других веществ. Однако наиболее часто фиксируются случаи отравления домашних животных антифризом. Он, предположительно, имеет сладкий вкус и привлекателен для некоторых собак и кошек. Минимальная летальная доза неразбавленного ЭГ составляет 4,4–6,6 мл/кг у собак и 1,4 мл/кг у кошек (6–7). ЭГ быстро всасывается после попадания в ЖКТ. Большее количество быстро выводится с мочой. Оставшаяся часть метаболизируется печенью с помощью алкогольдегидрогеназы и других печёночных ферментов до альдегида гликолевой кислоты и далее до гликолевой кислоты. Гликолевая кислота в основном превращается в щавелевую кислоту, но может следовать нескольким метаболическим путям. Щавелевая кислота связывает кальций, приводя к формированию кристаллов оксалата кальция. Отложение кристаллов происходит во всём организме, однако наибольшая часть откладывается в паренхиме почек, приводя к их тяжёлому повреждению. Кристаллурия является частой находкой у животных с отравлением ЭГ. До того, как ЭГ претерпевает метаболизм, он не более токсичен, чем этанол. Хотя ЭГ сильнее угнетает ЦНС, чем этанол. В организме ЭГ приводит к раздражению слизистой оболочки ЖКТ, повышает осмоляльность плазмы крови и угнетает ЦНС. Но в отличие от этанола, ЭГ претерпевает биотрансформацию до высокотоксичных метаболитов, результатом присутствия в организме которых является метаболический ацидоз и острое повреждение почек.
Почечная недостаточность — это наиболее тяжёлое осложнение при отравлении ЭГ. Основной механизм поражения почек заключается в отложении в почечной паренхиме кристаллов оксалата кальция. Первоначально кристаллы образуются в просвете почечных канальцев. Далее они адгезируются клетками эпителия канальцев, а затем поглощаются ими. Внутри клетки кристаллы повреждают клеточную мембрану, увеличивают количество активных форм кислорода, приводя к митохондиальной дисфункции и дальнейшей гибели клетки.
Первые симптомы отравления развиваются обычно в течение первых 30 минут после поглощения токсина и могут длиться до 12 часов. Они проявляются нарушением работы ЖКТ, выражающимся рвотой, гематемезисом, абдоминальной болью. Угнетение ЦНС выражается в атаксии, могут наблюдаться мышечные спазмы. Снижается температура тела. В результате повышения осмоляльности плазмы крови развивается полиурия и полидипсия. С прогрессированием поражения ЦНС жажда угнетается, однако сохраняется осмотрический диурез, что приводит к развитию дегидратации. Спустя 12 часов возможно наступление клинического улучшения состояния. Симптомы, развивающиеся по причине воздействия токсических метаболитов ЭГ, начинают проявляться спустя 36–72 часа после его попадания в ЖКТ у собак и через 12–24 часа у кошек. Клинические признаки могут включать тяжёлое угнетение состояния или кому, судороги, анорексию, рвоту, изъязвление слизистой оболочки ротовой полости. Отравление ЭГ часто осложняется олигоанурией, сопровождающейся изостенурией.
Лабораторные находки при отравлении ЭГ часто включают гемоконцентрацию и стрессовую лейкограмму, азотемию и гиперфосфатемию, гиперкалиемию при развитии олигоанурии. Изостенурия (плотность мочи от 1,008 до 1,012) развивается спустя примерно 3 часа после отравления. Параллельно снижается рН мочи вследствие метаболического ацидоза. Кристаллы оксалата кальция часто встречаются в осадке мочи и могут наблюдаться уже спустя 3–6 часов после отравления, при этом для интоксикации ЭГ более характерно наличие кристаллов оксалата кальция моногидрата. Также в осадке мочи могут обнаруживаться цилиндры, почечный эпителий, лейкоциты и эритроциты.
Важной диагностической ступенью является УЗИ почек. Для отравления ЭГ характерно выраженное повышение эхогенности коркового слоя почек, иногда с образованием гиперэхогенной кортико-медуллярной каймы.
Ещё одной важной особенностью диагностики отравления ЭГ является флуоресценция под лампой Вуда рвотных масс, мочи, иногда шерсти морды и перинеальной области. Связано это с тем, что многие производители начали добавлять в антифриз флуоресцентные компоненты.
Иммуноопосредованный гломерулонефрит редко протекает в виде острого состояния, хотя такие пациенты встречаются. Характерной особенностью ГН является протеинурия. Степень её может варьировать, а иногда соотношение концентраций белка к креатинину в моче остаётся в пределах нормы. Наиболее распространёнными причинами иммуноопосредованного ГН являются инфекционные заболевания. Для Ленинградской области и Санкт-Петербурга такими патогенами являются клещевые инфекции: бабезиоз, боррелиоз, эрлихиоз и анаплазмоз. Реже выявляются дирофиляриоз и лейшманиоз — в основном у животных, привезённых из других регионов. Нередко вышеперечисленные заболевания могут протекать бессимптомно. Однако острые состояния, приводящие к развитию ГН, нередко сопровождаются характерными клиническими признаками и лабораторными изменениями.
Так, при бабезиозе могут наблюдаться симптомы, обусловленные острым гемолизом.
Наиболее распространёнными последствиями боррелиоза являются Лайм-артрит и Лайм-нефрит. Для него не характерны какие-либо специфические изменения лабораторных показателей. Согласно последним данным, представленным Американским колледжем ветеринарной медицины (ACVIM) в 2018 году, у большинства серопозитивных собак не наблюдается каких-либо клинических признаков.
Для эрлихиоза характерны лихорадка, лимфадениты, спленомегалия, геморрагии, увеиты. Реже могут наблюдаться рвота, диарея, повышенная утомляемость, кашель и/или одышка, связанные с пневмонией. Лабораторные находки включают тромбоцитопению, анемию, лейкопению, гиперглобулинемию.
Клинические признаки анаплазмоза связаны с присутствием в организме антигена, тромбоцитопенией и иммуноопосредованным поражением суставов, почек и глаз. Таким образом, инфицированная анаплазмой собака может демонстрировать лихорадку, угнетение, анорексию, поверхностные геморрагии, хромоту, увеит. ГН у пациентов, заражённых анаплазмой, случается крайне редко. Лабораторные находки могут включать тромбоцитопению, анемию, лейкопению, гиперглобулинемию.
Выводы
Несмотря на то что все симптомы болезни Аддисона у описанной собаки можно бы было объяснить причиной и следствием развития острого поражения почек, необходимо иметь высокую настороженность относительно животных, поступающих с признаками почечной недостаточности, сопровождающимися выраженной дегидратацией, гиперкалиемией, гипонатриемией и гипохлоремией. Второй вывод, который стоит сделать из этого клинического случая, — это необходимость первоначальной стабилизации уровня артериального давления и регидратации пациента с анурией перед принятием решения о проведении гемодиализа.
Литература
- M. Rheault. Renal and Urologic Issues, An Issue of Clinics in Perinatology. 2014.
- A. Lehnhardt, M. J. Kemper. Pathogenesis, diagnosis and management of hyperkalemia. Pediatr Nephrol. 2011.
- C. E. Greene. Infectious Diseases of the Dog and Cat; 4th Edition. 2012.
- E. C. Feldman, R. W. Nelson, et al. Canine and Feline Endocrinology; 4th Edition. 2015.
- Kersting EJ, Nielson SW. Experimental ethylene glycol poisoning in the dog. Am J Vet Res. 1966.
- Schiavone FM, Cantor FD, Brogan GX. Emergency Toxicology, 2nd ed. Philadelphia, Lippincott-Raven. 1998.
- Osweiler GD, Carson TL. Handbook of Small Animal Practice, 3rd ed. Philadelphia: WB Saunders. 1997.
- M. Peterson. Small Animal Toxicology, 3rd Edition. 2012.
- J. A. Richardson, S. M. Gwaltney-Brant. Ethylene glycol toxicosis in dogs and cats. NAVC clinician’s brief. 2003.
- M. P. Littman, B. Gerber, et al. ACVIM consensus update on Lyme borreliosis in dogs and cats. J Vet Intern Med. 2018.
- A. Sainz, X. Roura, et al. Guideline for veterinary practitioners on canine ehrlichiosis and anaplasmosis in Europe. Parasit Vectors. 2015.
- J. F. Zachary. Pathologic Basis of Veterinary Disease Expert Consult,6th Edition. 2017.
- D. Chew, S. DiBartola, P. Schenck. Canine and Feline Nephrology and Urology; 2nd edition. 2010.
- J. Bartges, D. J. Polzin. Nephrology and Urology of Small Animals. 2014.
СВМ № 2/2019