Barbara Blicher Thomsen1, Hanne Gredal1, Martin Wirenfeldt1, Bjarne Winther Kristensen2, Bettina Hjelm Clausen1, Anders Elm Larsen3, Bente Finsen3, Mette Berendt1 and Kate Lykke Lambertsen3,4,5
1 Department of Veterinary Clinical Sciences, Faculty of Health and Medical Sciences, University of Copenhagen, Denmark.
2 Department of Pathology, Odense University Hospital, Denmark.
3 Department of Neurobiology Research, Institute of Molecular Medicine, University of Southern Denmark, Denmark.
4 Department of Neurology, Odense University Hospital, Denmark.
5 BRIDGE, Brain Research — Inter-Disciplinary Guided Excellence, Department of Clinical Research, University of Southern Denmark, Denmark.
Предпосылки к исследованию
Собаки страдают от спонтанного ишемического инсульта, неврологические симптомы и результаты магнитно-резонансной томографии (MRI) которого в значительной степени сравнимы с таковыми у человека [1, 2]. Как и у людей, у собак с ишемическим инсультом проявляются различные неврологические клинические признаки, зависящие от расположения окклюзии сосуда и размера инфарктной области [1, 3–5].
Использование грызунов в качестве экспериментальных моделей способствовало накоплению обширных знаний о патофизиологических механизмах ишемического инсульта [6, 7]. Однако оказалось трудным разработать успешные терапевтические меры для людей с инсультом на основе результатов, полученных от подобных моделей [8, 9]. Чтобы восполнить этот очевидный пробел в исследовании инсульта, было предложено найти альтернативные животные модели, заключающие в себе больше аспектов данного заболевания у человека [10].
Собаки напоминают человека наличием большого имеющего извилины мозга, его анатомией, кровоснабжением и высоким соотношением количества белого вещества к серому веществу [11–13]. Кроме того, собаки подвержены процессу естественного старения и, как и люди, страдают от заболеваний долгожителей, таких как заболевания сердечно-сосудистой системы и сахарный диабет. Они также подвержены воздействию схожих факторов риска развития ишемического инсульта, включающих в себя ожирение, гипертонию, воздействия загрязнения окружающей среды и пассивного курения.
Количество гистопатологических отчётов об ишемическом инсульте у собак невелико, и исследований, содержащих детальную оценку совокупности морфологических изменений нейронов, микроглии/маркофагов и астроцитов, всё ещё недостаточно [14–28]. У человека нейроглия расценивается как центральный компонент патофизиологии ишемического инсульта, и в особенности микроглия в последнее время привлекает внимание основных исследований, так как эти клетки могут оказывать как положительное, так и отрицательное влияние на нейроны, расположенные в пери-инфарктных патологических зонах [7, 29–32].
Данное исследование было направлено на описание результатов гистопатологических исследований с акцентом на нейроглиальные реакции в зоне инфаркта и соседних (пери-инфарктных) зонах мозга собаки со спонтанно возникающим инфарктом средней мозговой артерии (MCA). Также обсуждается возможность использования случая ишемического инсульта собаки в качестве спонтанной животной модели ишемического инсульта человека.
Описание клинического случая
Кастрированная сука породы ротвейлер возрастом семи лет и восемь месяцев была представлена в университетскую больницу для мелких домашних животных Университета Копенгагена (Дания) с острым левосторонним неамбулаторным гемипарезом и левосторонним пространственным игнорированием. В остальном клиническое обследование было без особенностей, и результаты гематологического и биохимического исследований, тромбоэластографии, исследования мочи и цереброспинальной жидкости были в пределах нормы. У собаки был выявлен пониженный уровень тироксина (Т4): 6,44 нмоль/л (11,2–40,8) и свободного T4: 3,86 пмоль/л (7,7–47,6) и повышение уровня тиротропина (TSH): 0,62 нг/мл (0,00–0,50), но без клинических признаков гипотиреоза. Результаты MRI были сопоставимы со спонтанной правосторонней окклюзией MCA (илл. 1). Собаку подвергли эвтаназии по просьбе владельца на третий день после приёма в клинику, и мозг был пожертвован для посмертного исследования.
Мозг клинически здоровой беспородной суки возрастом 1 год и 7 месяцев, усыпленной по просьбе владельца и пожертвованной университетской больнице для мелких домашних животных для педагогических и исследовательских целей, был использован в качестве нормального контроля для разработки иммуногистохимических (IHC) протоколов и для контрольных срезов.
Использование тканей собак было одобрено местной административной и этической комиссией Департамента ветеринарно-клинических и зоологических наук, Факультетом здоровья и медицинских наук, Университетом Копенгагена (номер разрешения 1 N/2013).
Илл. 1. Магнитно-резонансные изображения участка ишемического повреждения мозга собаки. Последовательные магнитно-резонансные изображения коронарных секций на уровне теменной и височной долей мозга собаки были сняты на второй день после начала ишемического инсульта. Направление изображений: от рострального до каудального. Изображения получили при помощи 0,2 T MRI (Vet-MR, Esaote). Верхний ряд: Не отмечается изменений сигнала на T1 снимках. Средний ряд: Гиперинтенсивные сигналы видимы на T2. Нижний ряд: Гиперинтенсивные сигналы видны на FLAIR. Гиперинтенсивность отражает паренхиматозные изменения вследствие ишемического инфаркта
Обработка ткани мозга
Мозг собаки с клиническим ишемическим инсультом был взят для исследования в течение двух часов после смерти животного. Фиксацию мозга проводили с помощью 4%-ного раствора формальдегида в течение 14 недель, после чего он был помещён на хранение на 15 месяцев в 0,15М натрий-фосфатный буфер с 30%-ной сахарозой и 0,1%-ным азидом натрия (pH 7,4) при температуре 4°C. Мозг поперечно разрезали на 19 пластин толщиной 5 мм. Каждая пластинка была пронумерована и сфотографирована так, чтобы ростральная поверхность среза была обращена вверх. Оболочки мозга были удалены, и пластинки разделили на более мелкие куски для того, чтобы они поместились в вибратом. Каждый кусок поместили в агар, а затем разделили на вибратоме (Leica VT1000 S, Leica Microsystems, Ballerup, Denmark), чтобы получить 24 комплекта свободно плавающих срезов толщиной 70 мкм. Срезы хранили при температуре –12°C в растворе криопротектора de Olmos, содержащем поливинилпиролидон и сахарозу, растворённую в смеси этиленгликоля и натрий-фосфатного буфера до дальнейшей обработки.
Гистохимическая окраска
Каждый 24-й свободно плавающий срез мозга собаки с инсультом окрасили 0,01% раствором толуидинового синего (ТВ) (Merck Millipore, Hellerup, Denmark), разведённого в 0,08М растворе Na2HPO4-2H2O и 0,07М растворе лимонной кислоты в дистиллированной воде [34] и раствором люксола быстрого синего (LFB) (Amplicon, Odense, Denmark) [35] соответственно. Срезы оставили на ночь для промывки в трис-буферном физиологическом растворе (TBS) при pH 7,4, а затем поместили на предметные стёкла, покрытые желатином и высушили на воздухе. Для окраски ТВ стёкла поместили в ТВ на 26 минут с последующей дифференциацией в ступенчатой серии спиртов и очисткой ксилолом (диметилбензолом). Для LFB-окраски дифференциация срезов началась с их помещения в ступенчатую серию спиртов, а затем секции поместили в раствор LFB на ночь при 4°C. На следующий день дифференциацию срезов продолжили путём их помещения в 0,05% раствор карбоната лития на 3 мин и контрастирующим окрашиванием гематоксилином и эозином (HE). Препараты покрыли заливочной средой Depex (VWR, Herlev, Denmark).
Иммуногистохимическое исследование
Для иммуногистохимического выявления в астроцитах микроглиального белка Iba1 и глиального фибриллярного кислого белка (GFAP) отобрали каждый 24-й свободно плавающий срез мозга собаки с инсультом. Процедуры промывки и инкубации проводили при комнатной температуре, если условия не были оговорены заранее. Секции отмывали дважды по 30 мин в 0,05М TBS, pH 7,4, а затем оставили на ночь в том же растворе при 4°C. Демаскирование проводили двукратной промывкой срезов по 15 мин в трис-ЭДТА буфере (TEG) с последующим выделением эпитопов путём подогрева срезов в TEG в микроволновой печи (Moulinex Optimo Duo, Groupe SEB, Ballerup, Denmark) дважды по 4 мин при 800 W и однократно в течение 10 мин при 480 W или до кипения. Срезы промыли в течение 30 мин в TBS с последующим троекратным отмывом по 25 мин в TBS и 1%-ном растворе Triton X, затем преинкубировали в 10%-ной сыворотке плода телёнка (FCS) в TBS в течение одного часа, а после этого инкубировали в течение трёх дней при 4°C с одним из следующих первичных антител: поликлональными анти-Iba1 кролика (1:500, Wako-Chem, Osaka, Japan) и поликлональными анти-GFAP кролика (1:200, Dako, Glostrup, Denmark), разведёнными в 10% FCS в TBS. Далее срезы мозга собаки с инсультом отмыли трижды по 15 мин в TBS, 30 мин в TBS и 1%ном Triton-X, 15 мин в TBS и заблокировали для активности эндогенной пероксидазы помещением на 30 минут в 100%-ный метанол и 0,2%-ный раствор перекиси водорода. Отмыв проводили 15 минут в TBS и дважды по 60 минут в TBS и 1%-ном растворе Triton-X. Срезы поместили для инкубации в EnVision™ + System-HRP (Dako) на ночь при 4°C. Затем все срезы отмыли трижды в течение 45 мин в TBS и поместили в проявляющий раствор 0,05% 3,3'-диаминобензидина (DAB) и 0,033% перекиси водорода. Срезы затем отмыли дважды по 30 минут в TBS и 30 минут в трис-буфере. Наконец, срезы поместили на предметные стёкла, покрытые желатином и во время сушки на воздухе провели контрастирующее окрашивание с помощью TB, разведённого трис-буфером до раствора на 16 минут, обезвожили помещением в ступенчатую серию спиртов, очистили диметилбензолом и покрыли заливочной средой Depex (VWR).
Контроль специфичности антител осуществляли на срезах тканей мозга контрольной собаки с помощью замены первичного антитела на иммуноглобулин IgG кролика (Dako) и исключением первичного антитела из протокола. Иммуноокрашивание срезов не проводилось.
 |
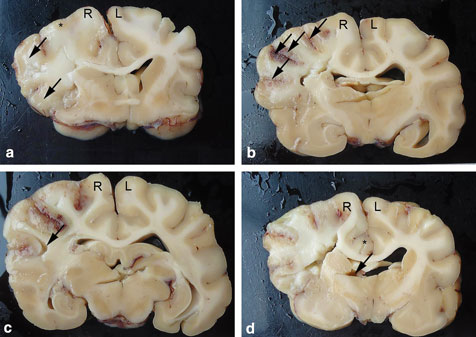
| Илл. 2. Макроскопически видимые повреждения мозга собаки с инфарктом правой средней мозговой артерии. А). Распухшие и уплощённые извилины с суженными бороздками (стрелки). Плохое разграничение серого и белого веществ и потемнение серого вещества (звёздочка). Поперечный срез на уровне базальных ядер. Б). Фокальные петехии в сером веществе нескольких бороздок (стрелки). Поперечный срез на уровне таламуса. С). Фокальное отслоение неокортекса от подлежащего серого вещества (стрелки). Поперечный срез на уровне таламуса. Д). Суженный и сдавленный правый латеральный желудочек (стрелка). Подсерповая грыжа со смещением правой поясной извилины (звёздочка). Отметьте общий зернистый вид нервной ткани, вызванный отёком, приведшим к асимметричности полушарий и среднелинейному смещению к левому полушарию. Поперечный срез на уровне хвостатого ядра. R — правое полушарие мозга. L — левое полушарие мозга |
 |
Илл. 3. Топографический обзор тканей мозга собаки, выбранных для гистопатологической оценки. А). Срез мозга, разделённый для обработки на вибратоме. Прямоугольник зоны инфаркта и прилегающая нейропаренхима. Б-Д). Ткани в прямоугольнике, окрашенные толуидиновым синим. IF инфаркт. P-IF периаинфарктная область. Стрелка Нейтрофильный гранулоцит. Мерные полоски b = 200 мкм, c = 100 мкм, d = 10 мкм |
Нейропатологическое исследование
Макроскопическое исследование мозга собаки с ишемическим инсультом сразу после его удаления из черепной коробки выявило мягкую и отёчную область диаметром примерно 20 мм, видимую на поверхности правого полушария мозга в области латерального сообщения лобной и теменной долей. Детальный осмотр мозга после фиксации и нарезки на секции выявил отёчную область, выступающую над естественной выпуклой дугой правой лобной и теменной долей мозга с уплощёнными извилинами и суженными бороздками. Расположение дефекта соответствовало поражённой области, видимой на MRI. Размеры дефекта составляли: в медиально-латеральном направлении до 32 мм, в вентрально-дорсальном до 36 мм и в рострально-каудальном до 35 мм. Дефект затрагивал серое вещество неокортекса и семиовальный центр белого вещества в каудальной части лобной доли, правой теменной доли, латеральной и высшей части правой височной доли и наиболее каудальной части правого гиппокампа. Медиальные части правой лобной и теменной долей в направлении серпа большого мозга, включая поясную извилину, медиальные части высшей лобной извилины и наиболее медиальный аспект правой височной доли не были повреждены. Также не были затронуты мозолистое тело, базальные ядра, таламус, мозговой ствол и мозжечок.
Дефект сгладил границу раздела серого и белого вещества, вызвал потемнение серого вещества и выглядел ломким и растрескивающимся (илл. 2а). Между дефектом и окружающей его паренхимой мозга была явно выражена чёткая граница. Ядро дефекта мозга собаки с инсультом было преимущественно блёклым. Тем не менее вдоль нескольких бороздок в сером веществе присутствовали фокальные петехии (илл. 2б), что указывало на кровоизлияние из-за реперфузии повреждённых сосудов и тканей, что обычно ассоциируется с эмболическими эпизодами. Фокальное отделение неокортекса от подлежащего белого вещества имело вид очерченного кортикального ламинарного некроза (илл. 2с). Отёк головного мозга проявлялся в виде зернистой шероховатости на поверхности среза в подозреваемой ишемической зоне на поражённых срезах. Присутствует очевидное среднелинейное смещение к неповреждённому левому полушарию и подсерповая грыжа со смещением правой поясной извилины под серп мозга и сдавливание полости правого бокового желудочка (илл. 2д). Патологические изменения в паренхиме мозга соответствуют ишемическому повреждению, вызванному прекращением кровотока на территории, снабжаемой МСА. Тромбоза сосудов и эмболии выявлено не было.
Гистологически мозг собаки с инсультом имел нормальную архитектуру и нормальную структуру белого и серого вещества. Не было отмечено признаков атеросклероза. В инфарктных областях правого полушария наблюдалась потеря нейронов и глиальных клеток и начало колликвационного некроза. В некротических областях паренхимы присутствовали инфильтрации нейтрофильных гранулоцитов и макрофагов, что соответствовало трёхдневному временному интервалу после повреждения (илл. 3). Ишемическое повреждение нейронов (сморщенные тела клеток и пикнотические ядра) и потеря нейронов были значительно более распространёнными, чем казалось по размерам видимого дефекта (илл. 4). Дальнейший морфологический анализ ишемических нейронов был ограничен из-за толщины и фрагментации срезов мозга собаки с инсультом, выполненных на вибратоме. Иммуногистохимическое маркирование Iba1 выявило явную микроглиальную/макрофагальную реактивность вокруг ишемического дефекта (илл. 5). На границе дефекта и в прилегающей дегенеративной ишемической паренхиме аккумулировались множественные круглые макрофагоподобные клетки (в последствие называемые «макрофагами»). Клетки микроглии демонстрировали реактивный микроглиоз с различными морфологиями, включая фенотип реактивного макрофага в близости дефекта. Также была идентифицирована и палочковидная микроглия. А в периинфарктной зоне наблюдался градиент микроглиальной реактивности, начинающийся со слабо реактивной микроглии на периферии дефекта (илл. 5). При приближении к инфаркту микроглия казалась более реактивной, с гипертрофией и усилением разветвлённости отростков, придающих клеткам кустистый вид. В контралатеральном полушарии отмечалась ограниченная область активации кортикальной микроглии в коре головного мозга, демонстрирующей антероградную аксонную (Валлерову) дегенерацию комиссуральных волокон от коры правого полушария. А в периинфарктной зоне наблюдался реактивный астроцитоз, который характеризовался повышенной экспрессией GFAP (илл. 6).
Ломкая текстура областей инфаркта правого полушария привела к фрагментации тканей при нарезке вибратомом. Множественные фрагменты в каждом срезе затруднили определение точного анатомического расположения патологических изменений в пределах каждого среза.
 |
| Илл. 4. Микрофотографии, демонстрирующие корковую периинфарктную зону мозга собаки. TB: толуидиновый синий. IF инфаркт. P-IF периинфарктная зона. Мерные полоски 200 мкм. Отметьте потерю нейронов и глиальных клеток в зоне инфаркта |
 |
| Илл. 5. Микрофотографии, демонстрирующие активацию микроглии/макрофагов в кортикальной пери-инфарктной зоне мозга собаки. IF инфаркт. P-IF периинфарктная зона. Секции, отмеченные для Iba1. Стрелки реактивная микроглия. Мерные полоски a = 200 мкм, b = 100 мкм, c = 30 мкм, d = 20 мкм. Отметьте реактивный микроглиоз в периинфарктной зоне |
 |
Илл. 6. Микрофотографии, демонстрирующие астроцитоз в кортикальной пери-инфарктной зоне мозга собаки. IF инфаркт. P-IF периинфарктная зона. Секции, отмеченные GFAP антителом. Мерные полоски a = 200 мкм, b = 30 мкм, c = 20 мкм. Отметьте реактивный астроцитоз |
Заключение
Нейропатологические изменения в повреждённой области мозга собаки с инсультом хорошо соотносятся с данными, описанными ранее для трёхдневного инфаркта человека [33,34] и экспериментальных мышиных моделей [35] и включают наличие повреждённых нейронов, реактивный микроглиоз и астроцитоз, а также инфильтрацию пери-инфарктной зоны нейтрофильными гранулоцитами и макрофагами.
При ишемическом инсульте мозга собаки в периинфарктной зоне была обнаружена реактивная микроглия. Патологические изменения, наблюдаемые в данном исследовании, схожи с таковыми у экспериментальной мышиной модели с перманентной окклюзией средней мозговой артерии [36,37]. Микроглия известна своей способностью отслеживать микросреду мозга и немедленно реагировать на повреждение путём прохождения морфологических и функциональных изменений [37, 38], таким образом, предполагается, что гибель нейронов запускает трансформацию фагоцитарной микроглии с амёбоидной морфологией, что наблюдалось в непосредственной близости к области некроза в данном исследовании [39]. Исходя из динамической роли микроглии в формировании ишемического дефекта, микроглия представляет растущий научный интерес [40, 41].
Астроцитоз наблюдался в кортикальной периинфарктной зоне. Одной из функций астроцитов является поддержание изменений сосудистого тона в ответ на нейронную активность, а также они способны синтезировать и поглощать нейромедиаторы. Реактивный астроцитоз развивается сразу после повреждения мозга. В то время как уже был показан отрицательный эффект астроцитоза в виде увеличения размера инфаркта [42], астроциты в то же время способны снижать уровень губительной эксайтотоксичности [43, 44]. Также известно, что в повреждённой ткани астроциты могут стимулировать микроглиальный ответ [37]. Таким образом, остаётся спорным вопрос: оказывают ли астроциты благотворное влияние на выздоровление или только усугубляют процесс повреждения [45]. Соответственно, этот тип клеток нуждается в дальнейшем исследовании на животных моделях ишемического инсульта, включая собак.
Распознавание нейтрофильных гранулоцитов основывали на морфологии ядра, что является методом, надёжность которого была ранее доказана при оценке секций, окрашенных ТВ [46]. В данном исследовании наблюдали инфильтрацию нейтрофильных гранулоцитов в некротический центр паренхимы мозга собаки (илл. 3). Это соответствовало ранним отчётам экспериментальных исследований на крысах и мышах, которые показали, что миграция нейтрофилов в паренхиму мозга, поражённого ишемическим инсультом, достигает пика в течение первых 48 часов [47, 48]. Однако не до конца понятны нейтрофильные реакции, следующие за ишемическим инсультом [49–52]. У человека нейтрофильные гранулоциты известны своей потенциально пагубной ролью в отношении прогрессирования инфаркта [53, 54]. Следовательно, изучение нейтрофилов при ишемическом инсульте проводилось с целью разработки новых методов лечения. Исследованию подвергались такие потенциальные мишени, как ингибирование активации, привлечения и трансмиграции нейтрофильных гранулоцитов [49]. У человека нейтрофилы составляют примерно 50–70% от всех лейкоцитов периферической крови [55]. По сравнению с человеком, нейтрофилы у мышей составляют всего около 8–24% от всех лейкоцитов периферической крови, в то время как у собак состав периферической крови очень сходен с человеческой, где нейтрофилы составляют примерно 60–80% от всех лейкоцитов периферической крови [57]. Соответственно было бы интересно изучить взаимоотношение между нейтрофилами и повреждением гематоэнцефалического барьера, геморрагической трансформацией и влиянием на окончательную неврологическую картину [49] у собак со спонтанным ишемическим инсультом.
Оценивая собак на роль потенциальной животной модели спонтанного инсульта, имеет значение то, был ли инсульт вызван локальным тромбозом или эмболией. В данном исследовании не было выявлено тромбов или эмболов ни на патологоанатомическом вскрытии, ни на гистологическом обследовании, хотя они подозревались в качестве подлежащей причины. Данный факт, однако, можно объяснить тем, что уменьшение эмбола in vivo, как и патологоанатомическое вскрытие собак, обычно происходит в течение нескольких часов (после смерти – прим. перев.) [58]. В данном случае, однако, эмболию считали наиболее вероятной причиной инфаркта из-за присутствия петехиальных кровоизлияний, указывающих на геморрагическую трансформацию, типично наблюдаемую при эмболических инфарктах человека (59). У человека большинство случаев ишемического инсульта вызвано тромбоэмболией [55]. Атеросклероз, являющийся наиболее частным типом сосудистой патологии, связанной с артериальным тромбозом у людей, кажется редким явлением у собак и наиболее часто связан с сахарным диабетом и гипотиреозом [16, 58]. Хотя у описываемой здесь собаки выявили низкий уровень Т4 и свободного Т4 и повышение TSH, не отмечались клинические признаки сопутствующего гипотиреоза, и на гистопатологическом исследовании не было выявлено атеросклероза. Это также подтверждает гипотезу о том, что ишемический инсульт у исследованной собаки был вызван эмболией.
Наиболее распространённым подтипом ишемического инсульта у человека являются инфаркты области, снабжаемой МСА [60], и, таким образом, целью большинства животных моделей является имитирование этого подтипа [61]. Окклюзия МСА также является распространённым подтипом спонтанного инсульта у собак [2] и тем самым предлагает интересную животную модель спонтанного инсульта. До настоящего момента экспериментальные исследования внесли весомый вклад в понимание патофизиологии ишемического инсульта, однако препараты, эффективные в экспериментальных исследованиях, провалились при тестировании на человеческих пациентах. Это может быть отчасти результатом того, что животные модели не способны в достаточной мере имитировать комплексность человеческого заболевания [62]. Преимуществом исследования патофизиологии спонтанного инсульта у собак является то, что при использовании экспериментальных моделей исключаются такие факторы, как анестезия и хирургическая травма. Кроме того, схожести между нейроанатомией мозга собаки и мозга человека могут объяснить схожести клинического проявления заболеваний, наблюдаемых у собак и человека в отношении неврологических дефицитов и окончательного исхода [2].
Ишемический инсульт у собак менее распространён по сравнению с человеком. Причины этого остаются неясными, но возможными объяснениями могут служить наличие в мозге собаки сосудистых анастомозов, редкость атеросклероза у собак [64] и быстрое рассасывание сгустков у собак [58]. Редкость ишемического инсульта у собак представляет неудобство для широкого использования собаки в качестве спонтанной животной модели ишемического инсульта у человека. Однако, так как по этическим причинам исследования разработки препаратов не могут быть проведены на собаках, собаки никогда не смогли бы заменить существующие животные модели инсульта. Вместо этого исследования патофизиологии спонтанного ишемического инсульта у собак могут помочь уменьшить различия между человеческими пациентами и экспериментальными животными моделями.
Результаты нашего исследования были основаны на исследовании одной собаки, и, следовательно, они не могут рассматриваться изолированно. В будущем их следует дополнить большими сравнительными исследованиями, предпочтительно с использованием мультицентрового дизайна, который может обеспечить большое число образцов мозга и поддержать заключения, основанные на полученных данных. Также было бы интересно провести дальнейшую нейропатологическую характеристику реакций нейронов и нейроглии в различные периоды времени после инсульта, а также необходимы исследования сосудистой патологии. Кроме того, нейропатологию белого вещества ранее связывали с клинически проявляющимися дефицитами у людей с ишемическим инсультом [65]. Следовательно, было бы интересно изучить подобные дефекты белого вещества у собак.
Сокращения
DAB — 3,3’-диаминобензидин; FCS — сыворотка плода телёнка; GFAP — глиальный фибриллярный кислый белок; HE — гематоксилин и эозин; IHC — иммуногистохимический; LFB — люксол быстрый синий; MCA — средняя мозговая артерия; MRI — магнитно-резонансная томография; PBS — натрия-фосфатный буфер; T4 — тироксин; TB — толуидиновый синий; TBS — трис-буфер; TEG — трис-ЭДТА буфер; TSH — тиротропин.
Вклад авторов
BBT, HG, BF, MB и KLL предложили идею исследования. BBT, HG и MB были ответственны за диагностику и лечение собаки. BBT, HG, BHC, AEL, BF и KLL были ответственны за разработку протокола пре-аналитической обработки ткани мозга и последующие гистохимическое и иммуногистохимическое исследования. BBT и HG провели все эксперименты и лабораторные анализы под непосредственным руководством BF и KLL. MW и BWK были ответственны за нейропатологическую оценку, а также внесли вклад в выбор методов окраски. BBT, BHC, BF и KLL были ответственны за обработку данных. BBT составил черновик рукописи. Все авторы внесли весомый вклад в составление рукописи. Все авторы прочли и одобрили окончательный вариант рукописи.
Благодарности
Исследование поддерживали датский совет независимых исследований (MB и KLL; номер гранта 11-106689/FTP) и Fonden til Lgevidenskabens Fremme (BF, KLL и BHC). Авторы благодарят Dennis Brok за помощь в извлечении мозга собаки из черепной коробки, Arne Mller и Jens Christian H. Srensen за помощь в разделении мозга собаки на секции, Line Freksen Stejlsted, Alice Lundsgaard Larsen, Dorte Lyholmer и Signe Marie Andersen за превосходную техническую поддержку проведения иммуногистохимических процедур.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Литература
1. Garosi L, McConnell JF, Platt SR, Barone G, Baron JC, de Lahunta A, et al. Clinical and topographic magnetic resonance characteristics of suspected brain infarction in 40 dogs. J Vet Intern Med. 2006;20:311–21.
2. Gredal H, Skerritt GC, Gideon P, Arlien-Soeborg P, Berendt M. Spontaneous ischemic stroke in dogs: clinical topographic similarities to humans. Acta Neurol Scand. 2013;128:e11–6.
3. Gredal H, Toft N, Westrup U, Motta L, Gideon P, Arlien-Soborg P, et al. Survival and clinical outcome of dogs with ischemic stroke. Vet J. 2013;196:408–13.
4. Kent M, Glass EN, Haley AC, March P, Rozanski EA, Galban EM, et al. Ischemic stroke in Greyhounds: 21 cases (2007–2013). J Am Vet Med Assoc. 2014;245:113–7.
5. Cervera V, Wilfried M, Vite CH, Johnson V, Dayrell-Hart B, Seiler GS. Comparative magnetic resonance imaging findings between gliomas and presumed cerebrovascular accidents in dogs. Vet Radiol Ultrasound. 2011;52:33–40.
6. Zille M, Farr TD, Przesdzing I, Muller J, Sommer C, Dirnagl U, et al. Visualizing cell death in experimental focal cerebral ischemia: promises, problems, and perspectives. J Cereb Blood Flow Metab. 2012;32:213–31.
7. Lambertsen KL, Biber K, Finsen B. Inflammatory cytokines in experimental and human stroke. J Cereb Blood Flow Metab. 2012;32:1677–98.
8. Howells DW, Sena ES, O’Collins V, Macleod MR. Improving the efficiency of the development of drugs for stroke. Int J Stroke. 2012;7:371–7.
9. Dirnagl U, Endres M. Found in translation: preclinical stroke research predicts human pathophysiology, clinical phenotypes, and therapeutic outcomes. Stroke. 2014;45:1510–8.
10. Fisher M, Feuerstein G, Howells DW, Hurn PD, Kent TA, Savitz SI, et al. STAIR Group: update of the stroke therapy academic industry roundtable preclinical recommendations. Stroke. 2009;40:2244–50.
11. Schaller O. Illustrated veterinary anatomical nomenclature. Stuttgart: Enke Verlag; 2007.
12. Anderson WD, Kubicek W. The vertebral-basilar system of dog in relation to man and other mammals. Am J Anat. 1971;132:179–88.
13. Gillilan LA. Extra- and intra-cranial blood supply to brains of dog and cat. Am J Anat. 1976;146:237–53.
14. Salger F, Stahl C, Vandevelde M, Piersigilli A, Henke D. Multifocal ischemic brain infarctions secondary to spontaneous basilar artery occlusion in a dog with systemic thromboembolic disease. J Vet Intern Med. 2014;28:1875–80.
15. Joseph RJ, Greenlee PG, Carrilo JM, Kay WJ. Canine cerebrovascular disease: clinical and pathological findings in 17 cases. J Am Anim Hosp Assoc. 1988;24:569–76.
16. Liu SK, Tilley LP, Tappe JP, Fox PR. Clinical and pathologic findings in dogs with atherosclerosis: 21 cases (1970-1983). J Am Vet Med Assoc. 1986;189:227–32.
17. Irwin JC, Dewey CW, Stefanacci JD. Suspected cerebellar infarcts in 4 dogs. J Vet Emerg Crit Care. 2007;17:268–74.
18. Palmer AC. Pontine infarction in a dog with unilateral involvement of the trigeminal motor nucleus and pyramidal tract. J Small Anim Pract. 2007;48:49–52.
19. Rossmeisl JH, Rohleder JJ, Pickett JP, Duncan R, Herring IP. Presumed and confirmed striatocapsular brain infarctions in six dogs. Vet Ophthalmol. 2007;10:23–36.
20. Cook LB, Coates JR, Dewey CW, Gordon S, Miller MW, Bahr A. Vascular encephalopathy associated with bacterial endocarditis in four dogs. J Am Vet Med Assoc. 2005;41:252–8.
21. Garosi L, McConnell JE, Platt SR, Barone G, Baron JC, de Lahunta A, et al. Results of diagnostic investigations and long-term outcome of 33 dogs with brain infarction (2000–2004). J Vet Intern Med. 2005;19:725–31.
22. Axlund TW, Isaacs AM, Holland M, O’Brien DP. Fibrocartilaginous embolic encephalomyelopathy of the brainstem and midcervical spinal cord in a dog. J Vet Intern Med. 2004;18:765–7.
23. Swayne DE, Tyler DE, Batker J. Cerebral infarction with associated venous thrombosis in a dog. Vet Pathol. 1988;25:317–20.
24. Patterson JS, Rusley MS, Zachary JF. Neurologic manifestations of cerebrovascular atherosclerosis associated with primary hypothyroidism in a dog. J Am Vet Med Assoc. 1985;186:499–503.
25. Patton CS, Garner FM. Cerebral infarction caused by heartworms (Dirofilaria immitis) in a dog. J Am Vet Med Assoc. 1970;156:600–5.
26. Kent M, Delahunta A, Tidwell AS. MR imaging findings in a dog with intravascular lymphoma in the brain. Vet Radiol Ultrasound. 2001;42:504–10.
27. Bagley RS, Anderson WI, de Lahunta A, Kallfelz FA, Bowersox TS. Cerebellar infarction caused by arterial thrombosis in a dog. J Am Vet Med Assoc. 1988;192:785–7.
28. Norton F. Cerebral infarction in a dog. Prog Vet Neurol. 1992;3:120–5.
29. Schmidt C, Frahm C, Schneble N, Muller JP, Brodhun M, Franco I, et al. Phosphoinositide 3-kinase gamma restrains neurotoxic effects of microglia after focal brain ischemia. Mol Neurobiol. 2015. doi:10.1007/ s12035-015-9472-z.
30. Lalancette-Hebert M, Gowing G, Simard A, Weng YC, Kriz J. Selective ablation of proliferating microglial cells exacerbates ischemic injury in the brain. J Neurosci. 2007;27:2596-605.
31. Nayak D, Roth TL, McGavern DB. Microglia development and function. Annu Rev Immunol. 2014;32:367–402.
32. Wirenfeldt M, Babcock AA, Vinters HV. Microglia insights into immune system structure, function, and reactivity in the central nervous system. Histol Histopathol. 2011;26:519–30.
33. Mena H, Cadavid D, Rushing EJ. Human cerebral infarct: a proposed histopathologic classification based on 137 cases. Acta Neuropathol. 2004;108:524–30.
34. Chuaqui R, Tapia J. Histologic assessment of the age of recent brain infarcts in man. J Neuropathol Exp Neurol. 1993;52:481–9.
35. Jin R, Yang G, Li G. Inflammatory mechanisms in ischemic stroke: role of inflammatory cells. J Leukoc Biol. 2010;87:779–89.
36. Lambertsen KL, Meldgaard M, Ladeby R, Finsen B. A quantitative study of microglial-macrophage synthesis of tumor necrosis factor during acute and late focal cerebral ischemia in mice. J Cereb Blood Flow Metab. 2005;25:119–35.
37. Davalos D, Grutzendler J, Yang G, Kim JV, Zuo Y, Jung S, et al. ATP mediates rapid microglial response to local brain injury in vivo. Nat Neurosci. 2005;8:752–8.
38. Nimmerjahn A, Kirchhoff F, Helmchen F. Resting microglial cells are highly dynamic surveillants of brain parenchyma in vivo. Science. 2005;308:1314–8.
39. Streit WJ, Walter SA, Pennell NA. Reactive microgliosis. Prog Neurobiol. 1999;57:563–81.
40. Benakis C, Garcia-Bonilla L, Iadecola C, Anrather J. The role of microglia and myeloid immune cells in acute cerebral ischemia. Front Cell Neurosci. 2015;8:461.
41. Hanisch UK, Kettenmann H. Microglia: active sensor and versatile effector cells in the normal and pathologic brain. Nat Neurosci. 2007;10:1387–94.
42. Adelson JD, Barreto GE, Xu L, Kim T, Brott BK, Ouyang YB, et al. Neu- roprotection from stroke in the absence of MHCI or PirB. Neuron. 2012;73:1100–7.
43. Rao VL, Dogan A, Todd KG, Bowen KK, Kim BT, Rothstein JD, et al. Antisense knockdown of the glial glutamate transporter GLT-1, but not the neuronal glutamate transporter EAAC1, exacerbates transient focal cerebral ischemia-induced neuronal damage in rat brain. J Neurosci. 2001;21:1876–83.
44. Rao VL, Bowen KK, Dempsey RJ. Transient focal cerebral ischemia down- regulates glutamate transporters GLT-1 and EAAC1 expression in rat brain. Neurochem Res. 2001;26:497–502.
45. Gleichman AJ, Carmichael ST. Astrocytic therapies for neuronal repair in stroke. Neurosci Lett. 2014;565:47–52.
46. Lambertsen KL, Ostergaard K, Clausen BH, Hansen S, Stenvang J, Thorsen SB, et al. No effect of ablation of surfactant protein-D on acute cerebral infarction in mice. J Neuroinflamm. 2014. doi:10.1186/1742-2094-11-123.
47. Clausen BH, Lambertsen KL, Babcock AA, Holm TH, Dagnaes-Hansen F, Finsen B. Interleukin-1beta and tumor necrosis factor-alpha are expressed by different subsets of microglia and macrophages after ischemic stroke in mice. J Neuroinflamm. 2008. doi:10.1186/1742-2094-5-46.
48. Tu XK, Yang WZ, Shi SS, Wang CH, Zhang GL, Ni TR, et al. Spatio-temporal distribution of inflammatory reaction and expression of TLR2/4 signaling pathway in rat brain following permanent focal cerebral ischemia. Neurochem Res. 2010;35:1147–55.
49. Jickling GC, Liu D, Ander BP, Stamova B, Zhan X, Sharp FR. Targeting neutrophils in ischemic stroke: translational insights from experimental studies. J Cereb Blood Flow Metab. 2015;35:888–901.
50. Kalimo H, del Zoppo GJ, Paetau A, Lindsberg PJ. Polymorphonuclear neutrophil infiltration into ischemic infarctions: myth or truth? Acta Neuropathol. 2013;125:313–6.
51. Enzmann G, Mysiorek C, Gorina R, Cheng YJ, Ghavampour S, Hannocks MJ, et al. The neurovascular unit as a selective barrier to polymorphonuclear granulocyte (PMN) infiltration into the brain after ischemic injury. Acta Neuropathol. 2013;125:395–412.
52. HerzJ, Sabellek P, Lane TE, Gunzer M, Hermann DM, Doeppner TR. Role of neutrophils in exacerbation of brain injury after focal cerebral ischemia in hyperlipidemic mice. Stroke. 2015;46:2916–25.
53. Buck BH, Liebeskind DS, Saver JL, Bang OY, Yun SW, Starkman S, et al. Early neutrophilia is associated with volume of ischemic tissue in acute stroke. Stroke. 2008;39:355-60.
54. Perez-de-Puig I, Miro-Mur F, Ferrer-Ferrer M, Gelpi E, Pedragosa J, Justicia C, et al. Neutrophil recruitment to the brain in mouse and human ischemic stroke. Acta Neuropathol. 2015;129:239–57.
55. Mestas J, Hughes CC. Of mice and not men: differences between mouse and human immunology. J Immunol. 2004;172:2731–8.
56. Doeing DC, Borowicz JL, Crockett ET. Gender dimorphism in differential peripheral blood leukocyte counts in mice using cardiac, tail, foot, and saphenous vein puncture methods. BMC Clin Pathol. 2003;3:3.
57. Stockham SL, Scotte MA. Fundamentals of veterinary clinical pathology. Ames: Blackwell; 2008. p. 70.
58. Moser KM, Guisan M, Bartimmo EE, Longo AM, Harsanyi PG, Chiorazzi N. In vivo and post mortem dissolution rates of pulmonary emboli and venous thrombi in the dog. Circulation. 1973;48:170–8.
59. Alvarez-Sabfn J, Maisterra O, Santamarina E, Kase CS. Factors influencing haemorrhagic transformation in ischemic stroke. Lancet Neurol. 2013;12:689–705.
60. Olsen TS, Skriver EB, Herning M. Cause of cerebral infarction in the carotid territory. Its relation to the size and the location of the infarct and to the underlying vascular lesion. Stroke. 1985;16: 459–66.
61. Howells DW, Porritt MJ, Rewell SSJ, O’Collins V, Sena ES, van der Worp HB, et al. Different strokes for different folks: the rich diversity of animal models of focal cerebral ischemia. J Cereb Blood Flow Metab. 2010;30:1412–31.
62. Hossmann KA. Pathophysiological basis of translational stroke research. Folia Neuropathol. 2009;47:213–27.
63. Wessmann A, Chandler K, Garosi L. Ischaemic and haemorrhagic stroke in the dog. Vet J. 2009;180:290–303.
64. Garosi LS, McConnell JF. Ischaemic stroke in dogs and humans: a comparative review. J Small Anim Pract. 2005;46:521–9.
65. Wang Y, Liu G, Hong D, Chen F, Ji X, Cao G. White matter injury in ischemic stroke. Prog Neurobiol. 2016;141:45–60.
Источник: Acta Veterinaria Scandinavica (2017) 59:7. This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons license, and indicate if changes were made.
СВМ № 2/2017