В первой части статьи рассматривались вопросы этиопатогенеза хилоторакса у домашних плотоядных, тогда как во второй — лечение хилоторакса.
1. Лечение
Лечение хилоторакса осуществляют методами консервативной терапии и/или хирургии. Выбор каждого из методов определяется причиной заболевания, качеством кормления животного, а также преимуществом или недостатками типа лечения (табл. 1 в первой части).
Лечение всегда следует начинать с медикаментозной терапии, особенно когда хирургическое вмешательство вызывает сомнение.
1.1. Консервативное лечение
Оно, в основном, показано при травме грудного протока.
Было установлено, что рана грудного протока, вызванная экспериментально, рубцевалась спонтанно в течение семи–десяти дней (J. Berg, 1982). Консервативная терапия показана на первом этапе развития хилоторакса идиопатической природы.
Такой способ лечения пациента преследует две цели: снижение формирования хилёзного выпота и дренирование (выведение жидкости из плевральной полости). Под этим подразумевают ограничение физических нагрузок, периодическое или постоянное выведение содержимого плевральной полости для обеспечения нормального функционирования респираторного аппарата, а также введение рациона, обеднённого жиром, обогащённого белками и жирорастворимыми витаминами.
До недавнего времени с целью улучшения кормления рекомендовалось включение в рацион кормовых добавок триглицеридов со средними цепями жирных кислот (ТСЦЖК) (каприловая, капроновая кислоты и т. д.), так как предполагалось, что они полностью абсорбируются в портальную систему без формирования хиломикронов (C.B. Quick, 1980). На сегодняшний день стало известно, что только некоторые ТСЦЖК включаются в хиломикроны, и, следовательно, ТСЦЖК вводить в рацион дополнительно не следует (D.A. Sikkema et coll., 1993). Добавление в корм дериватов (производных) флавоноидов, например, рутина гидрат, было показано для рациона, обеднённого жирами (S.J. Birchard et coll., 1995, 1998). Молекулы этого вещества, относящегося к группе бензопиронов, стимулировали бы тканевые макрофаги, обеспечивая таким образом повышение протеолиза и повторное улавливание через лимфатические капилляры (S.J. Birchard et coll., 1998). Этот препарат, назначаемый из расчёта 0,25–1 г перорально три раза в сутки, даёт обнадёживающие результаты при лечении кошки, но отдалённое исследование и число публикаций (четыре случая у кошки и два у собаки) недостаточны для доказательства эффективности такого способа лечения. У человека описан один случай ремиссии во время лечения постхирургического хилоторакса путём назначения соматостатина (C.G. Christensen, H.E. Evans, 1964). Механизм действия препарата, обладающего нейрогормональными и паракринными свойствами, заключается в способности вызывать снижение дебета печени и кишечника (C.G. Christensen, H.E. Evans, 1964).
В некоторых случаях развития хилоторакса возникает необходимость поддерживать функцию респираторного аппарата. Этого добиваются путём дополнительного введения кислорода пациенту, испытывающему тяжёлое состояние респираторного дефицита. Однако наиболее распространённым и вполне благоприятным способом облегчения его функциональной деятельности является торакоцентез.
Объектом терапевтического исследования у человека при хилотораксе является принудительная вентиляция лёгких. Она основана на увеличении давления в нижнем отделе дыхательных путей (бронхиолах и альвеолах) путём поддержания положительного давления при выдохе (E.C. Orton, 1993). Таким образом удаётся сохранить большой объём лёгких, обеспечивая тем самым коллабирование (спадение или закрытие) бреши в грудном протоке.
Этот способ требует применения аппарата ИВЛ, и, следовательно, в ветеринарной медицине он мало приемлем в связи с тем, что пациент должен находиться под анестезией в течение нескольких дней.
Иногда возникает необходимость прибегнуть к энтеральному питанию, так как животное часто страдает анорексией и отказывается принимать корм самостоятельно. В этом случае можно прибегнуть к простому введению назогастрального зонда.
Необходимо проводить контроль электролитного состава и кислотно-щелочного равновесия, которые изменяются в связи с выраженной утечкой хилёзной жидкости. Биохимический анализ крови (общий белок, гематокрит, электролиты и т. д.) выполняют один раз в два-три дня.
Применение кортикостероидов противопоказано. Некоторые авторы, тем не менее, рекомендуют их использование в случае осложнений (плевриты, заболевания аутоиммунной природы), устраняемых при назначении данной группы лекарственных препаратов (K.G. Kagan, E.M. Breznock, 1979). Кортикостероидную терапию проводят один раз в два дня, через неделю с момента их возникновения. Назначение антибиотиков (цефалоспорины и т. д.) авторы рекомендуют в случае введения дренажа в грудную полость, при котором может произойти контаминация у животных с ослабленным иммунитетом.
Применение диуретиков (фуросемид, сочетание алтизида со спиронолактоном) также показано и в отдельных случаях даёт результаты в начале заболевания (S. Jaque et coll., 1978; N.L. Browse et coll., 1974).
1.2. Хирургическое лечение
Принятие решения о проведении операции животному, страдающему хилотораксом, осуществляют индивидуально. В одном из проведённых исследований высказывается достаточно неопределённое мнение в отношении выбора оптимального времени проведения хирургического вмешательства (H. Chad, H. Brechtelsbauer, 1977). Тем не менее, авторы однозначно утверждают, что хирургическое лечение следует предлагать в отсутствие положительного результата (выраженного снижения объёма выпота хилёзной жидкости) в случае проведения консервативной терапии животного, испытывающего состояние интенсивного катаболизма (наличие выраженной гипопротеинемии, вызванной секвестрацией вследствие хилоторакса или нарушением рациона) (J. Lindena, I. Traudschold, 1983). При этом различают несколько методов хирургического лечения, которые могут носить комбинированный характер.
1.2.1. Перкутанное введение дренажа в грудную полость
Процедура основана на введении дренажа в грудную полость (табл. 1). С помощью этого способа удаётся длительно или временно удалять образующийся выпот из грудной полости. Чаще всего это проводят в сочетании с консервативной терапией. Эти мероприятия могут быть вполне достаточными для того, чтобы получить положительные результаты в лечении некоторых случаев возникновения хилоторакса (вторичного или вследствие травмы).
| Таблица 1. Введение дренажа в грудную полость |
| 1. Разрез кожного покрова на уровне 9–10-го межрёберного пространства. |
| 2. После проведения туннелизации в кожном покрове необходимо пройти сквозь грудную клетку на уровне 7–8-го межрёберного пространства, на границе средней и вентральной трети его высоты.
2.1. Введение дренажа осуществляют с помощью изогнутого гемостатического пинцета: после разреза кожного покрова дренаж для введения в грудную полость фиксируют изогнутым пинцетом, проводят туннелизацию под кожей протяжённостью, равной 2–3 межрёберным пространствам, через межрёберные мышцы. Дренаж вводят под контролем, избегая риска обширного отслоения плевры, выраженных повреждений межрёберных мышц и разрыва лёгкого. |
| 3. В плевральной полости дренаж не должен продвигаться далее второго ребра. |
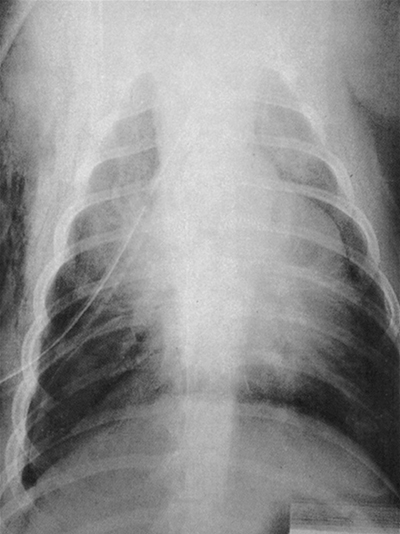
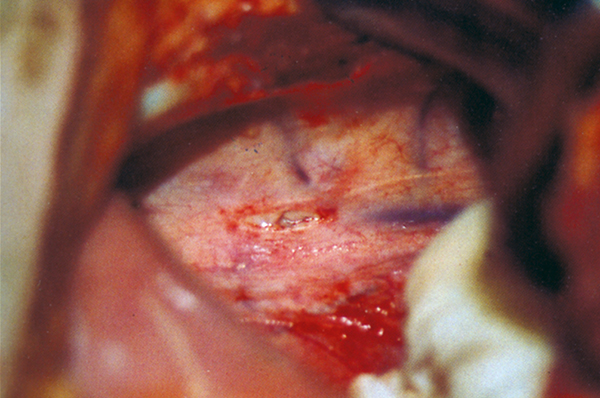
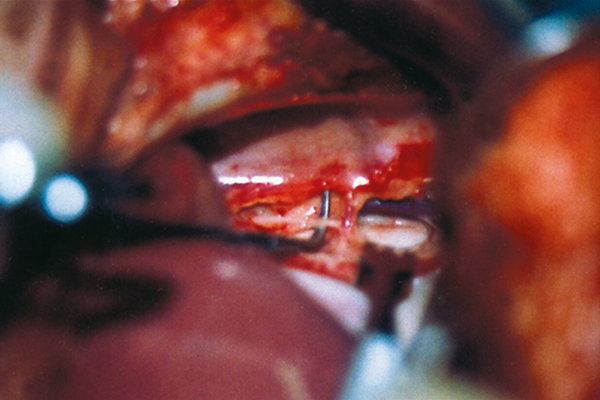
Авторы предпочитают непрерывное дренирование с помощью клапана Хеймлиха или Берла (фото 1). Выверку позиции дренажа осуществляют методом рентгенографии (фото 2) и дренаж оставляют до того момента, когда количество выделяемой жидкости в сутки составит объём ниже 2 мл/кг.
1.2.2. Лигирование грудного протока
Это метод был приоритетным, и его применяли на протяжении многих лет (J. Lindena, I. Trautchold, 1983; S.J. Birchard et coll., 1982; R.L. Meadows, P.S. McWilliams, 1994; T.W. Fossum, S.J. Birchard, 1986; J.L. Gookin, C.E. Atkins, 1999). В результате проведения отдельных ретроспективных исследований было показано, что в целом улучшение состояния при лигировании грудного протока составляет 50–60% у собак и 20% у кошек (S.A. Bibrey, S.J. Birchard, 1994). В описанных случаях, в основном, подобное вмешательство было необходимо при хилотораксе идиопатической природы (K.G. Kagan, E.M. Breznock, 1979).
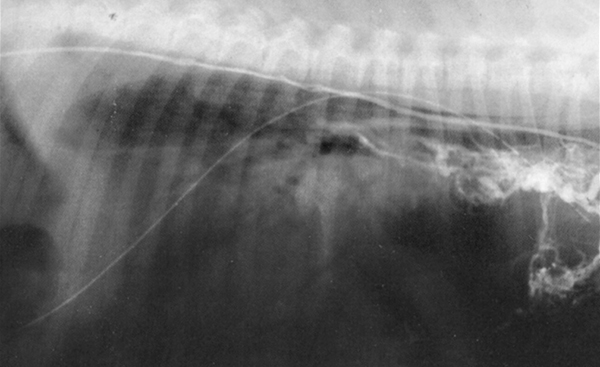
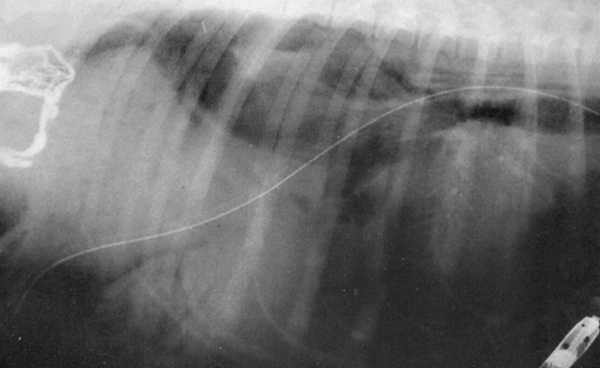
При этом до операции (фото 3а) и после её проведения (фото 3б) рекомендуется выполнять лимфангиографическое исследование, что позволяет оценить качество лигирования коллатералей и исключить тем самым риск возможного рецидива хилоторакса. Однако формирование заместительных коллатералей лимфатической системы после лигирования может в отдельных случаях привести к повторному образованию хилёзного или, что бывает чаще, серозно-геморрагического выпота (J. Lindena, I. Trautchold, 1983; S.J. Birchard et coll., 1982).
Техника лигирования грудного протока описана в таблице 2.
| Таблица 2. Метод хирургического лигирования грудного протока |
| 1. Торакотомия на уровне 10-го межрёберного пространства с правой стороны у собаки и на уровне 11-го межрёберного пространства с левой стороны у кошки. |
| 2. Надрез париетального листка плевры после отведения каудальной доли лёгкого. |
| 3. Осторожное, атравматическое отделение грудного протока. При выраженном плеврите, который осложняет отделение грудного протока, препаровку последнего следует проводить аккуратно, чтобы не допустить травмирования очень чувствительного к механическому воздействию грудного протока. |
| 4. Лигирование грудного протока осуществляют с помощью нити, которая должна иметь соответствующий диаметр (dec 3), или с помощью гемостатических клипсов, выполненных из металла или биологического рассасывающегося материала. Лигирование предназначено для блокирования грудного протока и его коллатералей (J. Hovard et coll., 2000). В случае выраженного фиброза лигатуру накладывают на непарную вену (vena azigos). |
| 5. Наложение грудного дренажа (см. табл. 1). Временное дренирование каждые четыре часа или постоянное. |
| 6. Выпот резорбируется через 3–7 дней. |
У собаки для осуществления данной манипуляции прибегают к правосторонней торакотомии (фото 4а и 4б), тогда как у кошки — к левосторонней. Также у представителей этого вида возможен трансдиафрагмальный доступ (J.R. Elk, G.A. Laine, 1990). По данным авторов, этот доступ обеспечивает лучшую визуализацию, что создаёт оптимальные условия выбора необходимого участка для лигирования грудного протока у кошки (краниально по отношению к хиатусу аорты).
Векурониум (Norcuron R), обладающий курареподобными и недеполяризирующими свойствами со средним действием во времени, может обеспечить условие для лигирования сосудов очень близко от верхушки диафрагмы, не оказывая побочного эффекта на функциональную деятельность респираторного аппарата (R.L. Meadows, P.S. McWilliams, 1994).
Ретроспективных исследований результатов лигирования грудного протока немного. S.J. Birchard (1982), проведя наблюдение пятнадцати лигирований у собак, установил, что положительный эффект от такого типа вмешательства составляет 60%.
Другие методы облитерации грудного протока, фигурирующие в литературе, носят скорее анекдотический характер. Pardo (1996) описывает эмболизацию грудного протока, создаваемую с помощью цианакрилатного клея, вводимого через катетер в мезентериальный лимфатический сосуд (как это происходит при лимфангиографии). Об эмболизации грудного протока с помощью металлической стружки (в том числе платиновой), вводимой перкутанно, также сообщается в литературе (T.W. Fossum et coll., 1991). С помощью этого метода тромбоз грудного протока был вызван у четырёх животных из шести.
Основным осложнением при лечении хилоторакса методом облитерации грудного протока является его рецидив за счёт нелигированных коллатералей, образовавшихся вторично после хирургического вмешательства. Экспериментально было доказано, что вторичные коллатерали замещают функцию грудного протока через пять–десять дней после лигирования (S.T. Kerpsach et coll., 1994). В связи с этим возникает необходимость провести повторное хирургическое вмешательство для лигирования коллатералей или грудного протока несколько ближе к верхушке диафрагмы либо прибегнуть к осуществлению плевровенозного и/или плевроперитонеального дренирования.
Другая форма осложнения проявляется в скоплении хилёзной жидкости под кожей на уровне задних конечностей (M.S. Williams, K.D. Josephson, 1997). Это осложнение возникает вследствие нарушения компенсаторной функции дренирования грудного протока через лимфатические капилляры. Скопление жидкости возникнет в момент лимфангиэктазии в более верхней части верхушки диафрагмы по отношению к месту наложения шва.
1.2.3. Плевроперитонеальное дренирование
К этому методу редко прибегают в начале лечения хилоторакса, но чаще при его рецидивах. Существуют два типа дренирования.
Активное дренирование
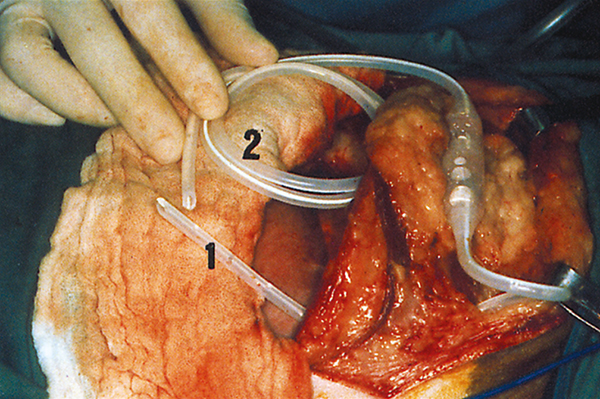
Этот способ основан на введении клапана, который за счёт снижения давления обеспечивает направленное движение жидкости из грудной полости в перитонеальную (P.F. Sutter, R. Greene, 1997). В данном случае мы можем использовать клапан Денвера (фото 5а и 5б).
Этот клапан также может быть использован для плевровенозного дренирования (T.W. Fossum et coll., 1986, см. далее). При этом необходимо учитывать, что эфферентный катетер не должен быть перфорированным. В таблице 3 резюмируется метод введения клапана Денвера для плевроперитонеального дренирования (ППД). Животные достаточно хорошо переносят ППД. Тем не менее, существует описание случая рецидива клинических признаков в виде диспноэ у собаки (четыре года назад подвергнутой плевроперитонеальному дренированию) вследствие формирования перегородки на уровне плевры, несмотря на то что последняя могла вступить во взаимодействие с дренажем (D. Stobie, J.L. Carponter, 1993).
| Таблица 3. Метод активного дренирования — плевроперитонеального или плевровенозного (клапан Денвера). Клапан Денвера (Денвер, выполненный из биоматериала, реализуется через Bernas Medical, Paris) — это система, основанная на использовании афферентного (перфорированного) и эфферентного (неперфорированного) катетеров (плевроперитонеальный и плевровенозный) диаметром 5 мм, соединённых необратимо с насосом, снижающим давление. При этом ни один из составляющих элементов клапана не оставляют вне организма пациента. При этом под кожей пальпируется один лишь насос. |
| 1. Надрез кожного покрова выполняют на уровне 7-го и 12-го межрёберного пространства. |
| 2. Плевральную (афферентную) часть дренажа проводят под кожей от места её надреза, расположенного каудально, до краниального надреза и фиксируют в плевральном пространстве при прохождении сквозь мускулы грудной клетки. |
| 3. Насос помещают под кожу между двумя кожными надрезами и опирают на ребро, чтобы иметь возможность осуществлять на него нажатие. |
| 4. Насос фиксируют под кожной клетчаткой с помощью нерассасывающегося шовного материала. |
| 5. Перитонеальную (эфферентную) часть дренажа, преимущественно перфорированную, вводят под кожу, начиная от места её надреза по отношению к 12-му межрёберному пространству вплоть до брюшной полости. |
| 6. Дренаж вводят в перитонеальную полость через небольшой надрез. |
| 7. На насос, помещённый на ребро, осуществляют нажатие 200–400 раз 3–4 раза в сутки. |
|
В случае плевровенозного дренирования эфферентную часть дренажа располагают следующим образом: 8. Проводят вышеописанным способом до полой вены. |
| 9. Фиксируют в полой или непарной венах с помощью двух швов в форме кисета (швы предпочтительно накладывать до введения катетера, затем завязывать по типу китайской шнуровки, то есть обвивным способом). |
| 10. Насос помещают на ребро и сжимают 200–400 раз 3–4 раза в сутки. |
Пассивное дренирование
Оно основано на трансдиафрагмальном сообщении плевральной полости с перитонеальной (D. Stobie, J.L. Carpenter, 1993; S. D. Forester et coll., 1991). Такой тип дренирования осуществляется опосредованно, через решётчатое окно, выполненное из силиконовой сетки, фиксируемой к диафрагме после удаления её фрагмента. Жидкость проходит из одной полости в другую благодаря респираторным движениям. Основным осложнением такого способа вмешательства является обструкция имплантированной сетки фибрином или большим сальником. Кроме того, можно наблюдать инфицирование или дилатацию живота по причине скопления жидкости вследствие нарушения её абсорбции брюшиной.
1.2.4. Плевровенозное дренирование
Плевровенозное дренирование основано на соединении плевральной полости с каудальной полой или непарной веной (табл. 3) (T.W. Fossum et coll., 1986).
При этом используют клапаны, идентичные таковым, предназначенным для обеспечения активного плевроперитонеального дренирования. В постоперационный период, в течение трёх–шести недель с момента проведения операции, животному назначают антикоагулянты (аспирин 10 мг/кг/сутки для собаки) с целью профилактики риска венозного тромбирования, эту терапию могут продолжать на протяжении трёх–шести месяцев после проведения хирургической операции. Описан случай удаления катетера вследствие тромбоза полой вены у собаки, возникшего в результате имплантации этой системы (J.E. Walgrop et coll., 2001). После изъятия катетера из полой вены плевровенозное дренирование стало носить менее активный плевроперитонеальный характер.
1.2.5. Плевродез
Плевродез — это полная адгезия висцерального и париетального листков плевры всей поверхности внутренней стенки грудной полости. Применение данного метода показано при возникновении рецидивов хилоторакса, а также этим методом пользуются для дополнения лигирования грудного протока, в основном, у кошек.
Данный метод основан на использовании химического или механического воздействия на плевру (табл. 4). Химическое воздействие осуществляют путём применения порошка талька или тетрациклина (T.W. Fossum et coll., 1994).
| Таблица 4. Выполнение плевродеза. | |
| А. Способ химического воздействия | В. Механическое воздействие |
| 1. В плевральную полость вводят от 40 мг/кг тетрациклина (плюс лидокаин 0,25%) или стерильный тальк из расчёта 80–105 мг/кг (1 г стерильного талька в форме пудры необходимо развести в 100 мл физиологического раствора). | 1. Абразия (выскабливание) двух плевральных листков сухой салфеткой. |
| 2. Доступ осуществляют методом стернотомии, которая даёт возможность проникновения ко всей поверхности плевры. Этот метод иногда дополняют плеврэктомией (или декортикацией*). | |
| 2. Вводят 200 мл воздуха для улучшения контакта антибиотика с плеврой. | 3. Возможно сочетание химического и механического методов. |
| 3. Активное непрерывное дренирование плевральной полости проводят до момента прекращения эффузии (выпотевания). | 4. Непрерывное активное дренирование плевральной полости осуществляют до момента прекращения эффузии. |
| * Декортикация — сложновыполнимая, требующая особой осторожности манипуляция, во время проведения которой очень часто возникает повреждение паренхимы, кроме того, при её проведении необходимо осуществлять дренирование. В связи с этим данный метод забыт как дополнительный метод лечения при проведении плевродеза, но находит применение при лечении констриктивного плеврита. | |
Результаты лечения хилоторакса у собаки и кошки, полученные при таком способе воздействия, носят противоречивый характер. Что касается экспериментального исследования плевродеза, проведённого химическим и механическим способами, то была отмечена более выраженная и вполне достаточная эффективность последнего, то есть механического способа (S.J. Birchard et coll., 1986), максимальная адгезия которого равнялась 21%.
В исследовании B.J. Gavaghan et coll. (1997), основанном на применении талька путём помещения его в плевральную полость под контролем торакоскопии, удалось добиться более выраженной адгезии, в сравнении с механической абразией (выскабливанием). Плевродез, осуществляемый механически, нуждается в проведении стернотомии, в то время как для химического способа можно воспользоваться методом дренирования.
Для осуществления механического плевродеза прибегают к использованию высокоэффективных анальгетиков (буторфанола или других производных морфина), необходимых для снятия сильной боли, связанной с проведением хирургической операции.
В исследованиях P. Jerram (1986) из пяти собак, подвергнутых плевродезу химическим способом, только одна нуждалась в проведении аналгезии.
Во всех случаях плевродеза необходимо применение активного и постоянного дренирования плевральной полости вплоть до исчезновения эффузии (выпотевания).
1.2.6. Использование сальника
В литературе имеется лишь одно описание метода применения сальника для лечения хилоторакса у собаки (J.S. Ikonomidis et coll., 1997). Доступ в грудную и брюшную полости осуществляли паракостально. Сальник вводили в грудную полость через разрез, сделанный в рёберной части диафрагмы, и фиксировали в краниальной части грудной клетки. Плеврального выпота у собаки не наблюдали 14 месяцев. Данный метод является перспективным, и применение его особенно рекомендуется при развитии плеврита взамен лигирования грудного протока, потому что последний обнаружить в этой ситуации очень трудно.
1.2.7. Устранение первопричины заболевания
Лечение, направленное на устранение первопричины данной патологии (нарушение функциональной деятельности сердца, неоплазия, поражение грибковой природы и т. д.), в настоящем источнике не детализируется. В данной ситуации прибегают к методам химио- (винкристин, преднизолон) и радиотерапии лимфом или лимфосарком у кошки (A.R. Selser et coll., 1997), применению специфического лечения заболевания сердца (хирургия или химиотерапия при хемодектоме, IECA или дигоксин, фуросемид при кардиомиопатиях и т. д., как сообщают об этом E.R. Graber в 1964 и N.L. Browse et coll., 1974) и использованию противогрибковых препаратов (итраконазол) при развитии фунгоидной гранулёмы (S.J. Birchard et coll., 1998).
1.2.8. Лечение в постоперационный период
Дренирование после проведения хирургической операции на грудной клетке, как это упоминалось выше, проводят постоянно. Для слишком ослабленных животных в постоперационный период осуществляют принудительное поддерживающее питание (парентеральное, энтеральное и смешанное). Животным, у которых отмечали анорексию до проведения операции, с профилактической целью вводят зонд методами эзофагостомии или гастростомии.
2. Прогноз
Прогноз при хилотораксе крайне сдержанный. В том, что лечение оказалось эффективным, можно быть уверенным лишь спустя несколько лет; рецидивы хилоторакса наблюдали даже через пять лет после проведения хирургической операции (K.G. Kagan, E.M. Breznock, 1979).
3. Осложнения
Кроме того, что прогноз заболевания неблагоприятный, разрушающее воздействие хилёзного выпота приводит к деградации общего состояния организма животного и даёт начало развитию осложнений.
3.1. Нарушение усвояемости, анорексия, кахексия
Такую клиническую картину часто наблюдают у животных в постоперационный период или с ярко выраженным выпотом.
На первом этапе потеря веса вызвана удерживанием в выпоте белков, жиров и электролитов, компенсированных интенсивным катаболизмом протеинов печени, скелетной мускулатуры и желудочно-кишечного тракта. На конечном этапе у животного отмечают слабость, заметное снижение мышечной массы, падение интенсивности образования ферментов в системе пищеварения, инволюцию паренхимы печени и слизистой желудочно-кишечного тракта (C.A. Stonesifer, W.F. Moffet, 1974). Эти изменения приводят к ухудшению общего состояния организма — слабости и анорексии. Слабость мышечной ткани (в основном межрёберных мускулов) приводит к нарушению дыхания, вызванного выпотом в грудной полости. Снижение иммунитета возникает вследствие нарушения кормления и секвестрации в грудной клетке большого количества лимфоцитов (C.A. Stonesifer, W.F. Moffet, 1974).
Снижение сывороточной концентрации альбумина наблюдают, в среднем, через неделю с момента развития хилоторакса. Это является причиной падения онкотического давления, вследствие чего отмечают выраженное снижение резорбции в организм жидкости из плевральной полости и нутриентов из желудочно-кишечного тракта. Это приводит к дефициту энергии, источниками которой являются белки и жиры (C.A. Stonesifer, W.F. Moffet, 1974).
По данным J.E. Meineke et coll. (1969), потеря электролитного состава объясняется гипонатриемией и гиперкалиемией, приобретённой вследствие нарушения экскреции калия почками.
3.2. Плеврит
Обычно хилёзная жидкость не вызывает воспаления. Тем не менее, у некоторых животных, страдающих хилотораксом, развивается плеврит, который может быть достаточно выраженным (R.L. Meadows et coll., 1993). Наблюдают его в основном у кошек, где он может иметь рестриктивный характер и стать драматическим (D.F. Peterson, T.D. Munson, 1958).
Его развитие подозревают при наличии или усугублении диспноэ, несмотря на полное дренирование хилоторакса. В ретроспективном исследовании пятнадцати случаев хилоторакса у кошек констриктивный плеврит (налёт коллагена и фибрина на плевре) был выявлен у 67% животных (D.F. Peterson, T.D. Munson, 1958).
При этом было отмечено, что плевра утолщается и вызывает компрессию долей лёгких. Затем паренхима лёгких подвергается ателектазу, и мышечная ткань бронхиол подвергается гипертрофии. Дыхание становится крайне затруднённым.
Прогноз при такой форме хилоторакса крайне сомнительный, и выживаемость пациентов в течение нескольких недель после постановки диагноза (максимум — один год) не превышает 30% (D.F. Peterson, T.D. Munson, 1958).
В ветеринарной медицине, в отличие от гуманитарной, лечение пациентов путём плевротомии и удаления вновь образованного на плевре фиброзного слоя (декортикация) проводят очень редко, в связи со сложностью выполнения данной манипуляции у животных (M.D. Willard, J.D. Conroy, 1985). Лечение, основанное на применении преднизона, может привести к более успешным результатам, чем плеврэктомия (D.F. Peterson, T.D. Munson, 1958).
3.3. Констриктивный перикардит
Значительно реже в сравнении с вышеназванными формами осложнений хилоторакса наблюдают хроническое воспаление серозных оболочек других органов грудной полости, в основном, перикарда (J. Hovard et coll., 2000). Имеется лишь один клинический случай, описанный у собаки. Физическая нагрузка усиливает развитие процесса и в конечном итоге приводит к развитию недостаточности сердца.
4. Резюме
В таблице 5 приведено общее руководство по диагностике и лечению хилоторакса у собаки и кошки.
| Таблица 5. Руководство при подозрении развития хилоторакса у собаки и кошки (модификация по Smeac D.D., Kerpsac S.J., 1995). |
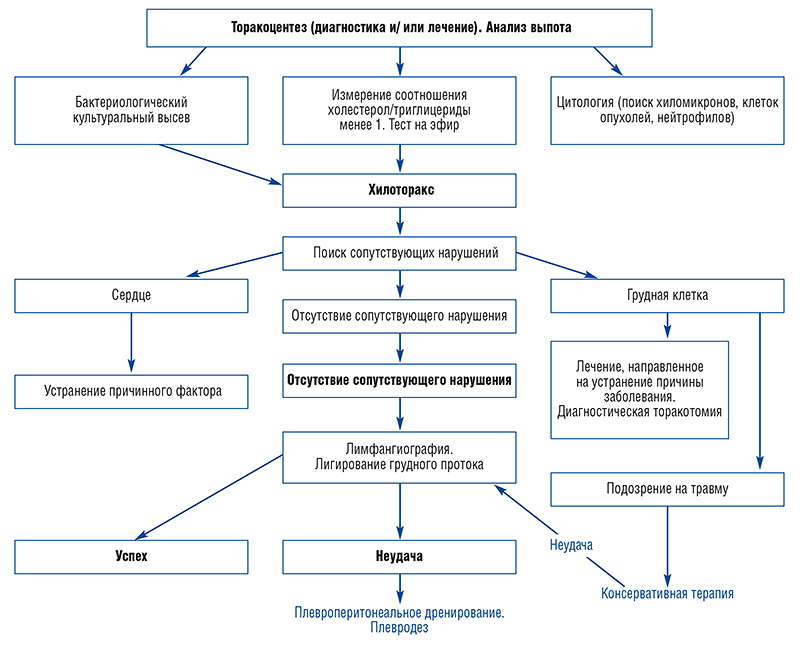 |
Торакоцентез остаётся основным методом исследования при постановке диагноза на хилоторакс. При выборе методов лечения изучают причину заболевания. Начинают лечение методами консервативной терапии и при отсутствии положительных результатов переходят к хирургии. Согласно наблюдениям, при рецидиве заболевания, наступившем через месяц, в течение которого проводилось лечение (дренирование грудной клетки, адаптированное питание) или после прерывания лечебного курса, необходимо проведение хирургической операции.
В первую очередь всегда выполняют лигирование грудного протока, за исключением тех случаев, при которых выраженный плеврит у животного не даёт возможности визуализировать грудной проток. Другие методы хирургического вмешательства, которые выполняют отдельно или как дополнение к лигированию грудного протока — это плевродез, а также введение и фиксация плевроперитонеального или плевровенозного клапанов.
Заключение
Хилоторакс — это нарушение, которое является ловушкой для многих публикаций. Постановка диагноза на хилоторакс сложности не представляет, её осуществляют простым методом торакоцентеза и анализом полученного жидкого выпота. Однако причины возникновения заболевания недостаточно изучены, несмотря на возможность проведения лимфангиографии, с помощью которой установлено, что аккумуляция жидкости вызвана в основном лимфангиэктазией, а нарушения целостности грудного протока встречаются крайне редко.
Возникновение вторичного хилоторакса может быть следствием каких-либо первичных нарушений, которые должны стать предметом всестороннего изучения.
Лечение хилоторакса всегда даёт нестабильные результаты, несмотря на использование дополнительных методов, таких как лигирование грудного протока. Кроме того, анатомическая топография грудного протока у разных пациентов имеет свои вариации, наличие которых иногда приводит к допущению врачебных ошибок в процессе лигирования грудного протока. Таким образом, прогноз выживаемости при данном заболевании на средний и длительный период жизни пациента сдержанный или неблагоприятный.
СВМ 2/2007