Методы визуальной диагностики
Визуальные (визуализирующие) методы диагностики (ВМД) (табл. 1 и 2) являются неотъемлемой частью стандартного клинического исследования пациентов с подозрениями на заболевания мочевыделительной системы (МВС). Визуальная диагностика тем более актуальна, что большинство нефропатий мелких домашних животных сопровождаются схожими клиническими проявлениями (если таковые вообще имеются[1]) и часто характеризуются однотипными изменениями в результатах лабораторных исследований биологических жидкостей (кровь, моча[2]).
Также выявление некоторых нефропатий может являться «случайной» находкой у пациентов, обследуемых при подозрении на другие патологии. Связано это с тем, что почки обладают огромными компенсаторными возможностями для поддержания гомеостаза организма даже на фоне серьёзных поражений своих паренхимы и структур.
Стандартное обследование животных с подозрениями на заболевания мочевыделительной системы (МВС)
- Сбор анамнеза (один из важных вопросов в котором — диагностировались ли у животного заболевания МВС ранее).
- Клинический осмотр и пальпация органов МВС.
- Общий и биохимический анализы крови.
- Анализ мочи общий (с микроскопией осадка) и по Нечипоренко, а также соотношение: белок мочи к креатинину мочи.
- УЗИ почек и мочевого пузыря.
- Бакпосев мочи (забор материала для исследования производится только путём пункции мочевого пузыря через брюшную стенку (чрезбрюшинный уроцистоцентез) при подозрении на инфекционные заболевания МВС).
- У кошек: исследование крови на вирусную лейкемию и вирусный иммунодефицит (лабораторное подтверждение у животного того или иного заболевания может кардинально изменить дальнейшую тактику ведения пациента).
ВМД можно разделить на морфологические и морфофункциональные. Морфологические ВМД используют в диагностике анатомических и структурных изменений органов МВС (УЗИ, обзорная рентгенография, компьютерная и магнитно-резонансная томография (КТ и МРТ)). Для морфофункциональной визуализации работы почек и мочевого тракта используют: выделительную урографию, различные виды сцинтиграфии, а также динамическую КТ, МРТ и магнитно-резонансную ангиографию (МРА).
При морфологических ВМД почек оценивается их количество, положение, размер, форма, контуры, структура паренхимы и почечного синуса (ПС). ПС образуют: почечная артерия и вена, нервные волокна и структуры лоханки с выходящим из неё мочеточником. При ультрасонографии ПС обычно называют центральным эхокомплексом (ЦЭ)[3] почки.
Морфологические ВМД также позволяют выявить анатомические аномалии почек, наличие конкрементов в паренхиме, лоханке и мочеточниках, жидкостные и опухолевые образования, а также изменения, характерные для некоторых острых и хронических нефропатий (как правило, без определения конкретной нозологической формы).
Морфофункциональная визуализация позволяет дать более полную характеристику пространственному расположению органов МВС и анатомическому строению структур мочевого тракта (от лоханки до мочевого пузыря), а также оценить выделительную и накопительную функцию каждой почки по отдельности и проследить перистальтику (или её отсутствие) мочеточников. А непрямая ангиография, проводимая в рамках выделительной сцинтиграфии, динамическая КТ, МРТ и магнитно-резонансная ангиография (МРА) являются современными методами для определения скоростных и объёмных характеристик почечного кровотока.
Ведущим морфологическим ВМД в ветеринарной нефрологии в силу относительной простоты и доступности, а также безопасности и отсутствия облучения при проведении является УЗИ. Этот метод широко используется как при диагностике нефропатий у пациентов с клиническими проявлениями, так и при скрининговых исследованиях (особенно среди породных животных, имеющих склонность к генетически наследуемым заболеваниям почек).
Вместе с тем ВМД (обычно УЗ-исследованиям) при выставлении нефрологических диагнозов может придаваться решающее значение. Но допустимо это далеко не всегда. С одной стороны, ВМД позволяют довольно точно дифференцировать нефропатии, сопровождающиеся макроструктурными изменениями почек. Но, с другой стороны, данные нефропатии занимают только около 5–10% от общего числа заболеваний, регистрируемых у кошек, и 20–35% регистрируемых у собак. Ни различные формы гломерулопатий (ГП) и гломерулонефритов (ГН), ни тубуло-интерстициальные нефриты (ТИН) и пиелонефриты даже на заключительных этапах своего течения не имеют характерных структурных изменений, визуализация которых позволила бы с высокой долей вероятности определить конкретную нозологическую форму заболевания. Выставление окончательных диагнозов в этом случае является прерогативой клинической гистопатологии и осуществляется прижизненно только после проведения нефробиопсии.
Кроме того, интерпретация результатов, получаемых при ВМД заболеваний почек и надпочечников, является достаточно трудной задачей для клиницистов ввиду сложности строения и широкой вариабельности размеров этих органов (даже внутри одного вида), а также многогранности и неоднозначности оценки получаемых при исследованиях изображений.
Таблица 1. ВМД в нефрологии, доступные для проведения в ветеринарных клиниках широкого профиля
| УЗИ (диагностическая сонография, ультрасонография) | |
| Получаемая информация или нефропатии, выявляемые при исследовании | Хорошее изображение почки независимо от её функционального состояния; определение её размера; оценка эхогенности почечной ткани; дифференцирует корковое и мозговое вещество почки (корково-медуллярная дифференциация); показывает полный контур и перинефральное пространство почек, позволяет оценить их размеры (в т.ч. в сравнении друг с другом); оценивает почечный кровоток при использовании метода Доплера (у собак и кошек данный метод актуален в большинстве случаев только в составе комплексной диагностики злокачественных новообразований); высокочувствительный метод диагностики, позволяющий выявить конкременты любого минерального состава (нефролитиаз) и жидкостные образования (кисты, гематомы, абсцессы) в паренхиме и ЦЭ; позволяет отдифференцировать кисты от твёрдых опухолей и соединительнотканных образований; определение перинефральных скоплений жидкости; ценный метод для диагностики постренальной ПН (обструкция нижних мочевыносящих путей, разрыв мочевого пузыря); может использоваться для визуализации процесса нефробиопсии, для мониторинга течения некоторых нефропатий (нефролитиаз, гидронефроз). |
| Недостатки | Очень часто клиническая ценность обследования зависит от квалификации, опыта и объективности врача, проводящего исследование; не даёт детальной визуализации почечных лоханок; не показывает нормальный мочеточник; существует вероятность невыявления мелких почечных конкрементов, особенно если они локализованы в дистальных участках мочеточников; не даёт информации о функциональном состоянии почек; требуется фиксация пациентов в определённых позах, частичное удаление шёрстного покрова (что вызывает протест у владельцев выставочных собак и кошек) и введение гипнотических препаратов (пропофол) агрессивным или стресс-неустойчивым животным (верно и для любых других ВМД). |
| Примечания | Является неотъемлемой частью стандартного нефрологического обследования пациентов с подозрениями на заболевания МВС; при исследовании нет необходимости в применении нефротоксичных рентгеноконтрастных веществ и облучения, что позволяет использовать УЗИ неограниченное число раз подряд; доступны, легки в исполнении, малотравматичны и имеют низкую стоимость; установки портативны и могут использоваться на дому у владельца животного; для диагностики разрыва мочевого пузыря через уретральный катетер вводится 0,9% раствор NaCl (при этом хорошо видно, как жидкость поступает в брюшную полость). |
| Урография (выделительная урография, контрастная урография, экскреторная урография) | |
| Получаемая информация или нефропатии, выявляемые при исследовании | Даёт максимально точное представление о пространственном расположении мочевыделительной системы по сравнению с другими методами визуальной диагностики; наиболее доступный метод, дающий представление о функциональном состоянии почек (экскрекция рентгеноконтрастного вещества возможна только в составе мочи) и моторной функции мочевых путей; наиболее ценный метод для диагностики обструкции мочеточников и их разрывов (в этом случае рентгеноконтрастное вещество попадает в брюшную полость) и связанной с этим постренальной ПН; ценный метод для диагностики открытых (т.е. открывающихся в лоханку) почечных кист; диагностика анатомических особенностей и патологий строения лоханки и мочевого пузыря; диагностика целостности мочеиспускательного канала после травм таза или падения с высоты. |
| Недостатки | Размещение рентгеновских аппаратов возможно далеко не во всех ветеринарных клиниках; рентгеноконтрастные (в нефрологии-урологии обычно рентгенопозитивные) вещества, используемые для данного метода диагностики, обладают нефротоксичностью и противопоказаны пациентам с почечной недостаточностью (ПН) и гиповолемией; это обстоятельство также не позволяет проводить исследование многократно; возможно развитие аллергических реакций на рентгеноконтрастные вещества; не позволяет диагностировать некоторые формы нефролитиаза (в случае, если конкременты рентгенопроницаемы (ураты и камни, образованные цистином)); не всегда позволяет дифференцировать закрытые (т.е. не связанные с лоханкой) кисты в почечной паренхиме; для получения более качественных изображений требует очищения кишечника, седации пациента внутривенным введением гипнотиков, в противном случае приводит к облучению владельцев, удерживающих животное в нужном положении во время съёмки. |
| Примечания | Обзорная рентгенограмма, обычно получаемая вместе с урографией, даёт представление о наличии осложнений, связанных с хронической ПН (например, почечной остеодистрофией), и процессах кальцификации в почечной паренхиме и мочевыводящих путях (конкременты, обызвествлённые опухоли). |
Таблица 2. Дорогостоящие и наукоёмкие ВМД
| Название метода | Получаемая информация или нефропатии, выявляемые при исследовании |
| Компьютерная томография (КТ) и спиральная КТ | Предпочтительнее, чем УЗИ, при диагностике плотных образований, особенно при подозрении на злокачественные опухоли почек. КТ позволяет определить распространённость опухоли, поражение лимфатических узлов, установить стадию онкологического процесса.
КТ также является методом выбора в диагностике травм почек. Отсутствие экскреции мочи, ушиб, разрыв, раздробление почки, периренальное скопление жидкости легко выявляются с помощью КТ. Одновременно предоставляется дополнительная информация о повреждении других органов. Используется для диагностики причин гидронефроза, когда более простые методы не дают результата. |
| Магнитно-резонансное исследование (МРИ) или магнитно-резонансная томография (МРТ) и магнитно-резонансная ангиография (МРА) | Эти методы используют в ветеринарной нефрологии в том случае, если другие визуальные методы исследования новообразований почек дают сомнительные результаты или требуется дополнительная оценка состояния почечного кровотока (в т. ч. интактных сосудов). |
| Реносцинтиграфия (радиоизотопная ренография) | У животных наиболее часто проводятся с целью:
|
| Исследования занимают много времени, требуют полной неподвижности и проводятся у животных, находящихся в медикаментозном сне. | |
Тактика выбора визуального метода диагностики при различных нефропатиях
Основной задачей ВМД при первичном обследовании пациентов (в подавляющем числе случаев это УЗИ) с подозрениями на заболевания почек, общем лечебно-профилактическом обследовании (например, перед хирургическими вмешательствами) или при скрининговых исследованиях является обнаружение нефропатий, имеющих характерные макроструктурные изменения (табл. 3). Выявление таких изменений позволяет с той или иной долей вероятности выставить окончательный нефрологический диагноз[4] и определить дальнейшую тактику обследования и лечения пациента.
Другие же неинвазивные методы диагностики помогают в установлении степени ПН у пациента (неазотемическая, азотемическая, уремическая или I–IV по классификации IRIS) и в выявлении осложнений основного заболевания (если таковые имеются). Исключение могут составлять случаи, когда при УЗИ у пациента выявляются солидные включения в паренхиме почек или в перенефральном пространстве. Для уточнения диагноза у таких пациентов целесообразно проведение КТ, МРТ, МРА (табл. 2), а также получение биоптата новообразования для цитологического и/или гистоморфологического исследования.
Когда же клинические данные и/или результаты лабораторных исследований позволяют предположить у пациента какую-либо нефропатию, а визуализация почек с помощью УЗИ либо не выявляет изменений вообще, либо даёт неспецифическую картину, возникает вопрос о тактике дальнейшего обследования пациента. Раньше всего следует внимательно проанализировать особенности анамнеза, результаты осмотра и изменения в результатах лабораторных исследований. И только после этого обращаться к другим ВМД. Причём при принятии решения о проведении ВМД следует обратить внимание на достоверность и ценность получаемой при конкретном исследовании информации, а также на их инвазивность и опасность для жизни и здоровья пациента (например, необходимость введения нефротоксичных контрастных веществ при рентгенографии или длительная седация с применением гипнотиков при МРТ и КТ).
Поэтому если информация, полученная при стандартном нефрологическом исследовании, достаточна для выставления клинического или даже окончательного диагноза пациенту, а терапевтическое лечение привело к улучшению общего состояния пациента и/или положительной динамике в результатах лабораторных показателей, то проведение дополнительных МВД можно считать нерациональным. Особенно это актуально для пациентов с тяжёлыми формами ПН. Немаловажным является и соотношение степени достоверности исследования и его ценности в диагностике нефропатии к его стоимости.
Таблица 3. Нефропатии, характеризующиеся яркими макроструктурными изменениями при УЗИ.
| Нефропатия | Характерные изменения, выявляемые при ВМД |
| Нефролитиаз | Гиперэхогенные включения различ. размера ярко-белого цвета в паренхиме и лоханке, дающие густую акустическую тень. Эхотень возникает вследствие значительного различия плотности почечной паренхимы и конкрементов, от которых и происходит максимальное отражение ультразвука. Местоположение конкремента определяется по месту начала эхотени. |
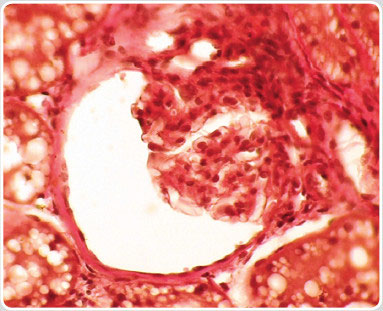
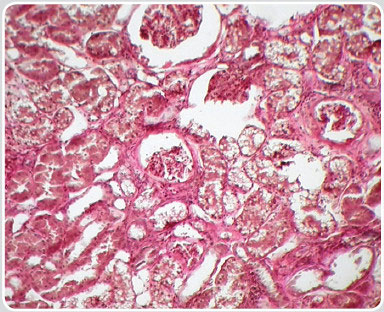
| Простые кисты почек | Имеют округлую форму и чётко выраженные ровные контуры. Также характеризуются отсутствием отражения ультразвуковой волны в пределах образования (гипоэхогенны) (фото 1.1 и 1.2). Поражения носят обычно односторонний характер. Клинически никак не проявляются. Посевы мочи не дают роста. Отклонения от нормы в лабораторных исследованиях биологических жидкостей появляются, только если у пациента имеются другие нефропатии. |
| Абсцессы почек и пионефроз | Как правило, имеют более толстые стенки и более эхогенное (гнойное) содержимое, чем кисты. Наличие в абсцессах хорошо визуализируемых пузырьков воздуха является веским признаком их инфекционной природы[5]. Для карбункулов же характерны неровные, как бы рваные края, которые выпячиваются наружу или в лоханку. Паренхима вокруг карбункулов имеет признаки воспаления (отёчность, нарушение структуры) или компрессии. Диагнозы считаются подтверждёнными только, если в посевах мочи, полученной чрезбрюшинным уроцистоцентезом, высевается патогенная микрофлора. |
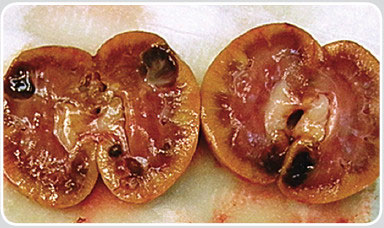
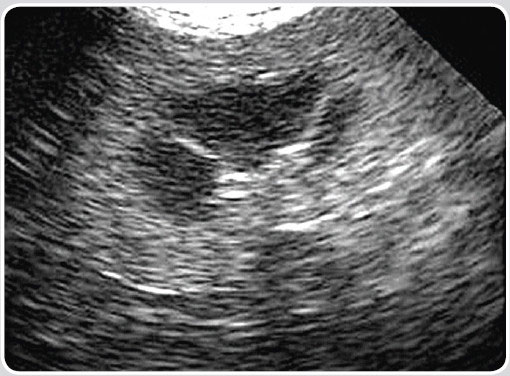
| Поликистоз почек | Различные по размеру множественные гипоэхогенные образования в корковом (у собак) и корковом и мозговом веществе (у кошек) обеих почек. Имеют круглую или овальную форму и заполнены жидкостным содержимым. Как правило, не меняют своей конфигурации после опорожнения мочевого пузыря (закрытые почечные кисты). На начальных этапах процесса УЗ-диагностика может быть затруднена, а само заболевание клинически никак не проявляться. В последующем признаки почечной недостаточности появляются, как правило, только после того, как атрофированными окажутся не менее 50% форменных элементов почки. На заключительных этапах поликистоза почек эти органы значительно увеличены в размерах и имеют крупноячеистое строение (фото 3.1, 3.2, 3.3). Поскольку поликистоз почек является генетически наследуемым заболеванием (причём не только у кошек персидской породы), то по возможности необходимо обследовать других животных, находящихся в близком родстве. Больные поликистозом почек животные должны быть исключены из разведения. Дифдиагноз: множественные мелкие абсцессы в паренхиме почек. У животных появление такого поражения паренхимы почек возникает обычно гематогенным путем и возможно только на фоне тяжелых иммунодефицитных состояний (например, вирусного перитонита кошек). В посевах мочи выявляют патогенную микрофлору. |
| Субкапсулярные гематомы и лимфоэкстравазаты | Жидкостные образования различного состава с гиперэхогенной взвесью и пузырьками воздуха (или без них) под капсулой почки. В отличие от гидронефроза ткани и структуры почки (если их не экранирует содержимое гематомы или гной и их возможно визуализировать) при этих патологиях частично или полностью сохранены (фото 5.1, 5.2, 5.3). |
| Неоплазия (в т.ч. с использованием цветного доплеровского сканирования) | Изменение формы и размера почек, нарушение кортико-медуллярной дифференциации в отдельных местах паренхимы одной, реже обеих почек. Возможно полное замещение тканей почки новообразованием (почечные структуры не визуализируются). Изменение картины почечного кровотока (особенно при новообразованиях с обильным кровоснабжением). Для подтверждения диагноза необходимо проведение КТ, МРТ, а также биопсии новообразования. Новообразования менее 1–3 мм (зависит от класса аппарата и квалификации врача, проводящего исследование) при УЗИ не визуализируются. Разумеется, многое зависит и от эхогенности тканей, которые опухоль образуют. |
| Гипоплазия (врождённая или приобретённая) | Значительное уменьшение в размерах одной или обеих почек. Парная гипоплазия почек не всегда является патологией и может быть вариантом нормы (внутривидовой полиморфизм размеров органов). Для уточнения диагноза следует обращаться к другим методам диагностики (радиоизотопная ренография). |
| Аплазия | Одна из почек не визуализируется. Аплазия почек обычно сочетается с недоразвитием или отсутствием её мочеточника. Для уточнения диагноза обычно рекомендуется проведение урографии. |
| Гидронефроз | Гидронефротическая трансформация лоханки (пиелоэктазия) и мочеточников, а также всей почки, если отток мочи затруднён длительное время. Подробнее см. схему 1. |
| Дистопия или аномалия положения почек | Значительное изменение положения почек относительно анатомической нормы. У собак и кошек, в отличие от человека, встречается редко и обычно не ведёт к нарушению функций этих органов. |
| Удвоение почек | Бывает одно- и двустороннее. Различают также неполное удвоение (у двух расположенных рядом (спаянных) почек общая лоханка и один мочеточник) и полное (у каждой почки своя лоханка и мочеточник; в этом случае можно говорить о том, что у животного три полноценные почки). УЗИ позволяет только предположить эту патологию. Уточняется она с помощью внутривенной урографии. |
УЗИ
УЗИ — неинвазивный метод отображения подкожных структур и органов при помощи не воспринимаемых человеческим ухом ультразвуковых волн, генерируемых датчиком (трансдуктором) по средствам пьезоэлектрического эффекта.
С момента появления УЗИ всё интенсивнее внедряется в клиническую практику, постепенно переходя в разряд рутинных методов диагностики. На сегодняшний день УЗИ, пожалуй, самый доступный ВМД в ветеринарной медицине в силу относительной простоты в использовании, невысокой стоимости обследования и безопасности для здоровья. В данной статье этот метод исследования будет рассмотрен более подробно ещё и потому, что диагностические принципы, лежащие в его основе, во многом верны и для других ВМД.
В нефрологии УЗИ МВ-системы является неотъемлемой частью стандартного обследования животных с подозрениями на нефропатии, поскольку позволяет «отсеять» пациентов с заболеваниями почек, которые сопровождаются яркими макроструктурными изменениями (табл. 3), или помогает в выборе дальнейшей тактики обследования. Однако отсутствие «видимых» изменений при УЗИ (равно как и при других визуальных методах исследования почек) не говорит о том, что у конкретного пациента нет угрожающей жизни нефропатии. Неазотемический этап может занимать до 90% времени течения почечного континуума и характеризуется не только отсутствием клинических проявлений, но и видимых при УЗИ структурных изменений в паренхиме и ЦЭ почек.
Одним из самых серьёзных ограничений при использовании УЗИ в ветеринарной нефрологии является неоднозначность интерпретации получаемых изображений. Изменения (или их отсутствие), описываемые в протоколе УЗИ, могут быть субъективным взглядом конкретного специалиста и не должны приниматься клиницистом как единственный источник информации при выставлении диагноза и назначении лечения. Немаловажным фактором достоверности при УЗИ являются компетентность специалиста, проводившего его, и уровень оборудования, которое при этом использовалось.
Поэтому в подавляющем числе случаев при постановке окончательного диагноза результаты ультрасонографии должны рассматриваться только в комплексе с клиническими данными, результатами неинвазивной, а в ряде случаев и инвазивной (аспирационная и/или пункционная биопсия) диагностики.
Методика проведения УЗИ в нефрологии и визуализируемые при этом основные макроструктурные характеристики органов МВС
УЗИ мочевой системы у собак и кошек проводится микроконвексным или конвексным датчиками с частотой 2,5–8,0 МГц и линейным датчиком с частотой 5,0–7,5 МГц. У животных, не страдающих ожирением, УЗИ при диагностике заболеваний мочевой системы может проводиться без предварительной голодной диеты и дачи ветрогонных препаратов (хотя эти мероприятия в некоторых случаях могут облегчить визуализацию как самих почек, так и других органов брюшной полости). Обязательными условиями является удаление шерсти с живота вплоть до последних рёбер (в противном случае ультразвук не пройдёт через воздушную прослойку, возникающую между датчиком и кожей, и изображение на экране не возникнет) и нанесение акустического геля на предварительно смоченную физиологическим раствором кожу. Агрессивным и пугливым животным для проведения УЗИ необходимо введение гипнотиков (препараты, вызывающие медикаментозный сон) с преимущественной конъюгацией в печени (пропофол).
| Клинический случай № 2. Кошка, ж., 8 лет |
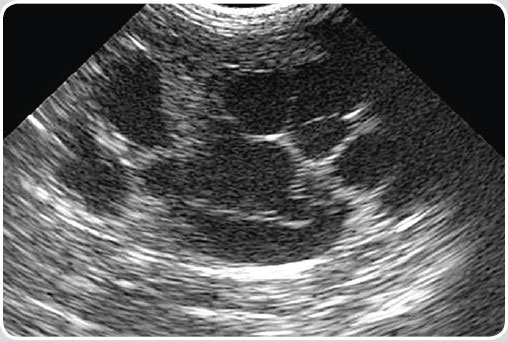 |
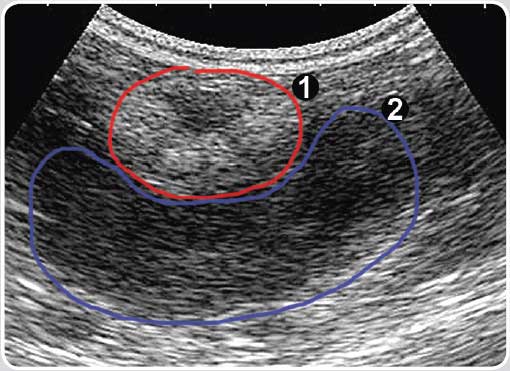
| Фото 3.1. УЗИ. Левая почка. Поликистоз |
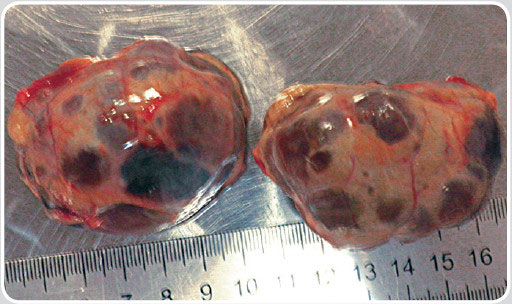 |
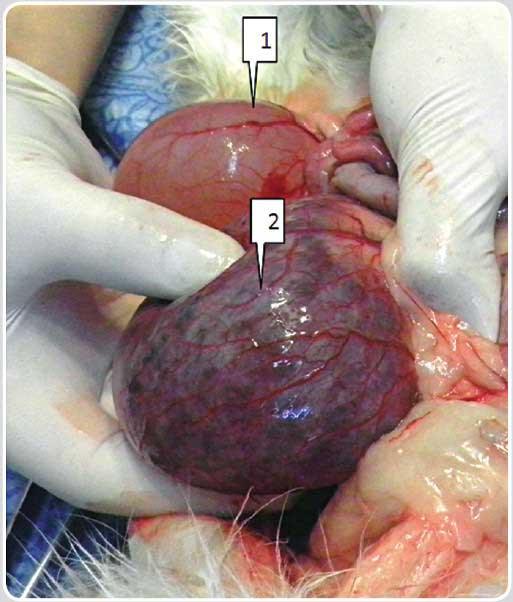
| Фото 3.2. Аутопсия. Левая и правая почки. Поликистоз |
 |
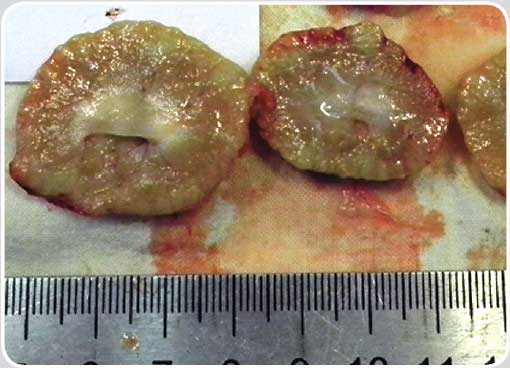
| Фото 3.3. Аутопсия. Левая почка в продольном разрезе. Поликистоз |
При УЗИ почек оценивают следующие параметры:
- форму (в норме бобовидная), контуры (в норме ровные и чёткие) и эхогенность различных слоёв паренхимы (в норме у почечной паренхимы и структур — смешанная эхогенность), а также размеры (обычно в сравнении друг с другом);
- положение почек;
- наличие границы между корковым и мозговым слоем (которая определяется по линии, проведённой через основание почечной пирамиды) и в норме параллельна внешнему контуру почки;
- толщина и площадь паренхимы, а также соотношение её к площади ЦЭ;
- структурные изменения, включая диффузные или очаговые изменения эхогенности, наличие конкрементов и очаговых образований;
- строение лоханки и её состояние: толщина и структура стенок, а также наличие в её полости включений и дополнительных структур;
- оценка почечного кровотока (с использованием метода Доплера) для выявления некоторых видов новообразований.
Важным при проведении ультрасонографии почек является не только класс, но и корректная настройка прибора, на котором проводится исследование. Так, например, при повышенной контрастности изображения возможно визуальное уравнивание эхогенности коркового и мозгового слоёв или пирамидок и гипоэхогенных структур и лоханки.
Почки у собак и особенно у кошек имеют длинную брыжейку, вследствие чего относительно легко перемещаются в брюшной полости. Так, например, при наполненном желудке они могут смещаться каудальнее, а во время беременности — краниальнее. Кроме того, у многих пациентов (особенно не страдающих ожирением и находящихся в медикаментозном сне) почки хорошо пальпируются, и их легко можно приблизить к брюшной стенке. У некоторых кошек даже удаётся проводить исследование, зафиксировав почку между пальцами (фото 2). Это обстоятельство и то, что эти органы имеют характерное, легко «узнаваемое» при визуализации строение, делает выведение их изображения на экран не очень сложной задачей.
Отсутствие подвижности почек встречается при значительном увеличении их размеров, а также при отёках, выраженном фиброзе или воспалительных процессах как в перинефральном пространстве, так и в самих этих органах.
С поверхности со всех сторон почка покрыта плотной неэластичной капсулой, которая визуально представляет собой тонкую гиперэхогенную мембрану (различимую только на аппаратах экспертного класса). Почки также окружены рыхлой гипоэхогенной жировой клетчаткой, которая неплотно примыкает к капсуле. Толщина паранефральной клетчатки зависит от степени упитанности животного, и у котят и щенков выражена слабо. Степень расширения полости почечной лоханки в норме может незначительно меняться и зависит от наполненности мочевого пузыря и степени гидратации организма.
У собак и кошек наилучшая визуализация почек достигается при проведении исследования в положении пациента лёжа на спине, а также на левом и правом боках. Сканирование проводят в промежутке между последними рёберными дугами (направляя датчик краниально под них) и поясничной областью вплоть до малого таза, располагая трансдуктор продольно, косо или поперечно. Сканирование обязательно должно быть полипозиционным, что является непременным условием для корректной оценки всей толщи органа и его структур.
В продольном сечении почки, которое обычно визуализируется при расположении датчика в передне-задней (сагиттальной) плоскости, хорошо различимы:
- почечный синус, или ЦЭ, — наиболее гиперэхогенная (благодаря высокому содержанию фиброзной ткани) часть почки;
- мозговое вещество почки — гипоэхогенный слой, который полукругом облегает лоханку, а на своей внешней границе вплотную граничит с корковым слоем;
- корковое вещество почки — изоэхогенный наружный слой, местами как бы выпячивающийся в мозговой; сверху корковый слой покрыт плотной и неэластичной фиброзной капсулой.
Сосудистые пучки вторичной микрокапиллярной сети и дуговые вены (которые проходят на границе коркового и мозгового слоёв) визуально делят почечную паренхиму на отдельные части (которые, однако, являются единой анатомической структурой). Почечная пирамида и, соответственно, почечный сосочек у этих видов животных один.
Когда не удаётся обнаружить одну из почек в типичном месте, необходимо проведение полипозиционного сканирования всех сегментов брюшной полости для исключения различных видов дистопии. Если в результате всё равно не удаётся её обнаружить, необходимо проведение урографии для подтверждения аплазии.
Длину и толщину почки измеряют при продольно-косом сканировании, слегка изменяя положение датчика и стараясь получить изображение наибольшей длины органа. Ширину почки оценивают при поперечно-косом сканировании через область почечного синуса и ворот. Измерив длину и ширину почки, можно вычислить её объём, используя для этого соответствующие измерительные программы ультразвукового аппарата.
Визуализация надпочечников у собак и кошек в большинстве случаев затруднена, поскольку эти железы внутренней секреции имеют одинаковую эхогенность с паранефральной жировой клетчаткой.
Факторы, учитываемые при оценке эхогенности почечной паренхимы
Достоверным критерием уменьшения массы функционирующей паренхимы является не абсолютная её толщина, а соотношение площади паренхимы к площади ЦЭ, которое в норме составляет 2 и более (фото 4.1). Эхогенность центрального комплекса почки растёт при повышении содержания в нём соединительнотканных компонентов (возрастные изменения) и снижается при отёке её клетчатки, например, при пиелонефрите. Лоханка почки в норме — анэхогенная структура.
Эхогенность коркового слоя (особенно у кошек, благодаря липидным вакуолям в клетках эпителия проксимальных канальцев) выше эхогенности почечной пирамиды. Существенное различие эхогенности коркового и мозгового слоёв почки является нормой и описывается в протоколе УЗИ как сохранённая кортико-медуллярная дифференциация.
Эхогенность паренхимы почек обычно сравнивают с эхогенностью печени и селезёнки (табл. 4). Однако не следует забывать, что паренхима этих органов также может находиться в изменённом состоянии (воспаление, липидоз, диффузные опухолевые поражения, возрастные изменения и т.д.), что требует от врача, проводящего исследования, сопоставление большого числа изображений, среди которых принять за константу нельзя ни одно. Это на порядок осложняет проведение исследования и может серьёзно повлиять на его объективность. Кроме того, установление прямой связи между диффузными изменениями эхогенности паренхимы почек и конкретными патологическими процессами на нынешнем этапе развития медицинской техники невозможно.
Таблица 4. Эхогенность паренхимы почек у собак и кошек в сравнении с эхогенностью паренхимы печени и селезёнки в норме и при патологии
| Степень изменения |
Эхо-структура |
| Норма | Эхогенность паренхимы почки сопоставима с эхогенностью паренхимы печени и несколько ниже эхогенности паренхимы селезёнки. |
| I | Эхогенность паренхимы почки равна эхогенности паренхимы селезёнки. |
| II | Эхогенность паренхимы почки выше эхогенности паренхимы селезёнки, но ниже ЦЭ почки. |
| III | Эхогенность паренхимы почки равна эхогенности ЦЭ почки. |
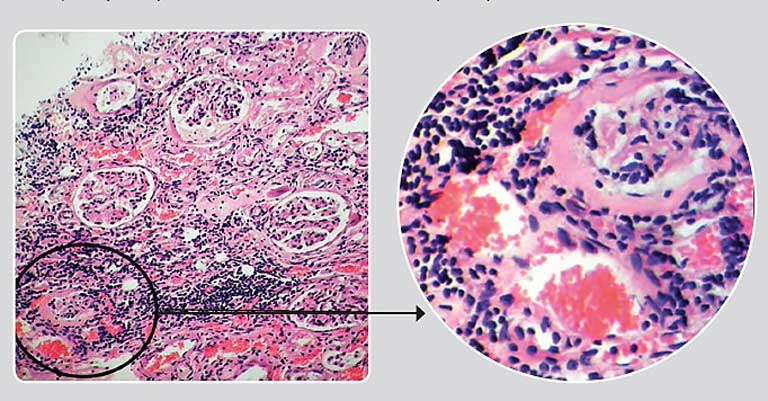
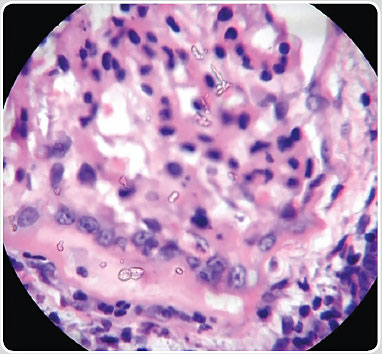
Поэтому дифференциация патологического процесса в почечной паренхиме (склероз, фиброз, гиалиноз, инфильтрация клетками воспаления, атрофия канальцев и т.д.) и тем более определённых нозологических форм (различные формы ГН, ТИН и т.д.) на основании эхогенности почечных структур не проводится или носит условный характер. Тем более что при гистоморфологическом исследовании тканей почек у собак и кошек, особенно страдающих хроническими протекающими нефропатиями, часто отмечается сочетание нескольких из перечисленных патологических процессов (фото 5.4, 5.5 и 5.6).
До определённой степени УЗИ диффузных изменений эхогенности паренхимы почек может помочь в определении длительности течения нефропатии у конкретного пациента. Если в корковом слое почки имеются признаки диффузного поражения, а кортико-медуллярная дифференциация паренхимы хорошо сохранена, то, скорее всего, речь идёт об остром процессе. При отсутствии кортико-медуллярной дифференциации паренхимы и наличии диффузных изменений как в корковом, так и мозговом слоях следует прежде всего предполагать хроническую нефропатию (хронические формы ГП, ГН и ТИН) на заключительном этапе своего течения (фото 4).
В протоколе исследования при обнаружении изменений эхогенности паренхимы почек необходимо указать: УЗИ-признаки структурных изменений паренхимы (коркового и/или мозгового слоёв) с сохранённой или нарушенной кортико-медуллярной дифференциацией или УЗИ-признаки структурных изменений почек, если помимо паренхимы в процесс вовлечены и структуры ЦЭ.
Если при УЗИ отмечаются признаки пиелонефрита (расширение почечной лоханки и огрубение её контуров, очаговые поражения мозгового слоя) или пионефроза (очаговые поражения паренхимы почек различной эхогенности с неровными краями), то в протоколе указывают УЗИ-признаки пиелонефрита или пионефроза. Однако диагноз считается подтверждённым только в том случае, если в корректно полученной (путём чрезбрюшинного уроцистоцентеза) моче выделяют патогенную микрофлору[6].
Гидронефроз
При гидронефрозе моча первоначально застаивается и накапливается в лоханке, в результате чего происходит её расширение (пиелоэктазия), а позже возникает компрессия всей почечной паренхимы. Если препятствие не устраняется длительное время, процесс может закончиться скоплением мочи под капсулой почки и в околопочечной клетчатке (уринома).
Гидронефроз (обычно односторонний) развивается вследствие препятствия току мочи в мочеточнике на любом уровне в результате обструкции его опухолями, сгустками, некротизированными и отторгнутыми сосочками или конкрементами. К гидронефрозу также приводят аномалии мочеточников и лоханки, рефлюксы (обратный ток мочи по мочевому тракту), опухоли предстательной железы или мочевого пузыря и нарушение оттока мочи из лоханки вследствие сдавливания извне лимфатическими узлами или опухолями.
Односторонний гидронефроз (или двухсторонний с частично сохранённым оттоком мочи, при котором наблюдается пиелоэктазия от лёгкой до средней степени) у собак и кошек не проявляется характерными клиническими признаками. Владельцы могут отмечать лишь ухудшение аппетита или анорексию, астению и болезненность в области живота. В результатах лабораторной диагностики также могут отсутствовать выраженные изменения (особенно при одностороннем гидронефрозе из-за компенсаторных возможностей контралатеральной почки). Стадии и возможные исходы гидронефроза приведены в схеме 1.
Схема 1. Стадии и исходы гидронефроза
Методика УЗИ мочевого пузыря
В самой каудальной части брюшной полости расположен хорошо визуализируемый при УЗИ (особенно в наполненном состоянии) полый орган — мочевой пузырь. При затруднении оттока мочи через уретру мочевой пузырь может увеличиваться до значительных размеров и занимать даже большую часть брюшной полости. В мочевом пузыре различают тело и шейку, переходящую в мочеиспускательный канал. Острая задержка мочи, наиболее часто возникающая по причине мочекаменной болезни, может привести к уремии и вызвать постренальную ПН. А незаполненный мочевой пузырь может свидетельствовать об анурии (особенно если внутривенное введение петлевых диуретиков не привело к его наполнению в течение 30–60 минут). Поэтому пальпация и визуализация на УЗИ мочевого пузыря является неотъемлемой частью обследования животных с подозрением на заболевания почек.
Для детального осмотра мочевого пузыря необходимо, чтобы он был в наполненном состоянии. Без этого невозможно оценить ни толщину его стенок (увеличивающуюся, например, при уроцистите), ни наличие новообразований, конкрементов и другой гиперэхогенной взвеси в его полости. Если в мочевом пузыре отсутствует достаточное количество мочи, возможно его наполнение стерильным физиологическим раствором NaCl или 0,02% раствором фурацилина. Последний, однако (особенно при неправильном приготовлении, когда кристаллы антисептика не полностью растворились в воде), может вызвать появление экзогенной гиперэхогенной взвеси и исказить получаемое изображение. Этот метод также незаменим при подозрении на разрыв мочевого пузыря (одна из причин постренальной ПН). При этом во время введения раствора хорошо видно, что мочевой пузырь не наполняется и жидкость вытекает в брюшную полость.
Введение уретрального катетера в сам мочевой пузырь у особей мужского пола нежелательно из-за вероятности травмирования и обсеменения слизистой уретры (которое может привести к сужению и без того узкого её просвета и затруднению микции). Во избежание этого катетер вводят в мочеиспускательный канал всего на одну четверть. У котов и кобелей мелких пород для этого вообще целесообразнее использовать катетеры для периферических вен G22-G24. После введения катетера необходимо пережать половой член ближе к головке и под давлением ввести раствор в мочевой пузырь. У особей женского пола уретра короткая и значительно более широкая, поэтому катетер у них во время этой процедуры необходимо вводить непосредственно в сам мочевой пузырь.
Мочеточники у собак и кошек визуализировать при УЗИ (особенно у некрупных животных) удаётся редко. Исключения могут составить случаи, когда в краниальной четверти мочеточника (расположенной ближе к мочевому пузырю) находятся конкременты или сам мочеточник сильно расширен из-за гидронефроза.
Ультразвуковые доплерографические исследования (УДИ) пока не нашли широкого применения в ветеринарной нефрологии. И дело здесь не только в высокой стоимости оборудования, которое для УДИ необходимо.
В медицине при обследовании нефрологических больных УДИ в подавляющем большинстве случаев используется для двух целей:
1) диагностики обильно кровенаполненных новообразований почек и/или паранефрального пространства;
2) тромбоэмболии и/или атеросклероза сосудов почки и связанных с ними ишемии или инфарктов паренхимы.
Но если опухоли с обильным кровоснабжением (достаточным для обнаружения при помощи метода Доплера) иногда встречаются у собак и кошек, то вторая группа заболеваний совершенно не характерна для этих видов животных.
Иногда визуализация изменений кровотока в паренхиме почек используется как косвенное доказательство определённых диффузных или очаговых поражений паренхимы. Однако проведение таких исследований доступно пока только на очень дорогих аппаратах, да и получаемые при этом изображения не имеют однозначной интерпретации. И так же, как в случае с оценкой изменений эхогенности паренхимы, не могут использоваться для окончательной верификации конкретных патологических изменений в паренхиме или выставления окончательных нефрологических диагнозов.
Урография
Морфофункциональный ВМД, основанный на избирательной способности почек выделять путём фильтрации внутривенно введённые водорастворимые йодсодержащие рентгенопозитивные вещества. Оптимальными препаратами (в силу значительно меньшей токсичности) для использования при урографии у мелких домашних животных является йогексол («Омнипак», «Юнигексол»), йопромид («Ультравист») и йодиксанол («Визипак»).
Урография довольно широко используется в ветеринарной нефрологии, хотя и имеет ряд существенных ограничений (табл. 1). Также нужно отметить, что проведение урографии целесообразно только после того, как пациенту было проведено УЗИ и сделаны обзорные рентгеновские снимки МВС.
Вместе с тем урография является наиболее ценным методом, позволяющим определить у пациента обструкцию или разрыв мочеточников. При этом на снимках, сделанных через 10–30 минут после введения контраста (которое может осуществляться на фоне использования петлевого диуретика торсемида), отчётливо видно, что моча либо останавливается в мочеточнике, не достигнув мочевого пузыря, либо попадает в брюшную полость. При разрыве же мочевого пузыря на фоне чётко прослеживающихся мочеточников видно, что моча не накапливается в нём, а выходит в брюшную полость.
Важным для получения качественных снимков при урографии является введение достаточного количества рентгеноконтрастного препарата и заблаговременное очищение кишечника от каловых масс и газов при помощи голодной диеты, слабительных веществ, очищающих клизм и ветрогонных средств (симетикон).
Для оценки морфологических особенностей строения почек и в составе комплексной диагностики постренальной ПН снимки при внутривенной урографии делают сразу после введения контрастного вещества, затем через 1–3 минуты, а также через 5, 10 и 20 минут [17]. Однако для оценки возможности почек (или одной из них) образовывать мочу[7], а также для оценки морфофункционального состояния почек животных, у которых по клинико-лабораторным данным можно либо предположить снижение уровня скорости клубочковой фильтрации (СКФ), либо была диагностирована ПН (в этом случае урография проводится только по жизненным показаниям), рентгеновские снимки делают сразу после введения контраста (фаза сосудистой нефрограммы), затем через 10, 30 и 60 минут (фаза экскреторной пиелограммы), а также через 2, 4 и даже 12 часов. В норме рентгеноконтрастное вещество отчётливо должно регистрироваться в почечной лоханке уже через 10–15 минут после внутривенного введения и большей частью выделиться почками в составе мочи в течение двух-четырёх часов.
При развитии аллергических реакций или даже анафилактического шока после инъекции рентгеноконтрастного препарата внутривенно вводят раствор тиосульфата натрия, стероидные гормоны (метилпреднизолон, преднизолон) и форсируют диурез с помощью кристаллоидов (Рингег-Лактат, раствор Хартмана и т.д.) и петлевых диуретиков (фурасемид, торасемид).
Литература
- Adin CA, Herrgesell EJ, Nyland TG, Hughes JM, Gregory CR, Kyles AE, Cowgill LD, Ling GV. Antegrade pyelography for suspected ureteral obstruction in cats: 11 cases (1995–2001). J Am Vet Med Assoc. 2003 Jun 1;222(11):1576–81
- Barrs VR, Gunew M, Foster SF, Beatty JA, Malik R. Prevalence of autosomal dominant polycystic kidney disease in Persian cats and related-breeds in Sydney and Brisbane. Aust Vet J. 2001 Apr;79(4):257–9.
- Beck C, Lavelle RB. Feline polycystic kidney disease in Persian and other cats: a prospective study using ultrasonography. Aust Vet J. 2001 Mar;79(3):181–4.
- Biller DS, DiBartola SP, Eaton KA, Pflueger S, Wellman ML, Radin MJ. Inheritance of polycystic kidney disease in Persian cats. J Hered. 1996 Jan-Feb;87(1):1–5.
- Bouma JL, Aronson LR, Keith DG, et al. Use of computed tomography renal angiography for screening feline renal transplant donors. Vet Radiol Ultrasound 2003; 44(6): 636–641.
- Burk RL, Feeney DA. Small Animal Radiology and Ultrasonography, A diagnostic Atlas and Text, 3rd Ed., W.B. Saunders Co, St. Louis 2003.
- Claudio Brovida. Canine and Feline Proteinuria: Diagnostic Approach and Management in the Dog and Cat. 29th World Congress protocols of WSAVA. Rhodes, Greece 2004.
- Daniel GB, Berry CR: Renal Scintigraphy. In: Textbook of Veterinary Nuclear Medicine, Ed. Twardock AR, Bahr A. 2006; 18: 329.
- Dibartola SP, Rutgers HC. Diseases of the kidney. In: The Cat Diseases and Clinical Management. Ed. Sherding RG, Churchill Livingstone 1989: 2: 1353–1395.
- Domanjko-Petric A, Cernec D, Cotman M. Polycystic kidney disease: a review and occurrence in Slovenia with comparison between ultrasound and genetic testing. J Feline Med Surg. 2008 Apr; 10(2):115–9.
- G. Javier Del Angel Caraza. Deciding the Medical Management of the Patient with Urolithiasis. 30th World Congress protocols of WSAVA. Mexico City, Mexico.
- Harkin KR, Biller DS, Balentine HL. Glomerulocystic kidney disease in a kitten. J Am Vet Med Assoc. 2003 Dec 15; 223(12):1780–2, 1778.
- http://my.erinet.com/~lebordo/PKD/pkdfaq.html#HowDiagnosed
- http://www.iris-kidney.com
- Kealy K, McAllister H. Diagnostic Radiology and Ultrasonography of the Dog and Cat. 4th Ed., Elsevier Saunders, 2005.
- Larry D. Cowgill. Acute Renal Failure in the Dog and Cat: Causes and Outcomes. 28th World Congress protocols of WSAVA. Bangkok, Thailand, 2003.
- Lavin, Lisa M. Radiography in Veterinary Technology / Edition 4. Elsevier Health Sciences, 2006
- Mareschal A, dʹAnjou MA, Moreau M, Alexander K, Beauregard G. Ultrasonographic measurement of kidney-to-aorta ratio as a method of estimating renal size in dogs. J Vet Radiol Ultrasound. 2007 Sep-Oct;48(5):434–8.
- Mareschal A, dʹAnjou MA, Moreau M, Alexander K, Beauregard G. Ultrasonographic measurement of kidney-to-aorta ratio as a method of estimating renal size in dogs. Vet Radiol Ultrasound. 2007 Sep–Oct; 48(5):434–8.
- Novellas R, Espada Y, Ruiz de Gopegui R. Doppler ultrasonographic estimation of renal and ocular resistive and pulsatility indices in normal dogs and cats. Vet Radiol Ultrasound. 2007 Jan-Feb;48(1):69–73.
- Nyland TG, Mattoon JS. Small Animal Diagnostic Ultrasound, 2nd edition, W.B. Saunders and Saunders, Ohio 2001.
- OʹLeary CA, Turner S. J Chronic renal failure in an English bull terrier with polycystic kidney disease. Small Anim Pract. 2004 Nov;45(11):563–7.
- Reichle JK, DiBartola SP, Leveille R. Renal ultrasonographic and computed tomographic appearance, volume, and function of cats with autosomal dominant polycystic kidney disease. Vet Radiol Ultrasound 2002; 43(4): 368–373.
- Stephen DiBartola. Selected Diseases of the Feline Kidney. 26th World Congress protocols of WSAVA. Vancouver, B.C., Canada – 2001.
- Takiguchi M, Inaba M. Diagnostic ultrasound of polypoid cystitis in dogs. J Vet Med Sci. 2005 Jan; 67(1):57–61.
- Tony Buffington. Feline Lower Urinary Tract Disorders (Session 1). 26th World Congress protocols of WSAVA. Vancouver, B.C., Canada – 2001.
- Walter PA, Johnston GR, Feeney DA, et al. Applications of ultrasonography in the diagnosis of parenchymal kidney disease in cats: 24 cases (1981–1986). J Am Vet Med Assoc 1988: 192(1): 92–98.
- Yamazoe K, Ohashi F, Kadosawa T, et al. Computed tomography on renal masses in dogs and cats. J Vet Med Sci 1994; 56(4): 813–816.
СВМ № 3/2012
[1] Доклинический (неазотемический) этап течения нефропатии может занимать до 90% времени почечного континуума.
[2] Лейкоцитурия и протеинурия, например, характерны для большинства форм гломерулонефритов, тубуло-интерстициальных патий и инфекционных заболеваний почек.
[3] Термин «чашечно-лоханочная система почек» (ЧЛС), обычно используемый в этом случае в медицине, не всегда может быть применим в ветеринарии, поскольку у собак и кошек, например, почки однососковые, и чашечки как анатомическая структура отсутствуют.
[4] В нефрологии в подавляющем большинстве случаев диагнозы, выставленные на основании неинвазивных методов диагностики (за исключением, пожалуй, пиелонефритов, пионефрозов и других инфекционных процессов, при которых моча теряет свою стерильность), считаются клиническими или предварительными. Диагностика ГП, ГН, ТИН и других хронических асептических нефропатий, как и определение более конкретной нозологической формы заболевания (например, мезангиопролиферативный ГН), осуществляется только после гистоморфологического исследования тканей почки.
[5] У кошек и собак абсцессы почек возникают обычно в результате гемато- или лимфогенного распространения патогенов на фоне выраженных иммунодефицитных состояний.
[6] Лейкоцитурия также является только косвенным признаком инфекционных нефропатий, поскольку встречается, например, и при асептически протекающих ГП и ГН.
[7] Способность концентрировать мочу, скорость клубочковой фильтрации и другие функциональные показатели работы почек при урографии оценить нельзя.