Наталья Пашинцева, к. б. н., ветеринарный клинический патолог ветклиники «Биоконтроль», pashintseva2009@yandex.ru
Анастасия Становая, ветеринарный врач-онколог ветклиники «Биоконтроль», stasyakiss@mail.ru
Ксения Лисицкая, к. б. н., ветеринарный врач, ветеринарный клинический патолог ветклиники «Биоконтроль», lisksenia@mail.ru
Резюме
Наиболее распространёнными причинами появления выпотных жидкостей в грудной полости у собак являются септический процесс, метастатические поражения и идиопатический хилоторакс, в то время как геморрагический выпот встречается редко. Гемоторакс может развиваться при врождённых и приобретённых коагулопатиях, отравлении родентицидами, наличии диафрагмальной грыжи, а также при различных травмах и нарушении целостности артерий и вен в грудной полости. Геморрагические выпоты могут быть связаны с новообразованиями в грудной полости, такими как гемангиосаркома, мезотелиома и другие образования в средостении. Кроме того, у молодых собак описаны острые идиопатические кровотечения в грудной полости, наиболее часто возникающие в ткани тимуса. В статье описан клинический случай кровотечения в грудную полость у 19-месячной собаки породы карело-финская лайка, ассоциированного с выраженной регрессией ткани тимуса и возникновением геморрагий. Рассмотрены основные причины и описаны основные морфологические изменения, происходящие в ткани тимуса и способствующие развитию кровотечений в краниальном средостении.
Введение
Гемоторакс — это наличие свободной жидкости в грудной полости, гематокрит которой составляет не менее 25% (по некоторым данным не менее 50%) от гематокрита венозной крови [1, 2]. Геморрагический выпот у собак может накапливаться при патологиях вторичного гемостаза, таких как наследственные или приобретённые коагулопатии, редко при нарушении первичного гемостаза, а также при различных травмах. Примерно в 50% гемоторакс образуется при опухолевом процессе. Злокачественные мезенхимальные опухоли, такие как гемангиосаркома, остеосаркома и другие образования средостения, способствуют развитию гемоторакса. Инвазируя межрёберные сосуды или некротизируясь, они провоцируют вторичное кровотечение в грудной полости [3]. Интересно, что причины развития гемоторакса, не связанные с вышеперечисленными патологиями, часто остаются неустановленными [1]. Спонтанный геморрагический выпот описан также при мезотелиоме, некоторых формах гельминтозов, в частности, сердечной форме дирофиляриоза и спироцеркозе, а также при перекруте доли лёгкого [4, 5].
Клинические признаки гемоторакса связаны со снижением общего объёма циркулирующей крови и наличием патологического объёма свободной жидкости в грудной полости. Могут наблюдаться угнетённое состояние, слабый пульс, учащённое сердцебиение и дыхание, бледность слизистых оболочек, кашель, реже коллапс.
После обнаружения свободной жидкости в грудной полости методами визуальной диагностики, следующим этапом является её цитологическое исследование, которое необходимо для дальнейшей дифференциальной диагностики [6]. Препараты, выполненные из геморрагического выпота, характеризуются большим количеством эритроцитов и небольшим количеством лейкоцитов, могут быть представлены макрофаги с эритрофагоцитозом, продукты деградации гемоглобина (гемосидерин, гематоидин). Обнаружение тромбоцитов, расположенных отдельно или в агрегатах, является признаком ятрогенной контаминации материала кровью, а также признаком сверхострого кровотечения на фоне травматизации крупного сосуда или органа, богатого эритроцитами (например, селезёнка или печень). Для установления этиологического фактора требуется сопоставление результатов цитологического исследования с анамнезом, клиническими симптомами и данными, полученными при помощи методов визуальной диагностики.
Описание клинического случая
На приём к онкологу поступила собака породы карело-финская лайка возрастом 1 год 7 месяцев, некастрированный самец в состоянии средней тяжести, с отказом от корма и бледностью слизистых оболочек. На рентгеновском снимке органов грудной клетки, выполненном в другом ветеринарном учреждении, контуры сердца были нечёткие, что характерно для плеврального выпота. В биохимическом и общеклиническом анализах крови не было выявлено отклонений. При ультразвуковом исследовании, проведённом в день обращения в клинику «Биоконтроль», в грудной полости определялись свободная жидкость и округлое гипоэхогенное образование в средостении, краниальнее сердца с чёткими контурами размером 58 × 50 мм. При торакоцентезе было аспирировано около 600 мл геморрагической выпотной жидкости, цитоз которой составлял 16,0 тыс. кл/мкл, а концентрация общего белка составляла 46 г/л. Необходимо отметить, что гематокрит выпотной жидкости составлял 36%, тогда как в венозной крови он был 22,1%. В цитологических препаратах содержались в небольшом количестве недегенеративные нейтрофилы, попавшие с кровью, а также в значительном количестве эритроциты и агрегаты тромбоцитов. Клетки злокачественного новообразования и микроорганизмы обнаружены не были. Данная выпотная жидкость соответствовала геморрагическому выпоту, ассоциированному со сверхострым кровотечением.
При оценке гемостаза было отмечено удлинение протромбинового времени (ПТ) до 48,6 сек. (норма: 5–10 сек.) и активированного частичного тромбинового времени (АЧТВ) до 109,6 сек. (норма: 10–15 сек.). Пациенту была выполнена гемотрансфузия в объёме 350 мл свежей цельной крови, после которой отмечалось значительное улучшение ментального статуса и была проведена повторная оценка вторичного гемостаза, при которой ПТ составляло 6,2 сек., а АЧТВ — 23,2 сек.
После стабилизации состояния пациенту была выполнена рентгеновская спиральная компьютерная томография (КТ) органов грудной полости. При анализе пространственных реформатов в трёх плоскостях в нативном режиме и с контрастным усилением в плевральной полости определялось около 250 мл жидкостного содержимого, не накапливающей контрастное вещество, плотностью 25–30 единиц Хаунсфилда (HU), что соответствовало жидкости экссудативного типа, вероятно, с достаточно густой консистенцией. Кроме того, в краниальном средостении в проекции тимуса визуализировалось объёмное образование неправильной формы размером 49 × 48 × 24 мм мягкотканной плотности (40–50 HU) с множественными полостями, неоднородной структуры с чёткими, неровными контурами, слабо накапливающее контрастное вещество. КТ-картина, наиболее вероятно, соответствовала гемотораксу с крупной гематомой в проекции краниального средостения (рис. 1).
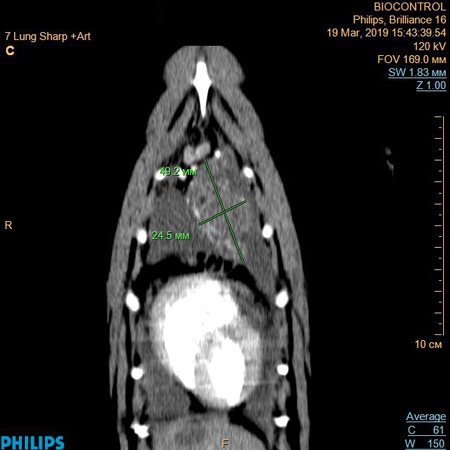 |
Рис. 1. Результат компьютерной томографии с использованием контраста, дорсовентральное положение. Линиями отмечены размеры новообразования средостения мягкотканной плотности (40–50 HU). Левее визуализируется свободная жидкость |
Методами визуальной диагностики достоверно нельзя было исключить опухолевый процесс краниального средостения, а также абсцесс или гранулёму, в связи с чем из описанного выше образования под контролем КТ была выполнена тонкоигольная аспирационная биопсия (ТИАБ).
Цитологические препараты, полученные из образования в средостении, содержали небольшое количество недегенеративных нейтрофилов, попавших с кровью, единичные вспененные макрофаги, клетки реактивного мезотелия, обильное количество эритроцитов и агрегатов тромбоцитов (рис. 2). Данная цитограмма имела низкую диагностическую значимость и соответствовала неспецифическому слабому макрофагальному воспалению с выраженной гемодилюцией. Для дальнейшей верификации было рекомендовано гистологическое исследование.
А 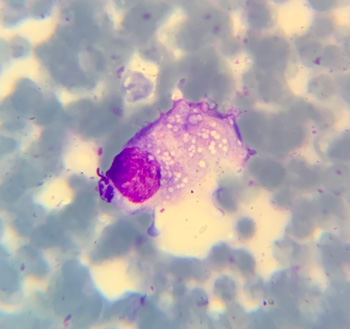 Б Б 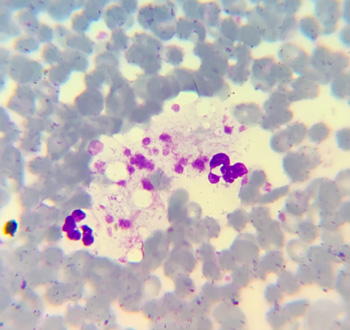 |
| Рис. 2. Цитологическая картина образования средостения: А — крупная клетка с эксцентричным округлым ядром и обильной вспененной цитоплазмой, морфология которой соответствует макрофагу; Б — агрегаты тромбоцитов и два недегенеративных нейтрофила, попавших с кровью |
С учётом данных КТ и по результатам цитологического исследования у пациента в первую очередь было предположено наличие гематомы в краниальном средостении, вероятнее всего, локализующейся в тимусе. Удовлетворительный ментальный статус и отсутствие накопления свободной жидкости в грудной полости не исключали риск развития повторного кровотечения, которое могло бы привести к летальному исходу, в связи с чем пациенту была проведена диагностическая торакотомия. Согласно протоколу операции, при осмотре грудной полости был выявлен тимус до 5 см в диаметре, рыхлой консистенции с подкапсульными множественными кистозными образованиями. Остальные органы краниального средостения без особенностей, свободная жидкость в грудной полости не определялась. Выполнена тимэктомия с последующим гистологическим исследованием.
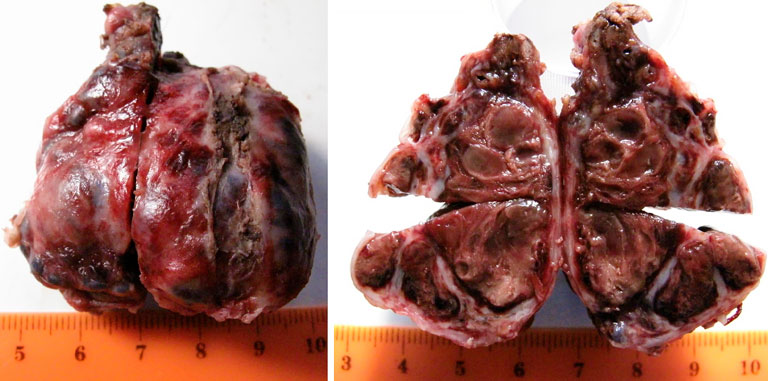
При макроскопическом исследовании капсула тимуса имела тёмный цвет. На разрезе определялись множественные соединительнотканные прослойки толщиной около 0,1–0,2 см, разделяющие ткань на округлые доли. Около 60% площади патологического очага было представлено гематомами, около 30% — некрозами. Остальная ткань имела очаги полнокровия (рис. 3А, Б).
А 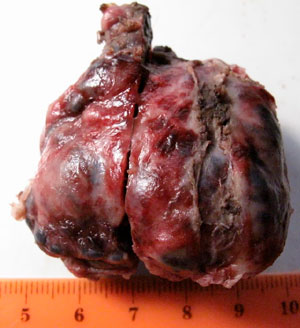 Б Б 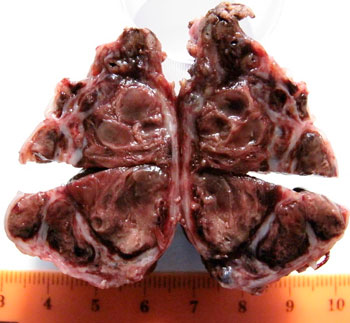 |
| Рис. 3. Макроскопическая картина образования краниального средостения у собаки. А — внешний вид удалённого тимуса; Б — вид тимуса на разрезе |
При гистологическом исследовании в исследуемых биоптатах была представлена коллагенизированная умеренная строма, в которую было погружено умеренное количество веретеновидных клеток с плохо или умеренно различимыми границами, скудным или умеренным количеством эозинофильной цитоплазмы, овальными нерезко полиморфными ядрами среднего размера с зернистым хроматином (рис. 4А). Митозы в пределах популяции веретеновидных клеток не выявлялись. Многоочагово в биоптатах были представлены резко расширенные кровеносные сосуды, заполненные эритроцитами и фибриновыми тромбами, местно распространённые массы фибрина, смешанные с эритроцитами, инфильтраты из малых лимфоцитов и гистиоцитов, цитоплазма последних заполнена коричневым пигментом (наиболее вероятно, гемосидерин) (рис. 4Б). Согласно заключению патолога, биоптаты содержали фиброзную строму с местно распространёнными подострыми геморрагиями и венозной гиперемией.
А 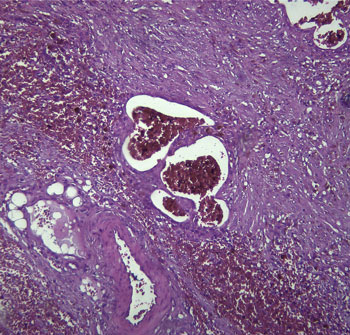 Б Б 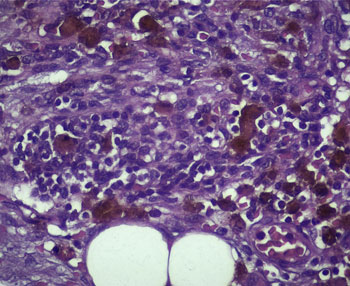 |
| Рис. 4. Гистологическое исследование ткани тимуса (согласно направлению и данным операционного протокола). А — коллагенизированная строма с погруженными в неё веретеновидными клетками и резко расширенные кровеносные сосуды, заполненные эритроцитами и фибриновыми тромбами; Б — лимфоцитарные инфильтраты и гистиоциты в ткани |
На основании проведённого обследования у пациента была диагностирована гематома тимуса с сопутствующим сверхострым кровотечением в грудную полость. После тимэктомии животное находилось в отделении реанимации и интенсивной терапии в течение 3 дней до стабилизации клинического состояния. На момент публикации статьи период наблюдения за животным после операции составил 3 месяца. Со слов владельцев, животное клинически здорово, рецидивы за всё время не наблюдались.
Обсуждение
Идиопатические, или спонтанные, кровотечения в области тимуса у собак встречаются редко, однако в большинстве случаев носят фатальный характер [7]. Возраст большинства собак, у которых диагностируется эта патология, варьирует от 3 до 9 месяцев и редко превышает 2 года. Породная и половая предрасположенности в исследованиях не выявлены. Возможными предрасполагающими факторами возникновения кровотечений в краниальном средостении могут быть автомобильная травма, нарушение целостности магистральных сосудов (аневризма аорты или сонной артерии), опухолевый процесс (гемангиосаркома, лимфома), однако в большинстве случаев этиологический фактор не определяется. Интересно, что при отравлении родентицидами очаги спонтанных кровотечений склонны формироваться в тимусе и переднем средостении [8, 9].
В одной из ранее опубликованных работ были описаны кровотечения в грудной полости у молодых собак, вызванные разрывом аневризмы аорты, непосредственно в области клапана или в области дуги аорты, а в преобладающем большинстве (80% случаев) они локализовались в области тимуса и окружающих его тканях [10]. Необходимо отметить, что летальность в этом исследовании достигала 100%, и все включённые в исследование собаки погибали внезапно от резко развившегося гиповолемического шока, а максимальная продолжительность одышки составляла не более одного дня до момента летального исхода. Наличие геморрагического выпота в грудной полости отмечалось в большинстве случаев.
В литературе описано как минимум две гипотезы патогенеза идиопатических тимических геморрагий у молодых собак, причём каждая основывается на том, что перед началом жизнеугрожающего кровотечения происходит инволюция тимуса. Так, по одной из них, регрессия ткани тимуса сопровождается снижением контрдавления на истончённые стенки венозных сосудов со стороны окружающей их жировой и рыхлой соединительной ткани, что при внезапном повышении кровяного давления приводит к нарушению целостности сосудистой стенки и развитию сильного кровотечения. Согласно второй теории, разрыв сосудов в регрессирующей ткани тимуса может возникать даже при незначительном механическом воздействии на область шеи, например, при чрезмерном натяжении ошейника при резкой остановке собаки [10].
Инволюция тимуса является нормальным запрограммированным необратимым явлением, которое начинается постепенно после полового созревания в возрасте около 6–12 месяцев [11]. Морфологически она проявляется потерей (апоптозом) лимфоцитов кортикального слоя, исчезновением нормальной кортико-медуллярной дифференцировки, инфильтрацией органа жировой тканью (рис. 5А). В дальнейшем инволюции подвергаются сосуды тимуса, их стенка становится склерозированной, что в норме предотвращает развитие кровотечений [10].
А 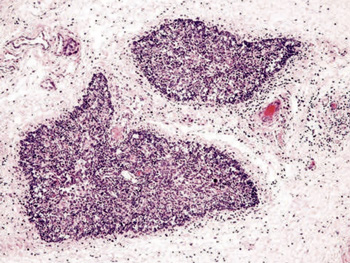 Б Б 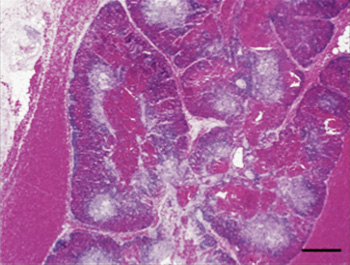 |
| Рис. 5. А — инволюция тимуса. Апоптоз лимфоцитов кортикального слоя, истончение кортекса, потеря кортико-медуллярной дифференцировки с хорошо выраженной междольковой перегородкой. Окраска гематоксилином и эозином [14]; Б — тимическое кровотечение у щенка 3 месяцев при отравлении родентицидами. Обширные области геморрагий, расширяющие междольковые септы тимуса, кортекс и медуллярный слой. Окраска гематоксилином эозином [9] |
В ходе дифференциальной диагностики идиопатических геморрагий тимуса необходимо исключить кровотечения, вызванные интоксикацией родентицидами с последующим нарушением коагуляции. В данном клиническом случае при исследовании вторичного гемостаза отмечалось значительное удлинение ПТ и АЧТВ, что соответствовало недостатку факторов внешнего и внутреннего пути коагуляции. Такие изменения коагулограммы у собак, действительно, характерны для отравления родентицидами [12]. Учитывая отсутствие других клинических симптомов, свойственных подобной форме интоксикации и нехарактерной гистологической картине исследованного патологического очага, нарушения свёртываемости крови у пациента, наиболее вероятно, соответствовали коагулопатии разведения, ассоциированной с ранее предшествующим тяжёлым кровотечением в грудную полость [13].
При гистологическом исследовании тимической гематомы, ассоциированной с отравлением родентицидами (рис. 5Б), в дольках и междольковой соединительной ткани тимуса выявляются геморрагии различной степени. Капсула органа перерастягивается, поражённые доли в различной степени теряют нормальную архитектонику, наблюдается снижение количества лимфоидных клеток кортикального и мозгового слоёв, некроз эпителиальных клеток [9]. По периферии располагается дольки тимуса обычного строения, что не соответствует гистологической картине инволюции тимуса [7].
Интересно, что идиопатические тимические геморрагии могут возникать раньше, чем наступление у пациента возраста, характерного для начала запрограммированной инволюции органа. Так, в одном из исследований, только у 6 из 18 собак с тимическими гематомами наблюдалась выраженная регрессия тимической ткани. В остальных случаях геморрагии были локализованы преимущественно в соединительнотканных септах и в мозговом слое с полным нарушением структуры последнего, тогда как кортикальный слой тимуса оставался интактным [10]. На основании этих данных можно предположить, что идиопатические гематомы в краниальном средостении ассоциированы не только с процессом инволюции тимуса, но и с его атрофией, которая может возникать при целом ряде предрасполагающих факторов, таких как неправильное питание и кахексия, дефицит витамина В6 и жирных кислот, различные интоксикации, применение лекарственных препаратов, инфекционные заболевания — вирус чумы собак, парвовирус собак, микотоксины. Сходными, но обратимым эффектами, обладает развитие стресс-состояния у животного с повышением уровня глюкокортикостероидов в крови.
В описанном клиническом случае гистологические препараты не содержали ткань тимуса нормального строения (рис. 4), срезы содержали фиброзированную строму с многоочаговыми геморрагиями, а лимфоидные клетки были разбросаны в срезах в виде маленьких островков. Вероятно, данная гистологическая картина может соответствовать тимической ткани в состоянии субтотальной регрессии, а учитывая локализацию описанного патологического очага, вовлечение тимуса остаётся наиболее вероятным. Интересно, что по данным визуальной диагностики, как при ультразвуковом исследовании, так и при КТ, патологическая ткань тимуса имела сходные с опухолевым процессом признаки.
Несмотря на опубликованные данные о высокой вероятности летального исхода у собак с тимическими геморрагиями, в описанном клиническом случае пациент с образованием в средостении не погиб после тяжёлого кровотечения в грудную полость, а клинические признаки развивались постепенно в течение двух дней. С другой стороны, в литературе всё же имеются упоминания о том, что не все собаки с описанной патологией погибают после возникновения однократно развившегося кровотечения [15]. В описанных случаях в патологических очагах тимуса выявлялись признаки хронических геморрагий и формирование грануляционной ткани, что говорит о наличии предшествующего кровотечения. Вероятно, все эти данные указывают на то, что эпизоды кровотечений могут иметь различную степень выраженности, что обуславливает различную степень риска летального исхода. Тактика лечения пациентов в каждом случае выбирается индивидуально [15]. Тимические геморрагии могут рецидивировать, что не позволяет в ряде случаев ограничиться консервативной терапией гемостатическими средствами, и поэтому показано хирургическое удаление тимуса.
Заключение
В данной статье описан клинический случай гемоторакса у молодой собаки, ассоциированный с острым кровотечением в краниальном средостении. Одной из наиболее вероятных причин его развития являлась инволюция тимуса, при которой просвет крупных кровеносных сосудов этого органа расширяется, их стенка становится более тонкой и хрупкой. При малейшем физическом воздействии целостность таких кровенаполненных сосудистых пространств может нарушиться и привести к тяжёлому, в большинстве случаев летальному кровотечению. Основными дифференциальными диагнозами являлись опухолевый процесс, в частности, гемангиосаркома, и отравления родентицидами. Опухолевый процесс был исключён при помощи гистологического исследования. Несмотря на то, что содержимое желудка не исследовалось на наличие родентицидов, интоксикация этими веществами маловероятна в связи с нетипичной клинической картиной заболевания и быстрым восстановлением активности факторов свёртывания в крови после однократной процедуры гемотрансфузии без терапии витамином К1, применение которого показано при таком типе интоксикации [16].
При выявлении гемоторакса у молодых собак необходимо помнить, что кровотечения в краниальном средостении могут носить острый характер, а причина их развития может быть не связана с опухолевым процессом. Тимус, особенно в стадии инволюции или атрофии, является одним из органов, крайне чувствительных к любым механическим воздействиям, резким скачкам артериального давления и отравлениям родентицидами, воздействие которых приводит к развитию острых геморрагий.
Литература
- Nakamura R.K., Rozanski E.A., Rush J.E. Non-coagulopathic spontaneous hemothorax in dogs. J Vet Emerg Crit Care. 2008;18:292–297.
- Mellanby R.J., Villiers E., Herrtage M.E. Canine pleural and mediastinal effusions: a retrospective study of 81 cases. J Small Anim Pract. 2002;43:447–451.
- Feeney D.A., Johnston G.R., Grindem C.B. Malignant neoplasia of canine ribs: clinical, radiographic and pathologic findings. J Am Vet Med Assoc. 1982;180:927–933.
- Morrison W.B., Trigo F.J. Clinical characterization of pleural mesothelioma in 7 dogs. Comp Cont Ed. 1984;6:342–348.
- Valenciano A.C., Cowell R.L. Cowell and Tyler's Diagnostic Cytology and Hematology of the Dog and Cat. 2014. 4th Ed.
- Watton T.C., Lara-Garcia A., Lamb C.R. Can malignant and inflammatory pleural effusions in dogs be distinguished using computed tomography? Vet Radiol Ultrasound. 2017;58:535–541.
- Liggett A.D., Thompson L.J., Frazier K.S., Styer E.L., Sangster L.T. Thymic hematoma in juvenile dogs associated with anticoagulant rodenticide toxicosis. J Vet Diagn Invest. 2002;14:416–419.
- Valli V.E.O.: 1993, The hematopoietic system. In: Pathology of domestic animals, ed. Jubb KVF, Kennedy PC, Palmer N, 4th ed. vol. 3, pp. 233, 264. Academic Press, San Diego, CA.
- Williams L.J., Buchweitz J.P., Rissi D.R Pathology in practice. Severe thymic hemorrhage. J Am Vet Med Assoc. 2014;244:905–907.
- Van der Linde-Sipman J.S., van Dijk J.E. Hematomas in the Thymus in Dogs. Vet Pathol. 1987:2459–2461.
- Cunningham J.G.: 1997, Textbook of veterinary physiology, 2nd Ed. WB Saunders, Philadelphia, PA.
- Vangrinsve E., Gommeren K. Thymic haemorrhage due to ingestion of human anticoagulant medication in a puppy. Vet Rec Case Rep. 2017;5:1–4.
- Haas T., Mauch J., Weiss M., Schmugge M. Management of Dilutional Coagulopathy during Pediatric Major Surgery. Transfus Med Hemother. 2012;39:114–119.
- Jubb, Kennedy, and Palmer’s pathology of domestic animals / edited by M. Grant Maxie. Sixth edition. 2016.
- Мальцева А.Н. Анестезиологическое пособие при геморрагическом шоке на фоне спонтанного кровотечения тимуса. Клинический случай. VetPharma. 2018;5:4–45.
- Park C., Lim C.Y., Kim J.H., Jang J.I., Park H.M. Successful therapy of coumatetralyl rodenticide induced pericardial effusion with pericardiocentesis in a dog. Can Vet J. 2011;52:165–168.
СВМ № 4/2019